腦網絡組圖譜提出后,歐盟人腦計劃(Human Brain Project, HBP)第一時間將其收錄。此外,國際著名神經影像分析軟件,如SPM等,也將腦網絡組圖譜作為主要人類腦圖譜提供給用戶使用。
雷鋒網《醫健AI掘金志》消息,近日,第四屆圖像計算與數字醫學國際研討會(ISICDM 2020),在遼寧省沈陽市的東北大學國際學術交流中心舉辦。
中科院自動化所的蔣田仔教授以《The Human Brainnetome Atlas and its Applications in Understanding of Brain Functions and Disorders》為題作大會報告。
蔣田仔教授是歐洲科學院外籍院士、我國腦網絡組研究中心主任、腦網絡組重點實驗室主任,同時也是IEEE Fellow、IAPR Fellow以及AIMBE Fellow。
他主要從事的領域包括多模態跨尺度腦網絡組圖譜研究、基于腦網絡圖譜的腦機融合和腦疾病早期預測和精準治療。
以下為蔣田仔教授的大會報告內容。經授權,《醫健AI掘金志》作了不改變原意的編輯和整理:
蔣田仔:大家好,今天報告的題目叫《腦網絡組圖譜及其在腦認知與腦疾病方面的應用》,將分為以下幾個方面:
首先,介紹什么是腦網絡組圖譜,接著重點介紹怎么繪制并驗證圖譜,以及圖譜的應用和對未來的展望。
在講腦網絡組圖譜之前,首先要講一下什么叫腦網絡組。

所謂腦網絡組(brainnetome)是由兩個基本要素構成,一是網絡的節點(node),二是節點跟節點的連接(connection)。
腦網絡組至少可以從三個不同的尺度進行定義和研究:節點為神經元(neuron)的微觀尺度、節點為神經元群的介觀尺度(mesoscale)、節點為腦區的宏觀尺度。
從微觀尺度看,人腦有1011個神經元和1015個連接,所以如果要從微觀尺度研究全腦是不可能的,至少以目前的計算資源是無法做到的。以后如果出現量子計算機什么的才有可能。
更小的規模就是介觀尺度。介觀尺度以目前的算力和計算水平也達不到全腦研究的要求。
今天要講的主要是宏觀尺度。宏觀尺度就是連接腦區,在腦區跟腦區之間可以定義解剖連接(anatomical connectivity)、功能連接(functional connectivity)等等。
我認為腦網絡組至少包括以下五個方面的研究內容。
第一個方面是網絡的拓撲結構;
第二個方面是網絡的動態變化規律;
第三個方面是不同的腦功能,如功能異常在網絡上是怎么表征的;
第四個方面是一些特定的網絡。如跟智力、注意等相關的網絡是否有遺傳基礎;
第五個方面是對網絡進行仿真與建模;
如果大家對腦網絡組有興趣,可以去看我于2013年發表在《NeuroImage》上的一篇文章《Brainnetome:A new -ome to understand the brain and its disorders》,里面詳細介紹了什么叫腦網絡組,以及一些腦網絡組研究的基本內容。
下面再回到今天的主題,腦網絡組圖譜。
我認為所謂的腦圖譜繪制,某種意義上就是圖像處理。它是在尋找具有不同特性的腦區之間的邊界,某種意義上就是一種圖像分割。

最早的圖譜叫Brodmann圖譜。目前而言,該圖譜是腦認知及腦疾病研究中使用得比較多的圖譜。
Brodmann圖譜主要是基于細胞構筑進行繪制的腦圖譜。
細胞構筑的意思就是看細胞的形狀。這一片跟那一片的形狀長得很類似,他們認為就在同一個腦區;這一片跟另一片在形狀上有明顯的不同,他們就認為在不同的腦區。這就是Brodmann圖譜繪制的基本思想。
Brodmann把皮層分成了52個不同的區域。現在看來,這個分區是非常粗糙的,而且有好多邊界其實是錯的。
1996年前后,德國于利希研究中心(Forschungszentrum Jülich)下面的神經科學與醫學研究所(Institute of Neuroscience and Medicine)就是想改造Brodmann圖譜。
這個研究所用的思想跟Brodmann是完全一樣的,還是把去世后的人捐獻的腦袋切成一片片,然后染色,看每一片上面的邊界在什么地方,再將它組成三維的。
這項研究從1996年到現在,二十多年過去了,盡管已經在《Science》上發表了兩篇文章,但仍然沒有完成全腦圖譜的繪制。
因為有一些腦區的細胞構筑比較復雜,很容易就能把它分成不同的類型;但還有一些腦區的細胞類型非常一致,這樣的腦區,如果完全基于細胞構筑的話,是沒辦法區分開的。
2010年左右,我們開始醞釀中國的973項目,設想的第一件事就是要用五年左右的時間重新繪制一個腦圖譜。
當時如果完全沿用國外原有的腦圖譜繪制思想是不可能完成的。因為國外做了那么長時間都沒有完成,我們怎么可能五年就能完成。
所以我們走了一條完全不一樣的道路。
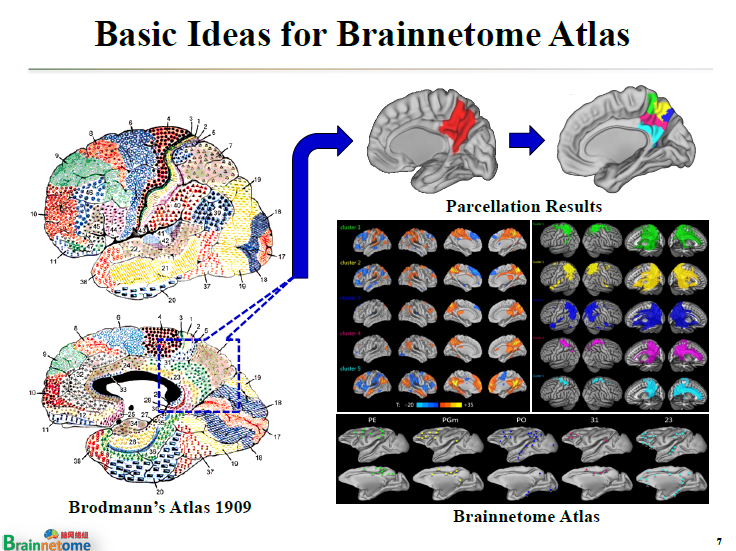
圖像處理相關領域的人應該都了解,腦圖像的基本單元不是一個個細胞,到不了那個程度。腦圖像的基本單位并不是細胞,而是體素。二維圖像的最小單位是像素,三維的最小單位就是體素。
腦圖像跟其他圖像有一個本質的區別,那就是腦圖像的每一個體素都可以定義跟全腦其他體素之間的連接。所以只要拿一個體素出來,就可以定義它在全腦的連接,即所謂的連接模式(Connectivity Profile)。
有了這個東西以后,就可以比較體素和體素之間的連接模式是否一樣。連接模式一樣的話,那么它們就在同一個區域里;不一樣的話,就在不同的腦區。
這就是腦網絡組圖譜繪制的最基本的思想。
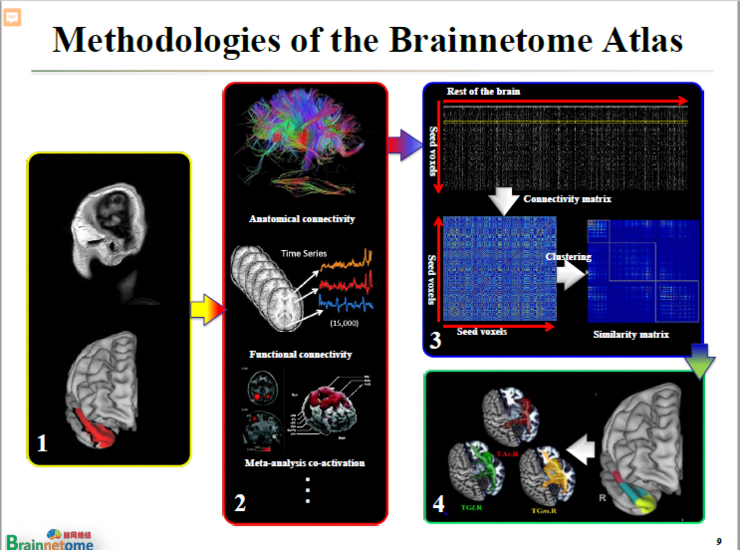
首先,需要有人的磁共振圖像以及結構像。如果要進一步定義連接模式,除了結構像以外,我們還需要用于定義解剖連接的彌散磁共振成像,以及可以定義功能連接的功能磁共振成像。
經過反復的論證,我們認為只有解剖連接才有可能作為繪制圖譜的工具。
由于功能連接會受各種各樣的因素影響,尤其是時間因素——早上跟晚上采集的,功能上有可能也不一樣,這種隨時間動態變化的東西,是沒辦法用于繪制圖譜的。所以我們使用的是彌散磁共振成像。
我們花了大概兩年時間——由于不同的腦區有著不一樣的特性,繪制全腦的圖譜還是面臨著很多挑戰——建立了腦圖譜繪制的框架。有了這個框架以后,就可以對不同的腦區進行劃分。
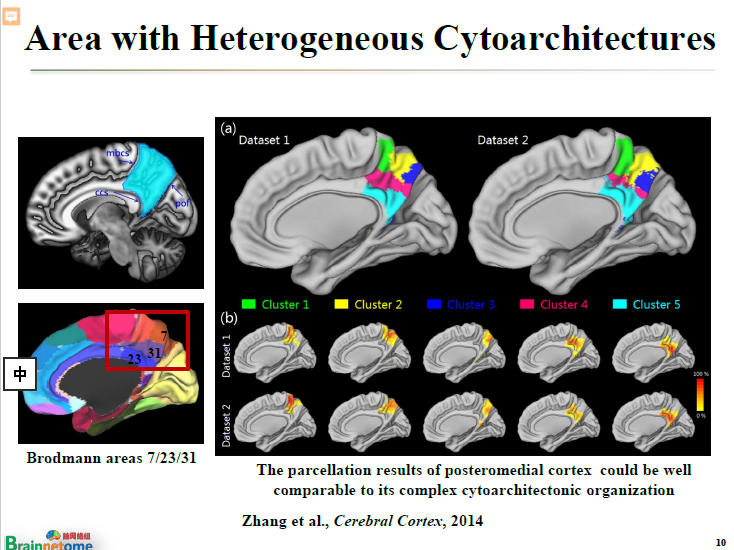
像內后皮質(posteromedial cortex)這個區域(左上圖藍色部分)的細胞構筑非常復雜,用細胞構筑去區分腦區是沒有任何問題的。但是剛才說了,我們希望能夠走另外一條道路。
所以,我們基于彌散磁共振成像來看這個區域跟前額的連接,把它建立起來以后,發現這個腦區可以分成五個不同的亞區。
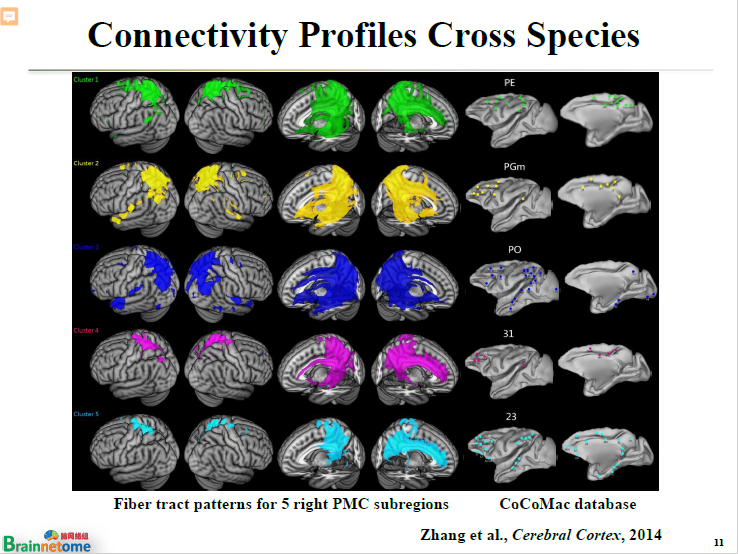
這個方法跟傳統的方法相比有一個最大的好處,就是不僅能夠提供分區——這是傳統腦圖譜繪制的最終目標,還能夠提供每一個亞區跟全腦其他腦區之間的連接模式——這個就叫連接圖譜。
所謂腦網絡組圖譜,就是比以前更加精細的分區,加上每一個腦區跟全腦區來連接的連接圖譜。我們不叫它腦圖譜,這個意義也就在這個地方。
這個例子就告訴我們,傳統的基于細胞構筑的方法能做的事情,腦網絡組圖譜也能做。但是腦網絡組圖譜能夠提供更多的信息。這個信息就是連接圖譜。這是第一點。
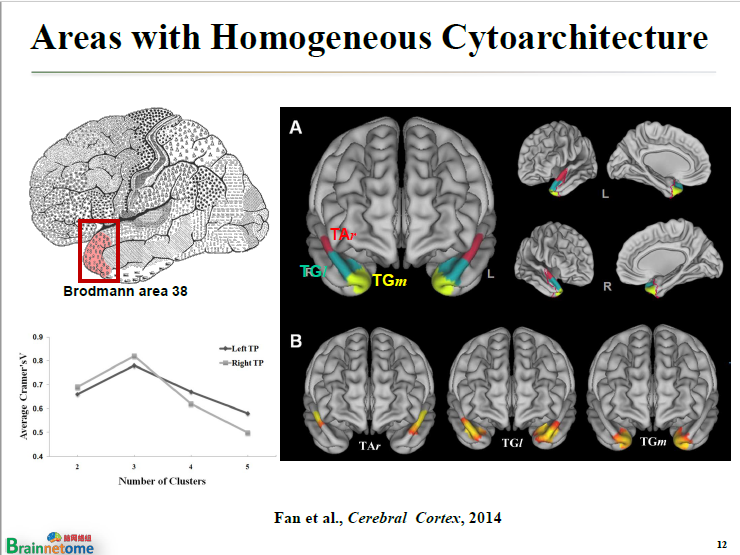
對于一些細胞構筑比較單一的腦區,如顳極這個區域就可以利用連接模式,把它分成三個不同的亞區。這三個不同亞區的連接模式是完全不一樣的。
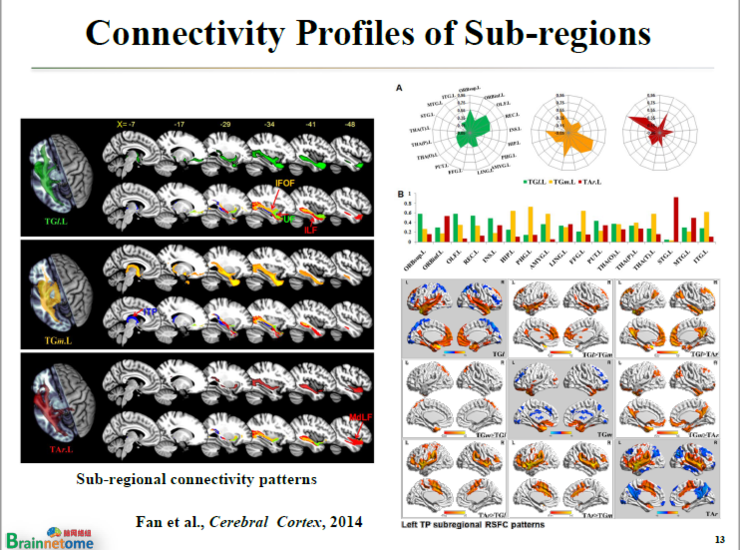
這就是功能連接模式的指紋圖,這三個不同的亞區跟全腦的連接完全不同。我們不光可以定義它的解剖連接,也可以基于三個亞區定義它的功能連接。
這個例子說明,傳統的方法,即完全基于細胞構筑去做分區的方法是區分不開的,但是利用連接模式就可以把它分成不同的亞區。傳統方法做不到的事情,我們能夠做到。
我們在2016年完成了對全腦的皮層和皮層下的分區。皮層分成210個不同的亞區,皮層下分成了36個不同亞區,加在一起就是246個不同亞區。這就是腦網絡組圖譜的分區結果。
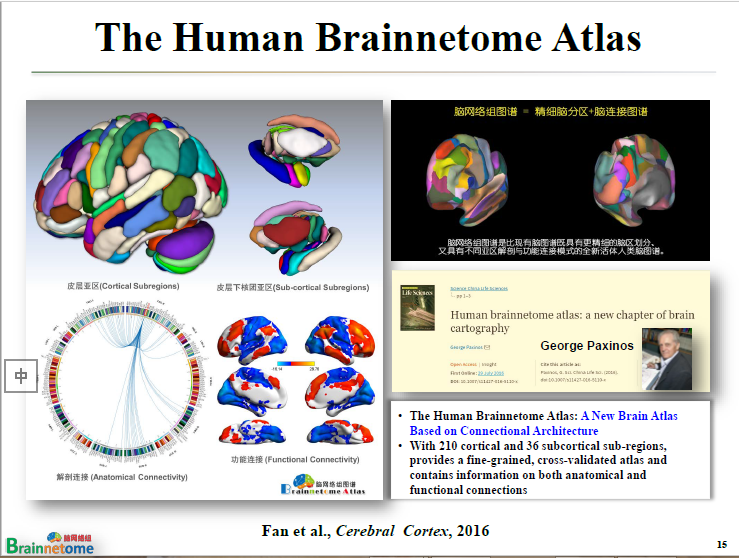
左邊這個圖的下方和右邊最上方提示的就是連接圖譜。
圓環,就是相當于把246個亞區放在一個圓環上面,點擊任何一個亞區就能夠展示跟全腦其他地方是怎么連接的。包括右邊那個可以動來動去的圖,也可以展示不同亞區的連接模式是什么樣的。
這個工作出來以后在國際上引起了一些非常重要的反響。George Paxinos就認為腦網絡組圖譜實際上開辟了腦圖譜繪制的新篇章。

現在,腦網絡組圖譜相關的軟件也已經開放共享給國內外相關研究領域的科研人員和臨床醫生免費使用。
腦網絡組圖譜出來以后,歐盟人腦計劃(Human Brain Project, HBP)第一時間就將它收錄到了平臺里面。此外,一些國際著名神經影像分析軟件,如SPM,也將腦網絡組圖譜作為主要人類腦圖譜提供給用戶使用。
接下來介紹怎么驗證這個圖譜是合理的。主要是從三個層面驗證。

第一個最簡單的就是跨模態比較(Cross-modality Comparison)。比如說用DTI(磁共振彌散張量成像)技術定義解剖連接模式得出的結果,和用功能連接、細胞構筑或其他模態得出的分區結果是否一致?
第二個層面是從遺傳機制這個全新的角度去證明其合理性。
第三個層面是最重要的,即能否基于連接模式預測腦區的功能在什么地方。比如說進行記憶任務時會激活某些區域,而如果基于解剖連接就能預測哪個地方會被激活,這就更上一個層次了。
先從第一個層面給大家介紹不同模態之間怎么去驗證。
這個驗證的背景在于,腦區的劃分有基于細胞構筑的,有基于解剖連接的,有基于功能連接的等等。那么,這些不同的劃分方式是否能夠得出一樣的分區結果?
如Broca區(布羅卡皮層區)基于細胞構筑已經區分出了很多腦區,那么再用解剖連接進行劃分,得出來的結果跟基于細胞構筑區分出的結構是否一樣?
我們發現結果非常一致。
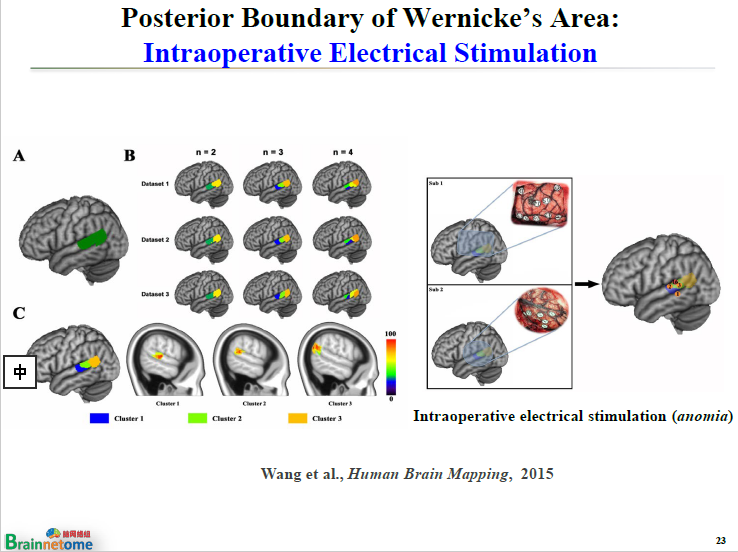
此外,也可以基于連接模式把Wernicke's area(韋尼克區)分成三個不同的亞區,然后再通過術中電刺激(Intraoperative Electrical Stimulation)刺激每一個亞區,看哪些亞區是跟語言有關的,或者去看不同亞區的功能是否一樣。這也是一種驗證方式。
除了皮層上面的腦區可以用跨模態驗證,皮層下的腦區也可以,如伏隔核(nucleus accumben)。用三種不同的成像模式所獲得的伏隔核的分區結果是完全一樣的。
第二個層面的驗證則基于遺傳相關性。這方面在人和動物上已經有了一些突破性的進展。
2011年,《NEURON》上發表了一篇文章,里面利用了雙生子進行計算。同卵雙生的遺傳系數是1,異卵的則為0.5。
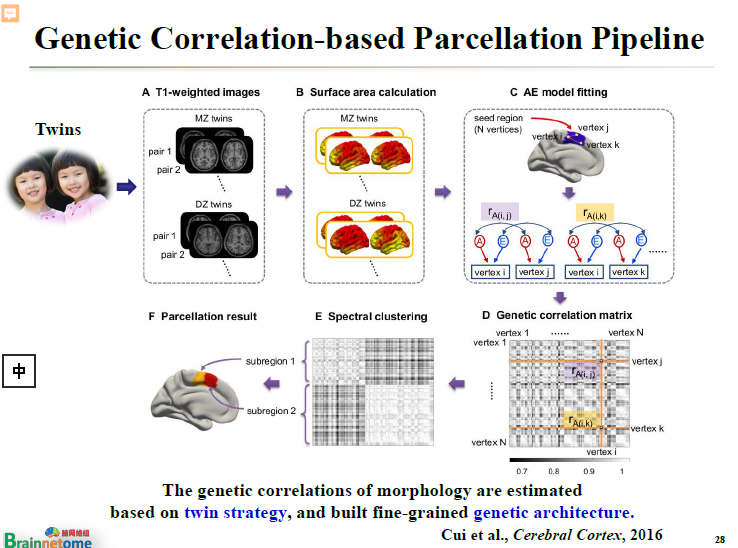
這就是所謂的雙生子模型。
雙生子模型是怎么做的呢?先提取人的皮層,進行三角剖分。每一個三角片都可以算出一個面積。因為三角片不是等三角片,有大有小,這樣就可以把每個頂點作為節點,然后用一個模型去算遺傳相關系數。
所謂遺傳相關系數,就是以三角形的頂點作為節點重新劃分皮層,得到一個遺傳相關矩陣(Genetic correlation matrix),在這上面去聚類,就可以把不同的亞區聚在不同的類里面。
這種方式既沒有用到連接模式,也沒有用到細胞構筑,但分區的結果跟基于連接模式得出的結果幾乎是完全一樣的。
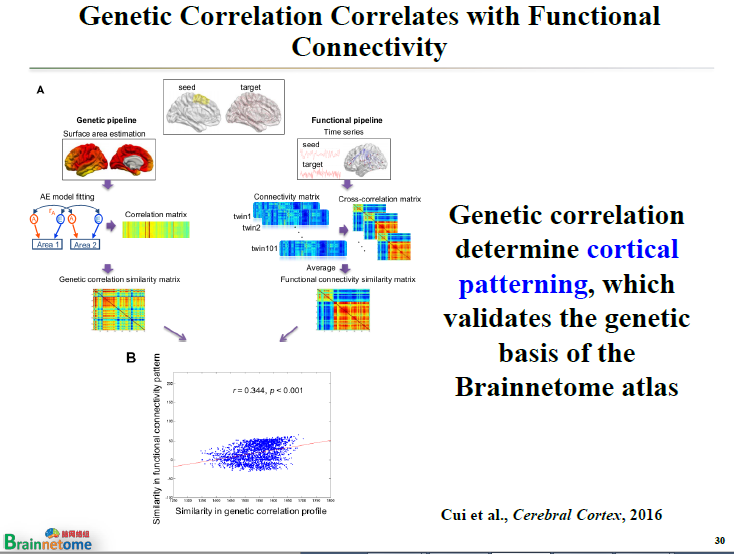
這就說明邊界的形成,即patterning,可能先天就是如此,后天也許會有一些改變,但那些改變在大尺度上可能是微不足道的。這是另外一種驗證方式。
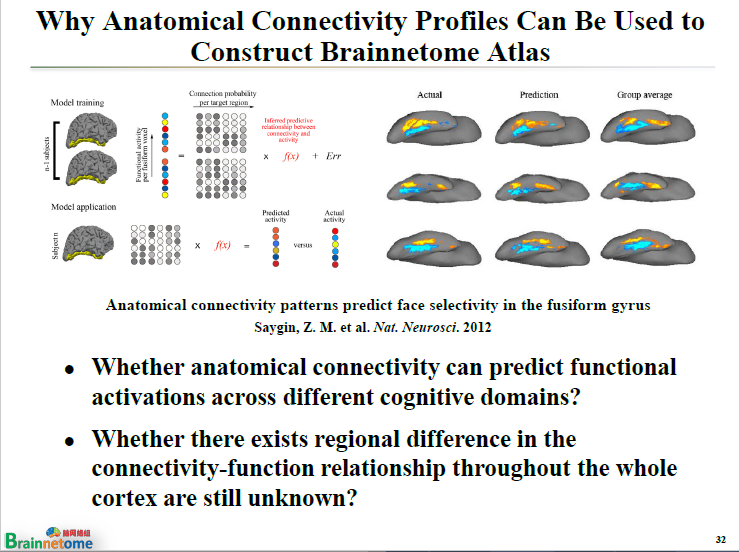
第三個層面,基于連接模式,甚至能夠預測人在進行某種任務時大腦所激活的區域。
我們不是第一個提出來的,我們只是想用這個方式去驗證它。
2012年《NAT NEUROSCI》上有一篇文章表示,基于DTI的解剖連接能夠預測一些非常簡單的區域,如面孔識別的區域,特別是梭狀回。識別面孔時,大腦的哪個區域會被激活?如果基于彌散磁共振成像所獲得的解剖連接同樣能夠預測到哪個地方有激活,這就很有意思了。
但更為關鍵的問題是,現在已經能夠預測一個腦區,那么全腦的其他功能區域能不能預測?
第二個非常關鍵的問題是,現在只是能夠預測一些很簡單的腦區,如動手指、識別面孔等等,那么對于像工作記憶(workingmemory)這樣的區域——復雜且激活的是多個腦區,能否進行預測?如果能夠預測,不同腦區的預測效果是否一樣?
為了解決這個問題,我們利用了一個跟機器學習有關的非常重要的模型。
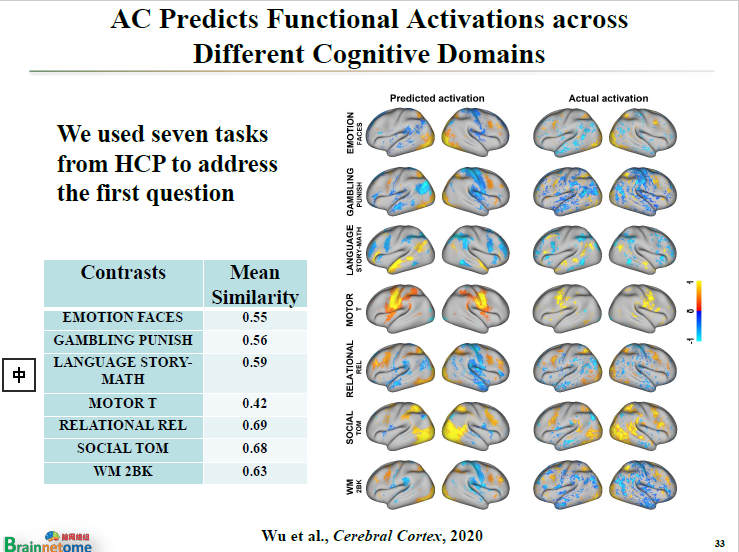
研究使用的是美國Human Connectome Project(HCP,人腦連接組計劃)的數據,里面提供了七個不同的任務,有工作記憶、體育、社會相關的、語言的等等,每個任務都會導致一些腦區的激活。
我們列出了兩列數據,一列是用解剖連接預測出來的結果,一列是真實的激活組。兩組數據一比較,幾乎是一模一樣的。所以第一個結論就是,任何一個任務都可以用彌散磁共振成像提供的解剖連接的方式進行預測。
如果能夠預測到,預測的效果是否一樣?為了判斷這個問題,我們定義了一種指標,Connectivity-function Relationship(CFR),用于刻畫預測精度。

CFR這樣一個量,它在全腦的分布是否一樣?也就是說,兩個完全不同的腦區,比如說聯合皮層跟感覺運動皮層,即一些復雜的皮層跟簡單一點的皮層相比較,它是一樣?還是不一樣?我們就發現不同腦區的CFR實際上是不一樣的。
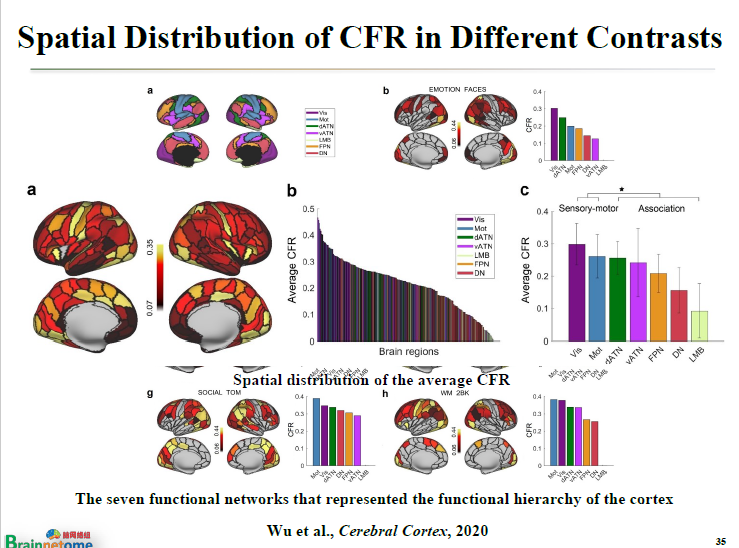
CFR不僅不一樣,還有一個層級結構,即越簡單的腦區,預測的精度就越高。按照從簡單到復雜的順序,把這七個任務相關的腦網絡進行排序,可以發現和視覺、運動相關的網絡的CFR指標很高,即預測的精度很高。
CFR指標會隨著從簡單到復雜的網絡,呈現出從高到低,逐步遞減的趨勢。
而這樣的層級結構,其分布方式跟大腦本身的很多生物學意義是完全一致的。
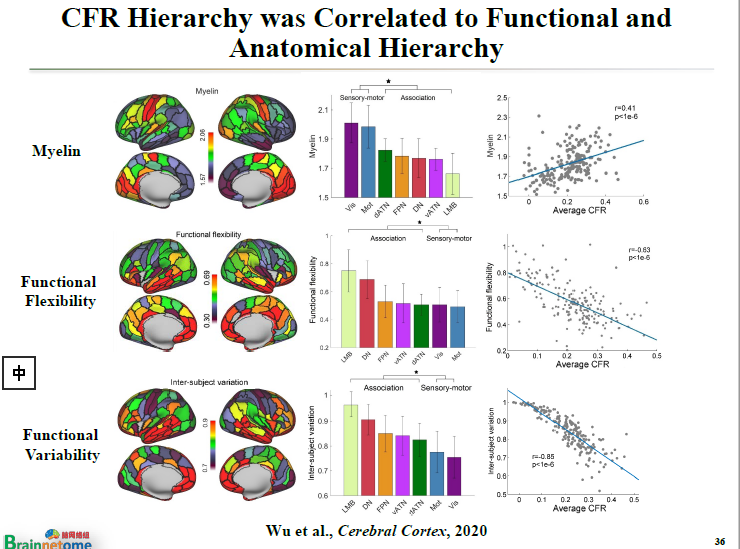
比如Myelin(髓磷脂),就是說髓鞘化功能的靈活性、個體之間的功能差異,也有這樣一種從簡單到復雜、CFR指標從高往低的排序過程。CFR指標跟它有非常好的對應關系。
大家如果對這個問題感興趣,可以看看我們最近剛發表在《CEREBRAL CORTEX》上的一篇文章。

下面再講幾個應用的例子。
第一,通過腦網絡組圖譜可能會發現一些新的腦區。
第二,與抑郁癥有關。我們發現男女在調節情緒方面使用的是完全不同的網絡。
第三,腦網絡組圖譜可能會給疾病的診斷或治療帶來一些全新的觀點。
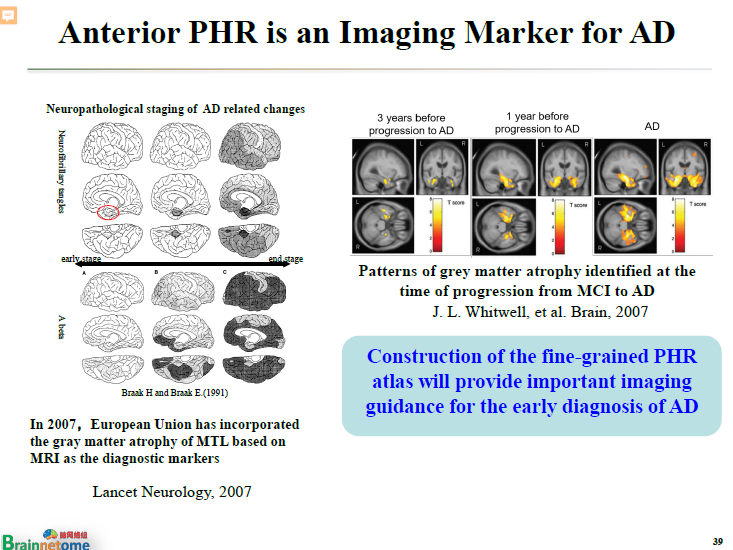
第一個應用以旁海馬腦區(lateral parahippocampal region)為例。
為什么以旁海馬為例呢?主要是因為這個跟老年癡呆有關。
像心理疾病、AD(阿爾茲海默癥)這樣的精神類疾病,影像到底能在多大程度上幫助醫生進行診斷?這方面的知識實際上非常有限。盡管文章發了很多,但要應用到臨床還是非常困難的。
但旁海馬這個腦區,包括內側顳葉、腦皮質的萎縮可以用于輔助診斷AD。早在2007年,歐盟的指南里就已經提到了內側顳葉。旁海馬實際上只是內側顳葉的一小部分。
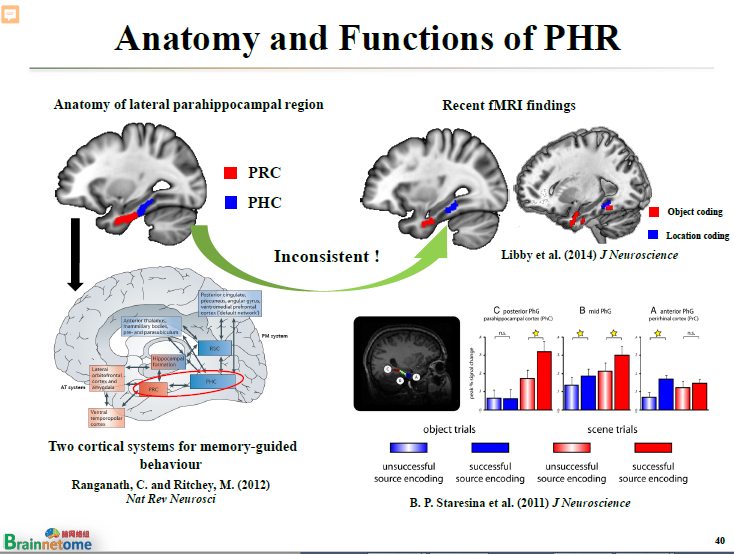
以前的傳統是將旁海馬分成前層跟后層。基于前層旁海馬和后層旁海馬,又提出了一個所謂的記憶系統。跟前層旁海馬相連的那些腦區所構成的網絡叫前記憶系統;跟后層旁海馬相連的那些腦區所構成的網絡就叫后記憶系統。
關于模型的提出發表在《Nat Rev Neurosci》上。這個模型出來以后,很多研究都想借助它解釋一些跟情緒相關的現象,但實際上沒辦法解釋。所以這樣就提出了非常嚴格的條件。
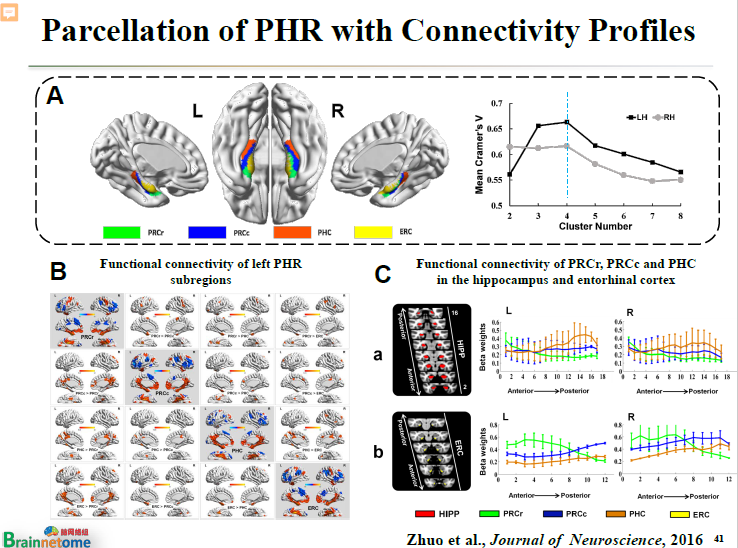
而用腦網絡組圖譜的思想對旁海馬重新分區以后,發現旁海馬不僅有前后兩個分區,而是至少可以分成前、中、后三個分區。
經過反復的驗證,從功能連接,到跟海馬從前到后的連接強度、跟內嗅皮層從前到后的連接強度等等,發現這三個腦區的模式是完全不同的,這就證明了旁海馬有三個分區。
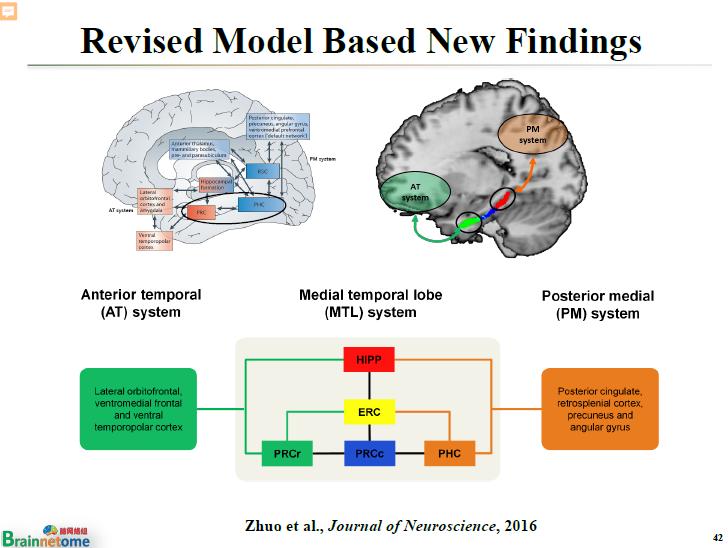
分出三個分區的意義就在于,以前的模型要重新改寫,包括旁海馬的連接圖譜都要發生變化,以前的圖譜就不能再用了。
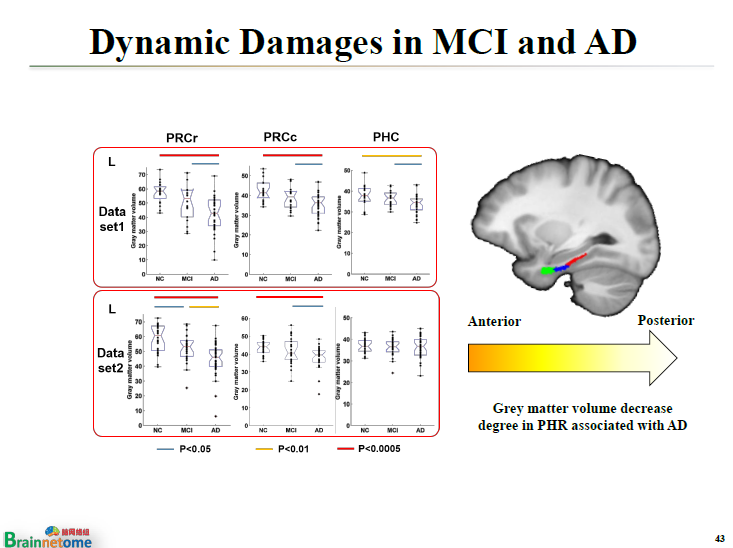
更重要的是,我們發現AD病人的旁海馬經歷了前、中、后這樣一個漸變的過程。在較早的時候,可能只有最前層開始萎縮,慢慢地往中間的過渡,等老年癡呆以后,整個旁海馬都開始萎縮了。
所以,使用腦網絡組圖譜的話,可能可以在很早的時候就發現這些蛛絲馬跡,而不是等到造成了災難性的后果以后才能知道。
這個例子就說明,基于腦網絡組圖譜可以去發現一些從前沒有發現的腦區,并且能夠給出一個非常清楚的解釋。
下面再講一下第二個應用的例子。

現在抑郁癥病人中,女性要比男性多很多。這是流行病學調查的數據,誰也不能解釋為什么是這樣的。另一方面,情緒調節是抑郁癥最核心的一個癥狀。
那么我們就要問,哪些腦區或者一個什么樣的腦網絡是支撐情緒調節的?
這個問題到現在并沒有非常清晰的答案。但有一些腦區跟情緒調節有關是非常明確的。像Amygdala,即杏仁核腦區,就是跟情緒調節有關的,而且這個結論非常明確。
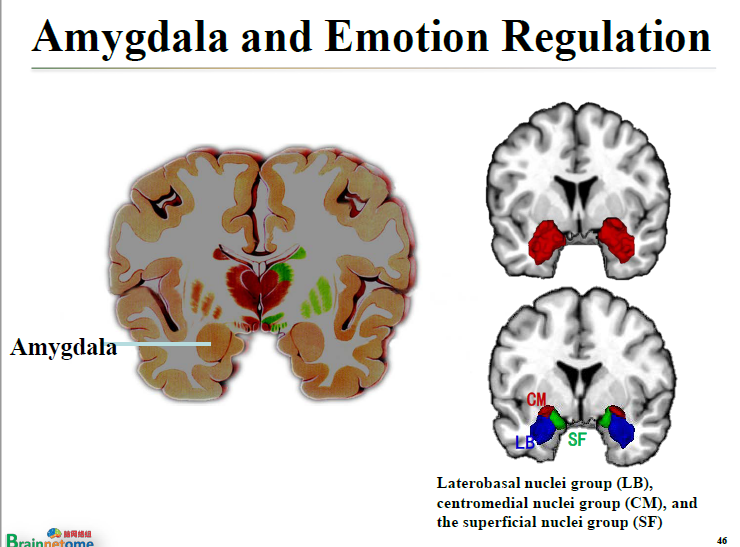
那么就以杏仁核為出發點,計算它跟全腦的連接強度,然后再按照連接強度跟情緒調節的分數之間的相關性,看女性和男性之間是否存在差別。
我們發現,如果用傳統的圖譜,即把整個杏仁核作為一個腦區進行分析,兩者是沒有差別的。
那么再往前走一步,用新的圖譜把杏仁核分成三個不同亞區,即centromedial nuclei group(CM)、laterobasal nuclei group(LB)跟the superficial nuclei group(SF)。
在這三個亞區上重復剛才的過程,即計算這三個亞區跟全腦的連接強度,再去跟情緒調節的分數做相關性分析,看女性和男性之間到底有沒有本質的區別。
我們招募了三百多個大學生進行研究,發現了一個很有意思的現象。
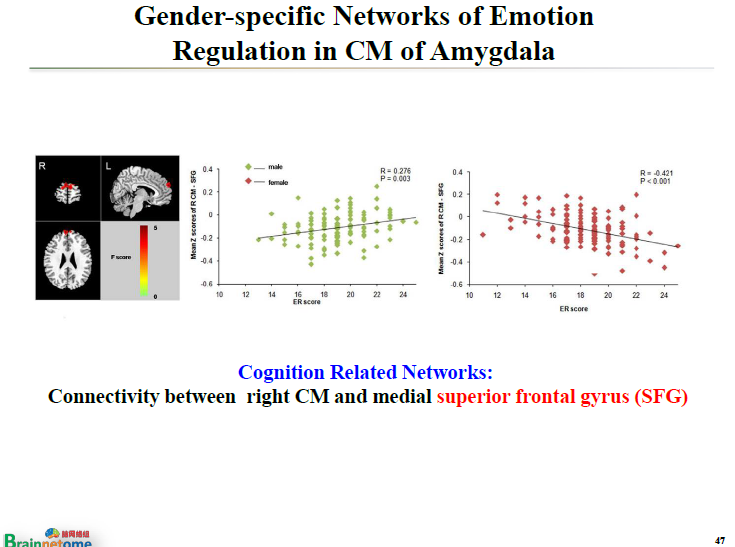
央內側核(CM of Amygdala)和額上回(superior frontal gyrus)的連接強度,跟情緒調節的分數做相關性分析以后,在男性里面呈現正相關,女性里面則呈現負相關。
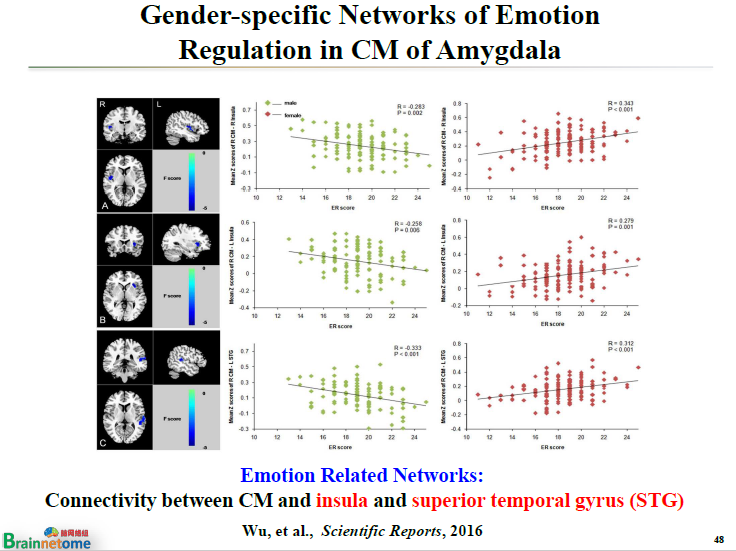
但同樣是中央內側核,它跟島葉(insula)或顳上回(superior temporal gyrus)這樣一些腦區的連接強度,跟情緒調節的分數做相關以后,男性里面又變成了負相關,女性里面則變成了正相關。
這也就說明,男性和女性使用了兩個完全不同的網絡進行情緒調節。這是非常有意思的一個證據。
這個例子也說明,如果仍然使用老圖譜,也許什么有意思的結果都發現不了。但如果使用新的圖譜,就會發現類似這樣一個非常有意思的現象。而以前基于老圖譜得出的很多結論有可能要重寫。
再講一個和診斷有關的例子。
大家都知道,現在精神類疾病沒有定量的生物標志,基本都是靠醫生的經驗對病人進行問癥分析,進而做出診斷。
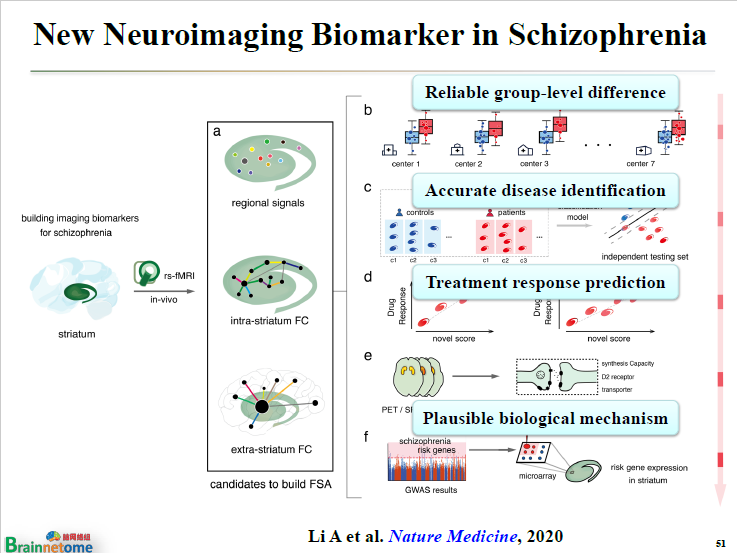
而我們通過腦網絡組圖譜,提取紋狀體進行分析,定義了一個紋狀體功能異常(Functional Striatal Abnormality, FSA)的定量指標。
我們基于973項目采集了五年所得到的數據,包含了千余例精神分裂癥患者與正常對照的多模態影像學數據。其中,有七家醫院,每家醫院都有大概中等規模的樣本。而紋狀體功能異常能夠在另外的至少七家醫院里面非常好地重復。
可重復性是能不能形成生物標志的最關鍵的因素。比如說,你發現了一個精神分裂癥患者與正常對照異常的指標,但是無法在不同機型的機器上得到重復性的結果,那么這個指標就是無效的。
現在發表的大部分研究成果都是在單中心上做出來的,但這個中心得出的結果,在另外一個中心卻未必能夠重復。
所以我們第一步就發現這七個中心都能很好地重復紋狀體功能異常這個指標。
接著,基于這個指標,可以回過頭來,利用深度學習等其他知識去做分類,發現它是一個能夠很好地將精神分裂癥和正常人區分開的生物標志。
病人服用現在常用的藥物進行治療以后,其生物標志的異常是否減輕?或者一個藥物療程以后,病人的癥狀有明顯的改善,這時的指標是否也已經往正常水平靠攏?答案是肯定的。
這個例子就說明,可以基于腦網絡組圖譜,去尋找一些疾病診斷的生物標志。
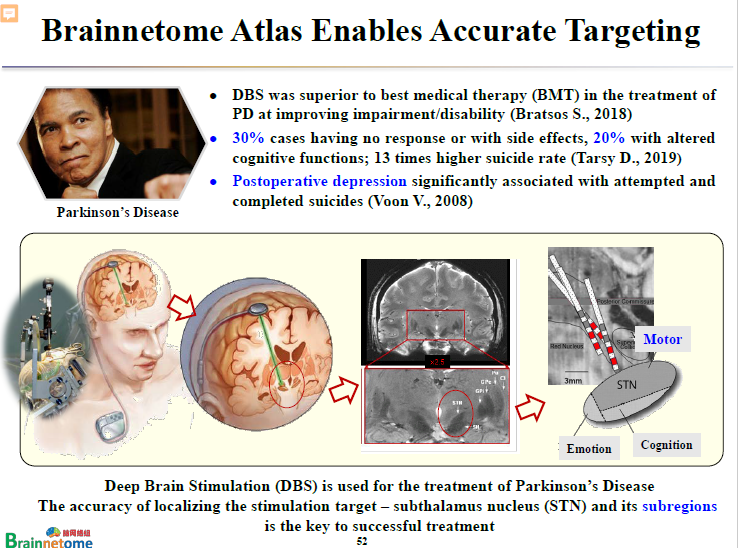
再講一個跟治療有關的例子。
現有的證據證明,對帕金森這類神經退行性的疾病來說,藥物治療的意義其實不是特別大。但現在有其他的治療方式,像DBS(Deep Brain Stimulation)就明顯比藥物治療的效果要好。但DBS治療也有副作用,它會導致抑郁、自殺等等。
DBS治療的靶點主要在丘腦底核(subthalamus nucleus ,STN)。而丘腦底核可以分成三個不同亞區,分別跟運動、情緒、社會認知功能有關。如果電極剛好放在跟運動有關的腦區,那么治療效果可能就很好。
但是如果放偏了,放在了跟情緒有關的腦區——本來帕金森不是情緒障礙,這就等于是來回刺激一個正常的腦組織,就會從正常變成異常,從而導致抑郁、自殺;當電極放偏到跟社會認知功能有關的地方,可能就會導致社會認知功能障礙。
本來有了腦網絡組圖譜以后,以前的那些問題都不是問題了,但就是因為電極放錯了位置,反而導致了新的問題。

所以要如何解決這個電極放置的問題?首先,醫生要利用腦網絡組圖譜找到合適的位置。但光有圖譜,有經驗的醫生可能可以一放一個準,新醫生卻未必能放準。
所以我們希望能夠建造一個手術機器人,手術規劃好以后由機器人去放置電極。為此,我們提出了一個新名詞——腦網絡組圖譜導航的手術機器人(Brainnetome Atlas Guided Neurosurgical Robot)。第一款機器人馬上就要出來了。

簡單地總結一下。
今天介紹了一個新的圖譜——腦網絡組圖譜,是用跟以前完全不一樣的基于解剖連接的信息構造的。
接著介紹了腦網絡組圖譜的作用,并通過不同的方式證明它是合理的。腦網絡組圖譜可以用于發現新的腦區,也可以用來尋找疾病診斷的生物標志,還可以提供神經調控的精準靶點等等。
腦網絡組圖譜不僅僅是一個圖譜,而是開辟了一個新的領域。
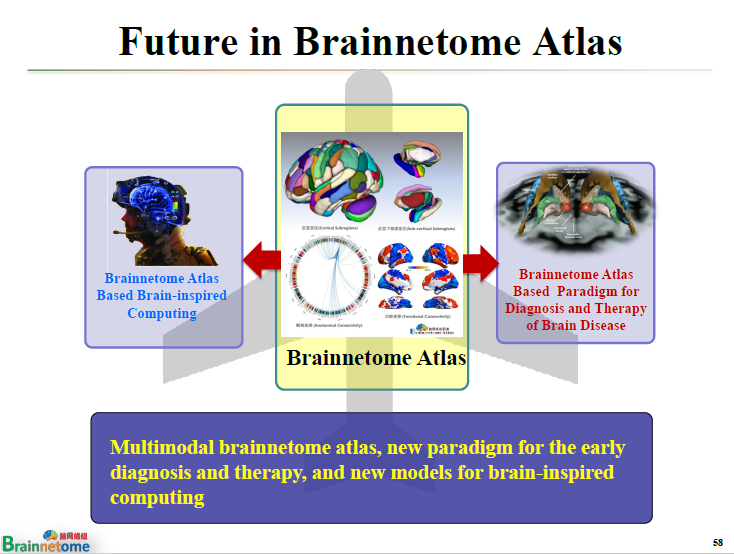
現在研究的方向分為“一體兩翼”。
“一體”就是腦網絡組圖譜本身。比如說,我們現在只是構建了一個人類腦圖譜,那么能不能把圖譜個體化?有沒有一種方式能夠將每個病人的圖譜快速地繪制出來?包括整個老化過程、發育過程對圖譜是怎么影響的等等。
更重要的是每一個腦區的功能是什么?像情緒記憶等等有哪些腦區參與了?這里面實際上有很多東西可以研究。這個就叫“一體”,就是關注圖譜。
除了腦圖譜本身的研究以外,還有“兩翼”,即兩個應用。
一個是跟“類腦”有關,也就是所謂的環路特異性的腦機交互,或者腦機融合。
另一個就是疾病的診療。前面已經舉了兩個例子,就已經不言自喻。引入新的圖譜以后,可能很多結論都會發生變化。大數據,加上腦網絡組圖譜,再加上人工智能的一些新方法,可能會讓現在腦疾病面臨的一些瓶頸問題取得突破。
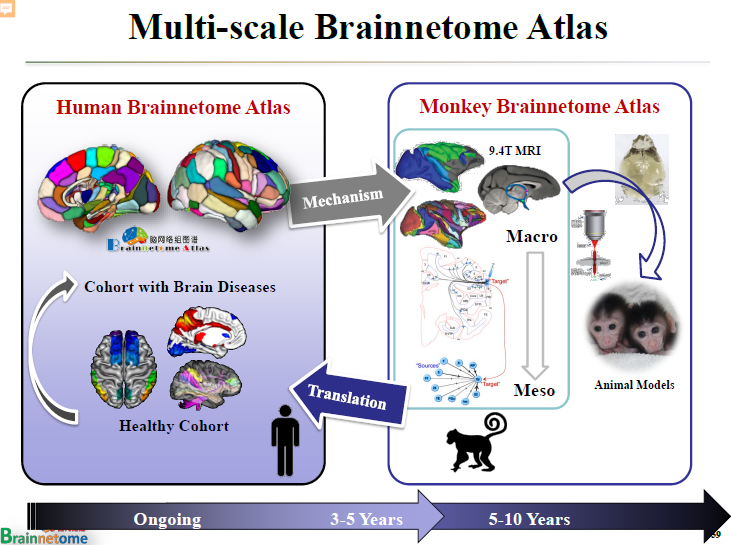
除了繪制人的腦網絡組圖譜,還可以繪制獼猴的腦網絡組圖譜。因為獼猴的腦袋跟人腦比較相似,所以獼猴是研究人類很多疾病所必須的一個模型。
更重要的是,我們不僅可以建立宏觀尺度的腦網絡組圖譜,還可以在獼猴上建立介觀尺度的圖譜。
所謂建立介觀尺度的腦網絡組圖譜,就是在宏觀尺度的基礎上,利用其他技術,把細胞尺度上面的不同連接統統構建出來。
未來我們也有一些國際合作項目。比如跟于利希中心有一個國際合作重點項目,主要是想把細胞構筑的分區跟基于連接模式進行分區的兩個結果放在一起進行比較。
腦網絡組圖譜研究項目是中國科學院國家自然科學基金委員會的重大研究計劃,獲得了科技部973項目、國家自然科學基金委以及中科院戰略性先導科技專項的資助。
謝謝大家,我的報告到此結束。
原文標題:萬字長文 | 中科院蔣田仔教授:腦網絡組圖譜及其在腦認知與腦疾病方面的應用
文章出處:【微信公眾號:IoT科技評論】歡迎添加關注!文章轉載請注明出處。
責任編輯:haq
-
網絡
+關注
關注
14文章
7522瀏覽量
88645 -
AI
+關注
關注
87文章
30212瀏覽量
268460
原文標題:萬字長文 | 中科院蔣田仔教授:腦網絡組圖譜及其在腦認知與腦疾病方面的應用
文章出處:【微信號:IoT_talk,微信公眾號:醫健AI掘金志】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
ADS1299測量腦電信號的寄存器配置該如何配置呢?
景昱醫療:腦機接口是治療難治性精神疾病更有效的手段

ADS1299為什么測量不到腦電信號?如何解決?
使用ADS1299進行腦電信號采集時采集不到腦電信號,怎么解決?
怎樣做ZL-01C單臂數顯小動物腦立體定位儀實驗?
SynSense時識科技成功收購瑞士類腦視覺傳感器公司iniVation,類腦智能航母蓄勢待發





 腦網絡組圖譜及其在腦認知與腦疾病方面的應用
腦網絡組圖譜及其在腦認知與腦疾病方面的應用












評論