【研究背景】
由于金屬資源有限和環境保護,鋰離子電池的回收是很重要的。然而,目前的大多數研究只著眼于從正極材料中提取有價值的成分,而正極中的鋰由于其濃度低,通常被忽略。
【工作介紹】
本工作報告了一種用于廢舊LIB的閉環回收策略。將電池直接拆卸,然后陽極(鋰化石墨)中的鋰被有效提取并用于直接再生陰極材料(鈷酸鋰(LCO)和Ni0.5Mn0.3Co0.2O2(NMC532))。通過固態燒結進行了再生過程。結果表明,層狀正極材料邊緣的缺陷和內部的鋰空位對于Li+進入正極材料的層間至關重要。退化的陰極和陽極在再生后都恢復了其電化學性能,使用再生的鈷酸鋰和石墨的全電池表現出與使用商業電極材料相似的循環性能。
【具體內容】
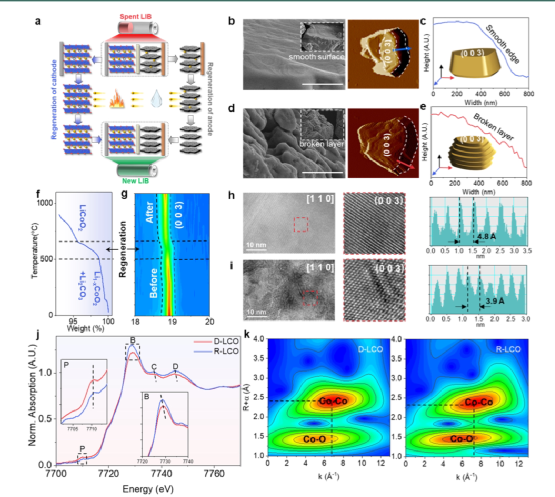
【圖1】廢LIB的封閉循環和陰極活性材料的再生機制。
圖1a顯示了的廢舊鋰離子電池封閉式回收循環的示意圖。陰極的再生和陽極的再生是通過鋰的循環聯系在一起的。將鋰直接與水反應,并吸收空氣中的二氧化碳,轉化為Li2CO3,而不需要額外的沉淀劑,這可以確保產品的純度,避免分離和提純步驟。以剩余容量為70%的降解的鈷酸鋰(D-LCO)為例,再生的鈷酸鋰被簡稱為R- LCO。R-LCO顆粒具有光滑的表面和邊緣,而D-LCO顆粒在邊緣有明顯的斷裂(圖1b和d)。在剩余容量為15%和40%的降解的鈷酸鋰(D-LCO-15和D-LCO-40)中也觀察到同樣的形態差異。在再生過程中,Li2CO3首先附著在階梯狀微裂縫上,然后通過加熱分解成Li2O。由于沒有鋰,D-LCO的破碎部分已經部分轉化為氧化鈷,Li2O與之反應,再生出LCO的晶體。隨后,隨著加熱過程的進行,新生成的LCO晶粒逐漸長大,并將覆蓋所有的微裂縫,從而生成具有光滑表面的LCO顆粒。
LCO的再生可以分為兩個關鍵步驟。(a)Li2CO3的分解和 (b) Li在D-LCO中的插層。
有趣的是,Li2CO3的TG曲線和Li2CO3分解反應的吉布斯自由能都顯示,其分解溫度遠遠高于500℃,但與D-LCO混合后,在500℃就開始分解了。很明顯,D-LCO對Li2CO3的分解有 "催化作用"。因此,對這個過程進行了理論計算。根據形貌特征,D-LCO的表面有明顯的微裂紋,這是由于長期循環造成的鋰損失(圖1d)。因此,在D-LCO顆粒的邊緣存在著一定量的鋰空位(圖2a)。計算結果表明,缺陷的存在導致Li2CO3分子的吸收能量更高(圖2b)。D-LCO吸收的Li2CO3分子的相對能量為-4.96 eV,遠遠高于沒有缺陷的原始LCO(P-LCO)(-3.21 eV)。在被吸附在D-LCO的邊緣后,隨著溫度的升高,Li2CO3更容易分解。這種分解的相對能量是-3.20 eV,遠遠高于P-LCO邊緣的能量。比P-LCO邊緣上的要高得多。為了證實這一點,比較了D-LCO + Li2CO3和P-LCO + Li2CO3的TG曲線。當與D-LCO混合時,Li2CO3在500℃開始分解,但當與P-LCO混合時,分解發生在大約680℃(圖2c和d)。根據Li2CO3-Li2O相圖和吉布斯自由能計算,Li2CO3只有在加熱到大約700℃時才能分解(圖2e和f)。P-LCO對Li2CO3的分解沒有什么影響,而D-LCO有 "催化作用"。
鋰進入D- LCO時的狀態:根據XANES和EXAFS的結果,鋰以Li+的形式進入層間空間。根據吉布斯自由能的計算,即使在超過1000℃的溫度下也不可能發生Li2O到Li的還原(圖2f)。因此,可得出結論,鋰以Li2O的形式存在,Li+在D-LCO內的擴散發生,以確保每個Li+空位的有效補給(圖2g)。計算結果表明,這個過程具有典型的過渡態擴散特征,在初始態和過渡態之間有一個大約1.45eV的擴散能壘。
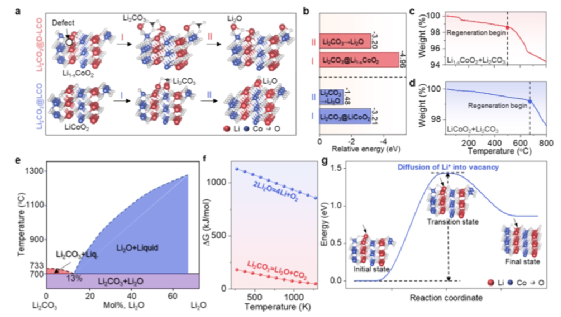
【圖2】陰極材料再生的理論計算結果。(a)不同LCO樣品和Li2CO3之間反應的示意圖。(b)不同LCO樣品和Li2CO3之間反應的相對能量。(c)D-LCO和Li2CO3混合物的TG曲線。(d)P-LCO和Li2CO3混合物的TG曲線。(e)Li2CO3-Li2O相圖。(f)再生過程中可能反應的吉布斯自由能。(g)Li+插入D-LCO空隙時的擴散能壘。
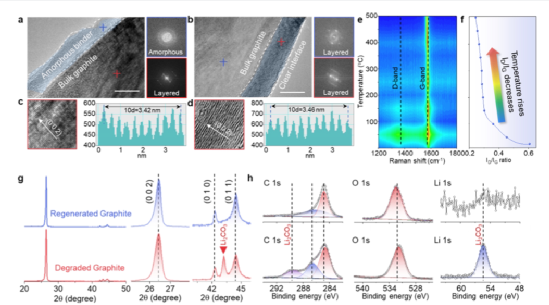
【圖3】鋰陽極的再生機制。(a)D-石墨的TEM圖像。(b)R-石墨的TEM圖像。(c)HRTEM圖像和D-石墨的相應平面間距。(d)R-石墨的HRTEM圖像和相應的平面間距。(e)再生過程中石墨的原位拉曼光譜。(f)再生過程中ID/IG的變化。(g)D-石墨和R-石墨的XRD模式。(h)D-石墨和R-石墨的XPS光譜。
脫鋰的降解石墨(D-石墨)經歷了一個由凈化和活化組成的再生過程。D-石墨和再生石墨(R-石墨)在形態上沒有什么區別。隨著放大倍數的增加,在D-石墨的邊緣觀察到無定形物質,這很可能是殘留的粘合劑和SEI(圖3a)。相比之下,在R-石墨中觀察到了一個干凈的邊緣,表明在再生過程中粘合劑和SEI都被去除(圖3b)。兩種石墨樣品的HRTEM圖像和相應的(002)平面間距幾乎相同(圖3c和d)。
如果在提取鋰之后,D-石墨中還有鋰,那么它應該通過酸的純化而被釋放出來,導致平面間的間距發生輕微變化。然而,再生后沒有這樣的變化,這意味著Li-GICs中的鋰已被完全提取。
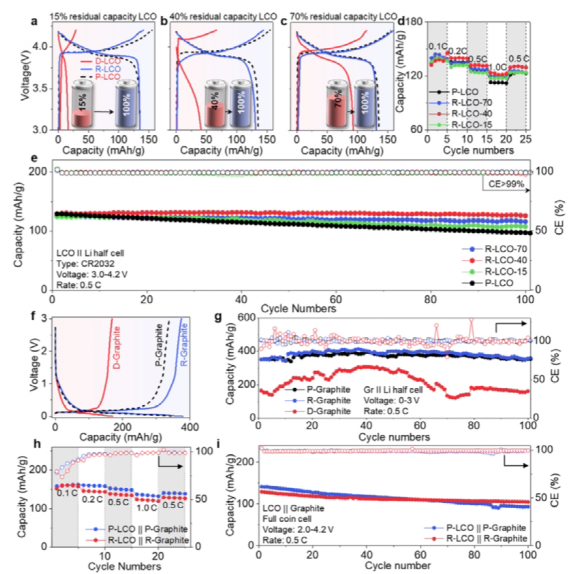
【圖4】采用回收電極材料制作的電池的電化學性能。
具有不同剩余容量的降解LCO可以被有效再生,并表現出與P-LCO相當的電化學性能。具體來說,D-LCO-70和D-LCO-40的剩余容量分別為101.9 mAh/g和49.7 mAh/g,再生后都恢復到大約140 mAh/g,非常接近P-LCO(138.9 mAh/g)。即使是剩余容量只有22.8 mAh/g的D-LCO-15,在補充了鋰和額外的鈷之后,也可以恢復到大約140 mAh/g的容量(圖4a-c)。所有三個再生的LCO的速率能力也與P-LCO相當(圖4d)。當電流速率增加到4C時,R-LCO-40的容量為80 mAh/g,而R-LCO-70、R-LCO-15和P-LCO的容量幾乎為零。
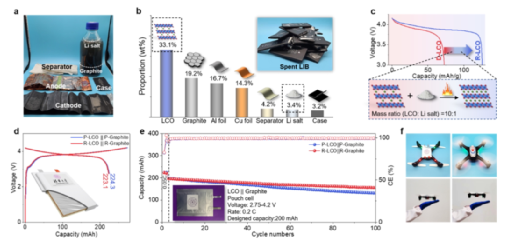
【圖5】本工作采用的封閉式回收循環,使用再生電極材料回收手機電池和軟包電池。
將這種閉環策略應用于商業手機電池,以證明其潛在的大規模可行性。一塊43.1克、標稱容量為2900mAh的典型手機電池被分解為陽極、陰極、隔膜、石墨、含鋰溶液和外殼(圖5a)。陽極、陰極和含鋰溶液被處理,以獲得D-LCO、D-石墨、鋰鹽和其他成分(圖5b)。共獲得14.3克D-LCO(占電池總重量的33.1%)和8.3克石墨(占電池總重量的19.2%),而從含鋰溶液中提取了1.5克鋰鹽(主要是Li2CO3,相當于0.28克的鋰)。經計算,陽極石墨中的鋰含量為3.4%。D-LCO與鋰鹽的質量比約為10:1。鋰鹽的數量足以使D- LCO的容量在再生后在0.1 C時從74.5提高到137.8 mAh/g(圖5c),這意味著不需要額外的外部鋰鹽,而且在陰極再生過程中唯一的試劑成本是水,這幾乎可以忽略不計。這種策略不僅適用于單個電池。在實際應用中,許多電池可以一起拆解,陰極和陽極可以分別收集。一旦陽極中的鋰被完全提取出來,相應的陰極的再生就不需要外部鋰。
使用商業或再生電極材料的軟包電池被組裝和比較,以驗證再生的LCO和石墨的電化學性能。帶有R-LCO陰極和R-石墨陽極的小軟包電池的容量為223.1 mAh,與使用商業電極材料的電池(224.3 mAh)在第一個循環中幾乎相同(圖5d)。此外,使用再生電極的小軟包電池的循環穩定性略好于使用商業電極的小軟包電池(圖5e),并滿足在無人機中使用的要求,如圖5f所示。
【要點總結】
目前幾乎所有的陰極材料再生方法,特別是固態燒結法,都需要加入外部鋰鹽。在這項研究中,從鋰化石墨中回收了含鋰成分,這在以前的研究中經常被忽視,并將其作為鋰源直接再生退化的陰極材料。因此,在陰極再生過程中不需要外部鋰鹽,這就降低了回收的成本。研究發現,LCO顆粒邊緣的缺陷在再生過程中對Li2CO3的分解和Li+的插層起著關鍵作用。脫鋰的石墨可以通過凈化和活化再生,并作為陽極材料重新使用。再生的陰極和陽極材料具有與商業原始電極材料相似的電化學性能。這項工作通過鋰的提取和再利用為陰極和陽極材料的直接再生搭建了橋梁,在廢舊鋰離子電池中形成了一個封閉的回收循環。這種回收策略有效地回收了鋰離子電池的陽極和陰極材料,具有低碳排放和低能耗的特點,為實際的電池回收提供了一個光明的前景。
Efficient Extraction of Lithium from Anode for Direct Regeneration of Cathode Materials of Spent Li-Ion Batteries
ACS Energy Letters(IF23.991)Pub Date:2022-08-03, DOI:10.1021/acsenergylett.2c01539
Junxiong Wang, Jun Ma, Kai Jia, Zheng Liang, Guanjun Ji, Yun Zhao, Baohua Li, Guangmin Zhou, Hui-Ming Cheng
審核編輯 :李倩
-
鋰離子電池
+關注
關注
85文章
3215瀏覽量
77550 -
電化學
+關注
關注
1文章
316瀏覽量
20571 -
lib
+關注
關注
0文章
16瀏覽量
9194
原文標題:成會明&周光敏:鋰電回收重要進展--負極提鋰,直接用于正極再生
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
朗凱威廢舊磷酸鐵鋰電池回收:環保與資源再生的新機遇

退役電動汽車鋰電池正極材料的直接再生策略—去除殘留污染物的關鍵作用




 一種用于廢舊LIB的閉環回收策略
一種用于廢舊LIB的閉環回收策略











評論