背景介紹
電化學阻抗譜提供了有關電化學氧化還原反應的穩態及其動力學的信息。比如,阻抗是研究電池動力學的一種非常有用的技術,深化對于電池運行期間的擴散過程或電荷轉移反應動力學的理解。
二、正文部分
1、成果簡介
威斯康星大學密爾沃基分校QuDeyang等人總結了對電池系統進行可靠阻抗測量的流程,包括電池配置、阻抗測試系統的準備情況、阻抗譜中數據的驗證、基于弛豫時間分布的電化學過程的反卷積和阻抗譜的等效電路擬合。該研究以題目為“Probing process kinetics in batteries with electrochemical impedance spectroscopy”的論文發表在國際頂級期刊《Communications Materials》。
2、研究亮點
本文討論了準確和可重復的電池阻抗測量的關鍵參數。
3、圖文導讀
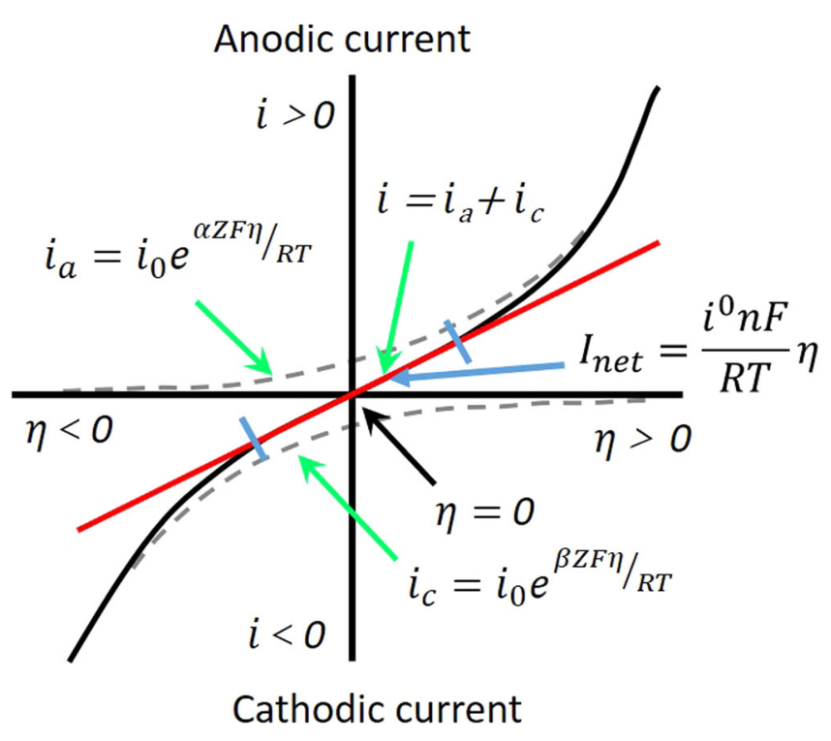
【圖1】電化學極化曲線。電化學極化曲線顯示了電池電壓如何偏離其OCV,可以將其視為其熱力學平衡電壓。充電或放電期間電池電壓與其OCV的差異是過電位。ia和ic 分別是負極和正極電流密度;α 和β (= 1?α) 分別是負極和正極的電荷轉移系數;η 為電荷轉移過電位;R 是氣體常數,F 是法拉第常數。
對 EIS 的誤解之一是它被錯誤地認為是一種非穩態技術。非穩態實驗中的擾動信號大到足以使電化學系統遠離其初始穩態。例如,當電池以大電流放電時,電化學系統被極化到遠離平衡態的Tafel區。然而,EIS 實驗是在穩態下進行的,其中小幅度激發信號疊加在穩態電位上。
由于激發信號的幅度很小,因此電極從未離開過穩態附近。與極化信號將不可避免地對電化學系統造成不可逆變化的非穩態實驗不同,在穩態實驗中可以避免這種不可逆的改變。電池通常需要很長時間才能達到穩定狀態。在進行EIS 之前,確保弛豫電流(直流電流)遠小于激發電流是至關重要的。偶爾向系統施加10?mV 脈沖(假設激發幅度為10?mV),記錄峰值電流。
當開路電壓(OCV) 下的電流衰減到小于峰值電流的10% 時,可以對電池進行EIS。當施加寬頻率范圍的激發信號時,可以在不偏離初始穩態的情況下獲得大范圍時間常數的界面過程。因此,EIS 非常適合研究電極穩態附近的動力學參數,因為它橋接了各種時間常數的穩態和瞬態。
因此,在進行阻抗測量之前,應確保電化學系統接近其平衡狀態。大多數交流阻抗儀器和相關的數學處理僅適用于線性系統。如圖1所示,電化學系統是非線性系統;例如,電極/電解質界面處的電流與電位成指數關系(Tafel 關系)。非線性可以顯著地扭曲響應信號,因為它們可以通過在電池響應中產生激發信號的諧波來表現出來。
這種失真可能導致在阻抗結果建模期間對結果的錯誤表示或誤解。接近平衡或穩態(i = 0 mA/cm2)的區域可以被認為是一個線性系統。
如果激發信號不足以將電化學系統極化到 Tafel 區域,則可以安全地假設電化學系統并將其視為線性系統。通常,大多數情況下使用10?mV 的峰間幅值。 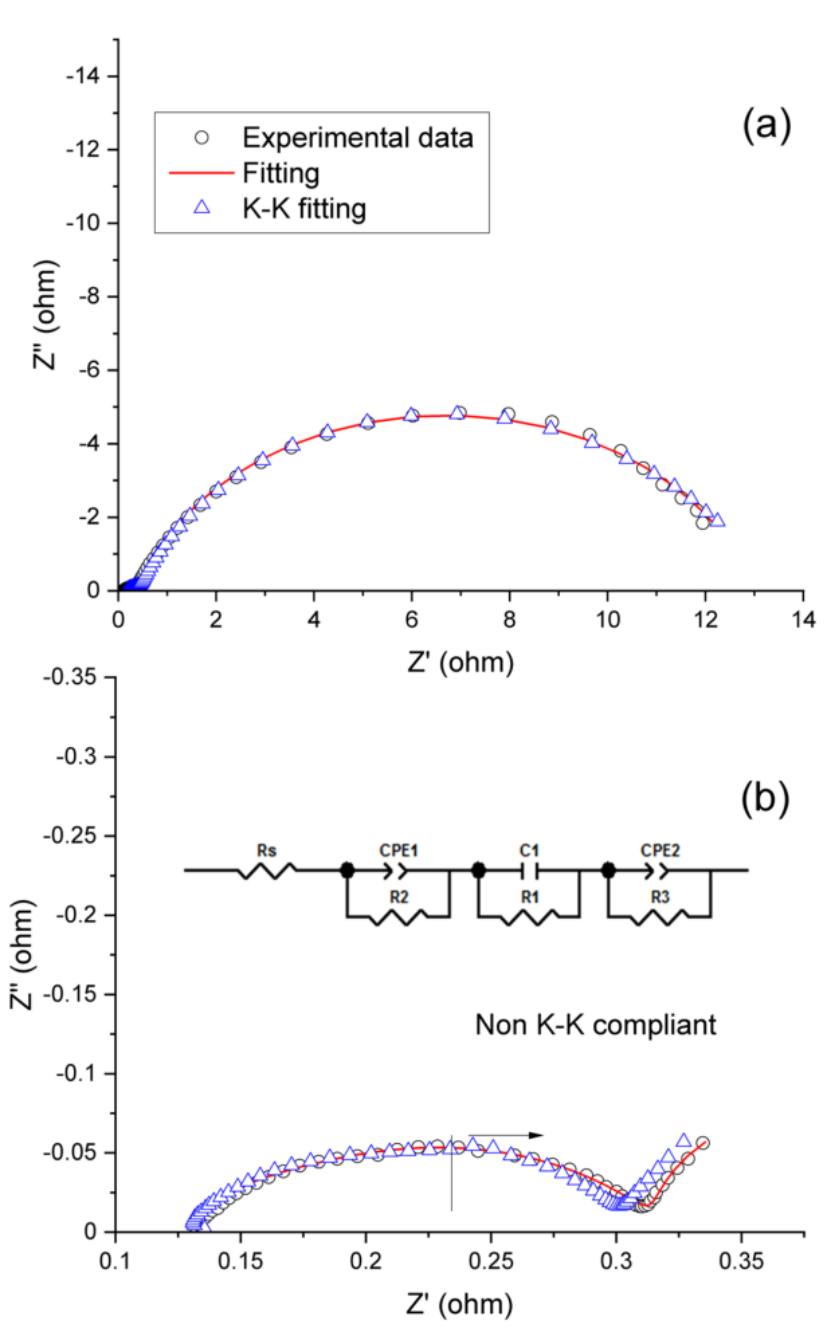
【圖2】典型阻抗譜的數值擬合和K-K擬合。需要 K-K (Kramers-Kronig) 合規性來確保電化學系統的線性度。a符合 K-K 標準;b 不符合 K-K 標準;等效模型用于計算測量頻率范圍之外的阻抗點。
阻抗譜的測量、解釋和模擬是基于電化學系統的線性假設。即使是很小的測量噪聲也可能導致不合規性,從而導致對電化學過程的誤解和不準確的電化學參數。因果關系、線性、穩定性和有限性用于保證合規性。
Kramers-Kronig (K-K) 關系通常用于證明阻抗數據的合規性。K-K 關系由 Kramers 和 Kronig 提出用于光學分析,然后由 Bode 在電子電路分析中引入。
可以識別不符合要求的數據點并將其從阻抗譜中移除。 圖 2 顯示了兩組阻抗數據的 K-K 驗證。用于 K-K 驗證的軟件是 BioLogic EC-Lab 。圖 2a 顯示了整個頻率范圍內符合 K-K 標準的阻抗譜,而圖 2b 顯示了只有頻譜的高頻部分符合 K-K標準。圖 2b 中低頻的不符合 K-K標準的數據點需要從后續的數據建模和計算中排除。
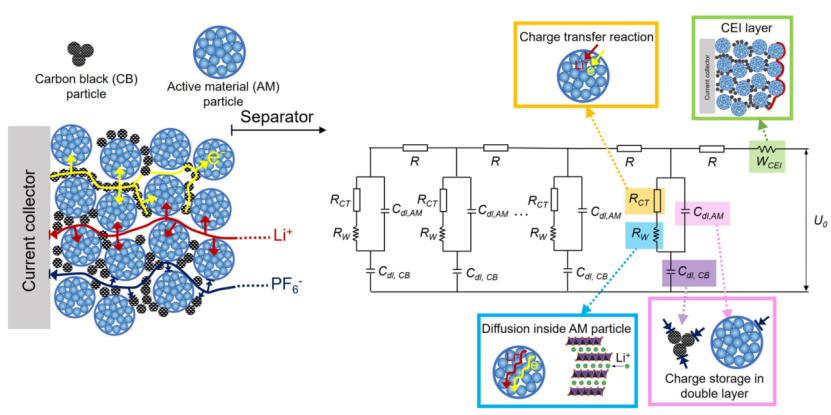
【圖3】LIB 正極和傳輸線等效電路中所有可能的物理和電化學過程以及相應的電化學過程的圖示。該圖顯示了如何在傳輸線模型中表示物理和電化學過程。例如,活性材料顆粒界面處的電荷轉移過程可以用電阻器 (RCT) 表示,Li 在活性材料內部和通過 CEI 的擴散過程可以用 Warburg 電阻器 Rw 和 RCEI表示。CEI 代表正極上可能的表面界面;Rs為電阻;Cdls 為雙層電容,U0 為外加電壓。
理想情況下,人們會根據從真實電化學過程(例如Fick 定律、電化學吸收、Butler-Volmer 關系等)派生的數學分析阻抗數據。然后可以使用理論阻抗函數來提取動力學參數。由于正確分析所需的數學水平,幾乎所有的阻抗分析都是使用基于等效電路的硬元件進行的。盡管該方法忽略了EIS 解釋電化學機制和動力學的能力,但它仍然產生了許多有用的信息,特別是對于電極、電池和電池組的實際設計。
即使使用降級或簡化的等效電路建模,研究人員有時也打算輕而易舉地使用它而沒有仔細考慮。等效電路中的等效一詞代表電化學過程的等效。沒有一種萬能的或通用的等效電路。與搭建樂高玩具類似,您需要熟悉每一件樂高積木。構建等效電路,需要對整個電化學過程、這些過程之間的關系(串聯或并聯)以及每個組件(電阻器、電容器,尤其是CPE(恒相元件))的物理和電化學意義進行假設。
人們可能會閱讀文獻,其中在Nyquist圖中顯示了半圓和斜線。在討論中,得出的結論是該過程與平行擴散過程具有界面反應。如果沒有仔細分析,結論可能會產生誤導或根本不充分。讓我們研究鋰離子電池 (LIB) 正極中的電化學過程以及如何將它們組裝到等效電路中。圖 3 說明了 LIB 多孔正極中所有可能的電化學過程。與任何電化學電極一樣,包括四個基本電化學過程中的三個——電荷轉移、雙電層和擴散,而電吸附不應用或至少可以忽略不計。
電荷轉移過程發生在正極活性材料顆粒和電解質之間的界面處。只要電化學反應保持在平衡狀態附近,電荷轉移過程就是線性的,如圖1所示。因此,該過程可以用電阻器表示,并遵循歐姆定律。
在LIB的多孔正極中,雙電層可以在活性材料顆粒和導電碳顆粒的表面上。對于單個活性材料顆粒,電荷轉移電阻 RCT 與其雙電層電容器并聯,而附加碳顆粒上的雙層電容器與 R/C 單元并聯,如圖 3 所示。正極中使用的導電碳是一種微量成分,其表面積較低(<100 m2?g-1),通常忽略導電碳的雙電層貢獻。
值得強調的是,在發生電化學反應的所有表面上都建立了雙電層,因此,雙電層電容可用于估計動態電化學可及表面積。 傳質可以說是所有電化學過程中最重要和最復雜的。擴散速率決定了活性材料的利用率,在高倍率操作中尤其如此。擴散就像一個信使,在整個多孔電極的基質中傳輸質量,并將離子移入和移出電極和電解質界面。
在等效電路中使用 Warburg 阻抗來表示擴散過程。Warburg 阻抗可以直接通過求解 Fick 第二定律的偏微分方程得到。
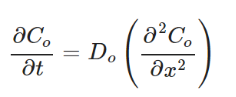
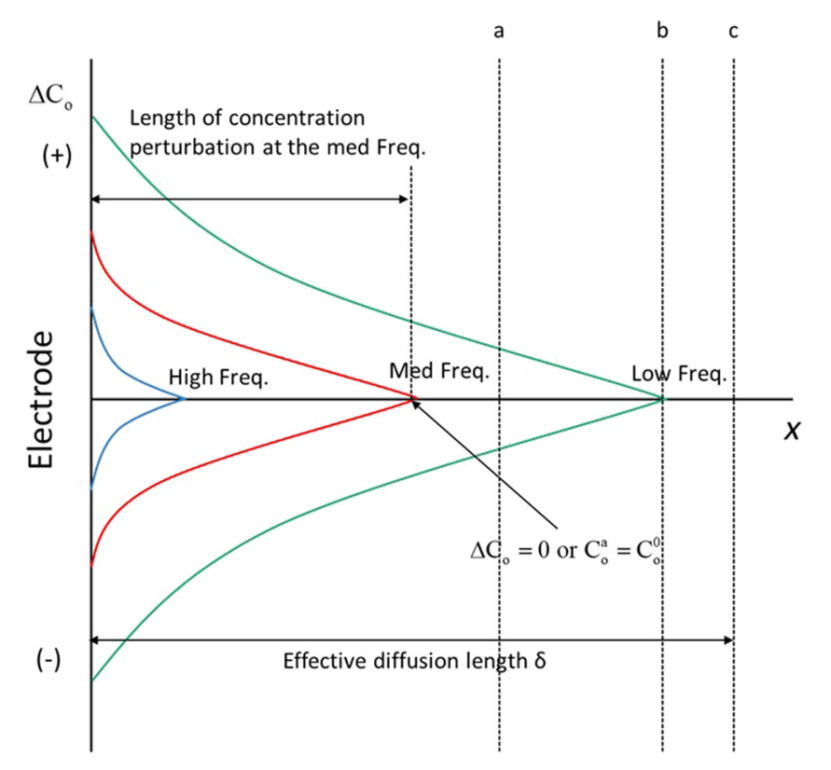
【圖4】濃度擾動長度與激發頻率。隨著激發頻率變低,擴散長度變長。由于在低頻下,離子在一個方向上擴散的時間更長。ΔC 濃度變化。
在經典的電化學中,包含固體扁平電極的系統浸入充滿的電解質中。使用半無限邊界條件 (Co(∞,t)=C00) 來求解 Fick 的偏微分方程。半無限假設總是正確的,因為扁平電極上的擴散層長度總是比充滿電解液的電化學電池的尺寸小幾個數量級。
然而,鋰離子正極可能無法滿足半無限邊界條件,尤其是在低頻激發或擾動條件下。圖 4 顯示了不同頻率激發下濃度微擾長度的變化。有效擴散長度 (δ) 代表可用于發生擴散的物理空間。顯然,激發頻率越高,濃度擾動長度越短。與大量溢流電解質中的扁平電極不同,其中 δ 可以是燒杯電池的大小,多孔正極中的鋰離子擴散發生在活性材料的初級粒子中,在薄的 SEI(固體電解質界面)層和多孔電極內的孔隙中。
根據初級粒子的大小、細孔的直徑和 SEI 層的厚度,可能不適用半無限條件。假設,如果 SEI 層的厚度約為圖 4 所示的“a”長度,則半無限 Warburg 阻抗不應該用于低頻區域,但適合用于高頻區域。根據我們的經驗,“a”情況是電池系統中最常見的情況。
這種情況下的邊界條件是在x = δ,ΔC0= 0。 Warburg 阻抗,無論是半無限的還是無限的,都不能很好地代表分布式多孔擴散矩陣中的擴散,即使沒有發生電荷轉移或法拉第反應,例如在理想的雙層電容器中。Warburg 阻抗僅適用于邊界條件用于求解 Fick 第二定律的連續介質。如圖 3 所示,由于離子在不同尺寸的孔隙內擴散,在非連續介質中,物理孔隙表面的可及性并不均勻。只有一小部分可用表面,即大孔的表面,可以在高頻調制下變得可及。
由于這些細孔中的傳質比極化速率慢,因此細孔表面沒有發生電化學反應或雙電層。同樣的問題也適用于厚電極。只有靠近隔膜的電極部分以高速率參與反應,而最靠近集流體的電極部分保持未反應。 Levie 提出的圖 5 所示的傳輸線通常用于模擬非連續和多孔介質的分布現象。
傳輸線的數學方程與擴散方程具有相似的形式,因為發生在 RC 電路中的過程可以被視為電子擴散到半無限介質中。如圖 5b 所示,每個RC 單元包含RCT。RW和 CDL代表多孔電極基質中的活性正極表面。
理想情況下,傳輸線模型中的 RC 單元的數量(n)(模擬發生在總孔表面的 1/n 上的電化學反應)應該是無限的,以代表多孔電極的全貌。每個 RC 單元,即孔隙表面的 1/n,具有不同的時間常數。
換句話說,并不是所有的表面都可以同時被電化學可及。使用圖 5 所示的傳輸線模型,可以估計多孔電極的電化學可及表面積或電化學可及深度。圖5 顯示了具有孔隙率梯度設計的厚電極的電化學可及性的模擬。
圖5d 清楚地表明,100% 的電極表面可以在非常低的頻率(0.01?Hz)下參與電化學反應。
隨著頻率的增加,電化學反應所占據的物理表面積(例如,通過N2吸收等溫線測量)的百分比會大幅下降。根據作者的經驗,只有不到50% 的電極表面可用于中等頻率下厚度約為200 μm 的電極。 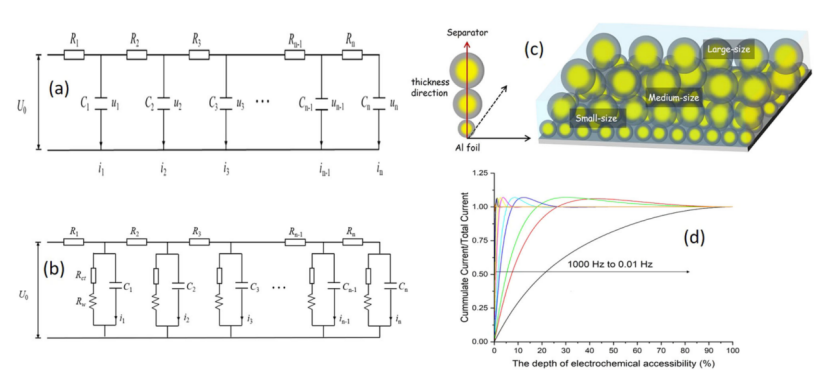
【圖5】多孔電極的傳輸線模型。a 沒有電荷轉移,b 有電荷轉移過程。c 厚電極的孔隙率梯度設計說明和 d 不同頻率下的穿透深度估計。該圖演示了如何使用傳輸線等效電路來表示具有不同孔結構和相關電化學可及性深度的多孔電極。
作者在經典電化學中研究了一個特定電極上的電化學過程。正在研究的電極稱為工作電極 (WE)。為了確保電化學電池中的所有變化都歸因于 WE,通常使用帶有參比電極 (RE) 的三電極設置。RE 的組成是恒定的,并且電極在整個實驗過程中保持在電化學平衡狀態。
不允許有明顯的電流通過 RE,否則會發生極化,導致電位偏移。因此,在三電極系統中,人們觀察或控制 WE 相對于 RE 的電位。如圖 6 所示,極化電流在 WE 和稱為對電極(CE)的輔助電極之間流動。在三電極系統中,CE 的電化學特性不會影響工作電極的行為,其唯一目的是促進電流流動。
然而,在電池研究中越來越多地報道了雙電極電池。在雙電極電池中,兩個電極的極化都包含在電化學數據中,例如阻抗譜。除非另有證明,否則不能假設雙電極系統的電化學結果可歸因于正極或負極。 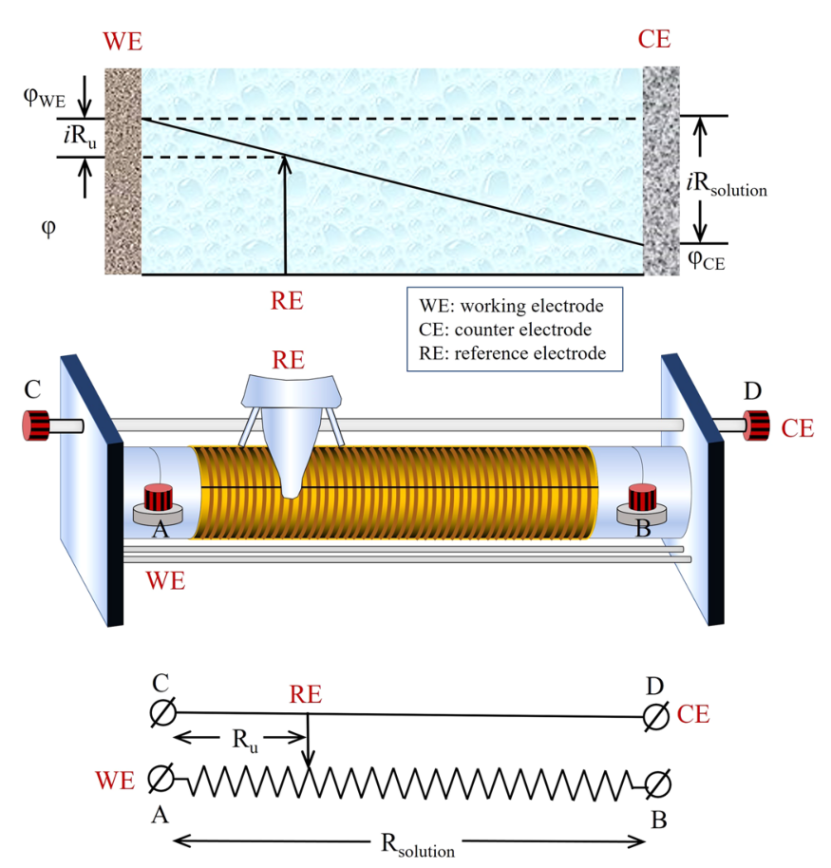
【圖6】三電極系統的圖示。可變電阻器用于演示工作電極 (WE) 和參考電極 (RE) 之間的 IR 壓降。CE為對電極;φWE和φCE 分別是工作電極和對電極的電位。
盡管參比的使用是一種非常有用的診斷工具,但它是一種破壞性的方法。有時,RE 的使用在技術上具有挑戰性,例如,將參比插入到卷筒狀電池中。
從理論上講,RC 單元在時間弛豫空間中連續分布的廣義電路可用于表示任何電化學阻抗,而與電化學性質無關。弛豫時間是系統在擾動后恢復到穩定狀態所需的時間。因此,弛豫時間越短,反應動力學越好。例如,對于具有較高交換電流的電化學反應,弛豫時間很短。
為了解卷積頻域中重疊的極化效應(阻抗譜),可以通過傅里葉變換或擬合到廣義電路中,將阻抗譜轉換為時域中的時間弛豫分布。在 DRT 分析中,在沒有預先假設物理和電化學過程的情況下擬合阻抗。因此,每個過程可以沿著代表相應過程的速率常數的弛豫時間的變化分布。
圖 7 顯示了相應頻域和時域中的物理和電化學過程。DRT 方法在電化學儲能研究領域引起了越來越多的關注,因為它能夠解開和解卷積在阻抗譜中相互重疊的各種過程的極化。
如果結合參比探針的使用,可以詳細研究正極和負極的動力學。圖 8 顯示了具有寬溫電解質的 LIB 與對照電解質的阻抗研究結果。Li 參比電極在面對面的單層軟包電池中使用。實現正極vs.參比;負極vs.參比。在形成后、50 次循環后和 100 次循環后測量電池(正極與負極)。
如圖 8 所示,阻抗譜中每個物理和電化學過程的速率常數(弛豫時間)和極化電阻(弛豫幅度,相應峰的積分)沿弛豫時間去卷積。圖 3 顯示了鋰離子陰極的完整等效電路。將阻抗譜擬合到完整的等效電路既費時又麻煩。實際上,人們基于有根據的推測構建了一個簡化的等效電路;這種方法適用于簡單的電化學系統。由于電池系統中使用的多孔電極的分布式特性,重要的電化學過程可能在不同的頻率范圍內變化。
DRT 可用于識別不同頻率范圍內的主要電化學過程,方法是對它們進行去卷積以及時間的弛豫。然后可以相應地構建等效電路。 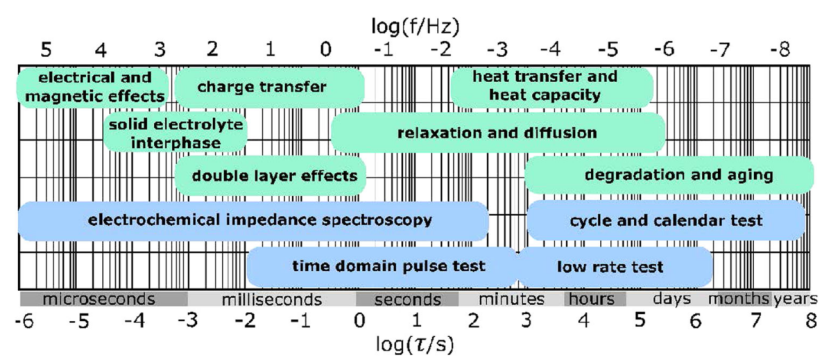
【圖7】具有典型特征時間常數范圍的電化學系統(綠色)和電池測試方法(藍色)的動態、頻率相關過程。該圖顯示了電池中各種電化學和物理過程的動力學及其時間常數。電化學技術的種類也被推薦用于不同過程的研究。 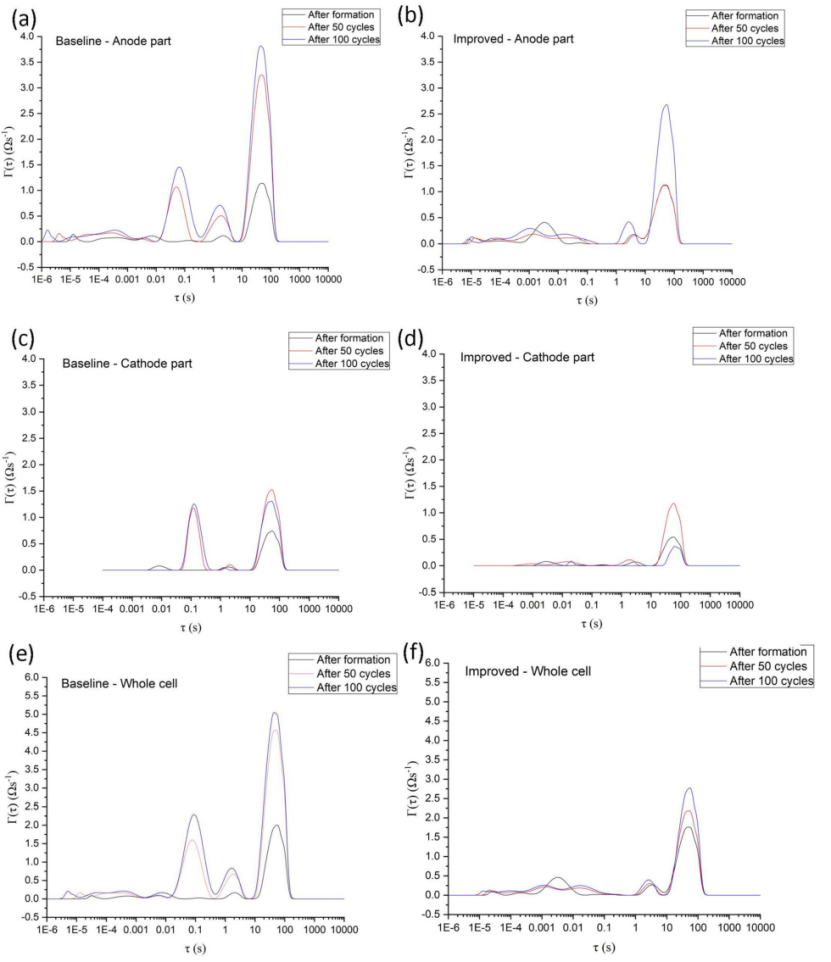
【圖8】DRT 在不同的老化狀態。a 基準負極,b 改進的負極,c 基準正極,d 改進的正極,e 基準全電池,f 改進的全電池。
固態電池最近引起了很多關注。EIS 的基本原理也適用于所有固態電池。全固態電池的一個獨特特征是固態電解質的本質是固態電解質的電荷載流子。
與電極之間的電流由離子物質承載的液體電解質不同,固態電解質中可能存在電子傳導性。雖然它很小,但電子導電性會造成潛在的漏電流,這相當于在正極和負極之間連接了一個大電阻。
理論上,電子電導率和離子電導率可以很容易地使用 DC 和 AC 分開。但實驗上很難獲得可重復的測量結果。
使用精心設計的電化學電池進行簡單的交流阻抗測量和擬合可能是有利的。在阻抗測量期間,可以使用離子阻擋或電子阻擋或氧化還原電極。
離子阻擋電極可以是金屬,例如 Pt 和 Au 或熱解石墨,離子阻擋電極是惰性的,不利于界面處的電荷轉移。電子阻擋電極是高離子電導率材料,其電子電導率可忽略不計。
因此,僅測量離子電導率。如果使用氧化還原電極,例如鋰金屬,則離子電導率和電子電導率都包含在阻抗測量中。
4、總結與展望
EIS 是一種強大的電化學研究技術。它連接了穩態和瞬態,因此可以在放電或充電的不同階段研究電極的動力學。作者希望它可以正確地最大限度地發揮其潛力,希望本次討論能為儲能領域的研究人員,尤其是非專業電化學工作者提供一個有用的起點。
審核編輯:劉清
-
阻抗匹配
+關注
關注
14文章
348瀏覽量
30760 -
電荷
+關注
關注
1文章
617瀏覽量
36113 -
電池系統
+關注
關注
9文章
387瀏覽量
29896
原文標題:Nature子刊: 怎樣做靠譜的阻抗測試?
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦




 對電池系統進行可靠阻抗測量的流程總結
對電池系統進行可靠阻抗測量的流程總結











評論