一、全文概要
電解質(zhì)和相關(guān)的界面構(gòu)成了支持新興電池化學(xué)的關(guān)鍵組成部分,這些電池提供了誘人的能量密度,但卻涉及劇烈的相位和復(fù)雜結(jié)構(gòu)。設(shè)計更好的電解質(zhì)和相間物是這些電池能被成功應(yīng)用的關(guān)鍵。作為唯一一個與設(shè)備中其他所有部件相連接的部件,電解質(zhì)必須同時滿足多個標(biāo)準(zhǔn)。這些標(biāo)準(zhǔn)包括傳輸離子,同時在電極之間絕緣電子,并保持對極端化學(xué)性質(zhì)的電極的穩(wěn)定性:強(qiáng)氧化性正極和強(qiáng)還原性負(fù)極。在大多數(shù)先進(jìn)的電池中,兩個電極的工作電位遠(yuǎn)遠(yuǎn)超過了電解質(zhì)的熱力學(xué)穩(wěn)定性極限,因此,其中的穩(wěn)定性必須通過電解質(zhì)和電極之間的犧牲反應(yīng)形成的中間相來實現(xiàn)。最近,來自芝加哥大學(xué)的Y. Shirley Meng和來自美國阿貢國家實驗室的Venkat Srinivasan和Kang Xu在國際期刊《Science》上發(fā)表題為“Designing better electrolytes”的綜述性文章。該文章綜述了電池的界面化學(xué),為未來的電解質(zhì)的發(fā)展指明方向。

二、正文部分 01 研究亮點(diǎn)  綜述了電池的界面化學(xué)的研究現(xiàn)狀,指明了界面的關(guān)鍵基本屬性,如離子在界面上的傳輸速度和機(jī)制仍然未知,但離子溶解鞘的結(jié)構(gòu)已被確定為指導(dǎo)界面形成過程的有效工具。 ? 02 圖文導(dǎo)讀
綜述了電池的界面化學(xué)的研究現(xiàn)狀,指明了界面的關(guān)鍵基本屬性,如離子在界面上的傳輸速度和機(jī)制仍然未知,但離子溶解鞘的結(jié)構(gòu)已被確定為指導(dǎo)界面形成過程的有效工具。 ? 02 圖文導(dǎo)讀 
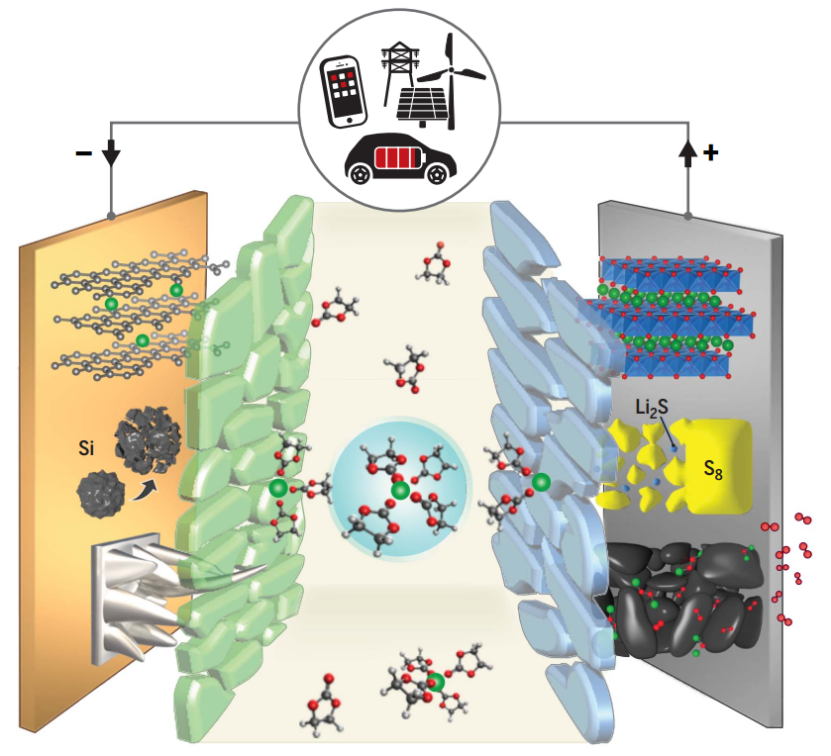
電解質(zhì)和相關(guān)的互化物在支持多樣化的電池化學(xué)中起著核心作用。在負(fù)極一側(cè)(左),電解質(zhì)必須形成一個中間相,以防止石墨負(fù)極剝落,并且容納硅電極的急劇體積變化,還要抑制樹枝狀金屬鋰的生長。在正極一側(cè)(右側(cè)),中間相對于防止與電解質(zhì)發(fā)生不可逆反應(yīng)、維持過渡金屬氧化物的晶格結(jié)構(gòu)、抑制多硫化物物質(zhì)的跨電池穿梭以及協(xié)助空氣正極的復(fù)雜三相反應(yīng)至關(guān)重要。在所有這些情況下,相間層必須在絕緣電子傳輸?shù)耐瑫r實現(xiàn)離子傳輸。
1.通過中間相運(yùn)行的LIB
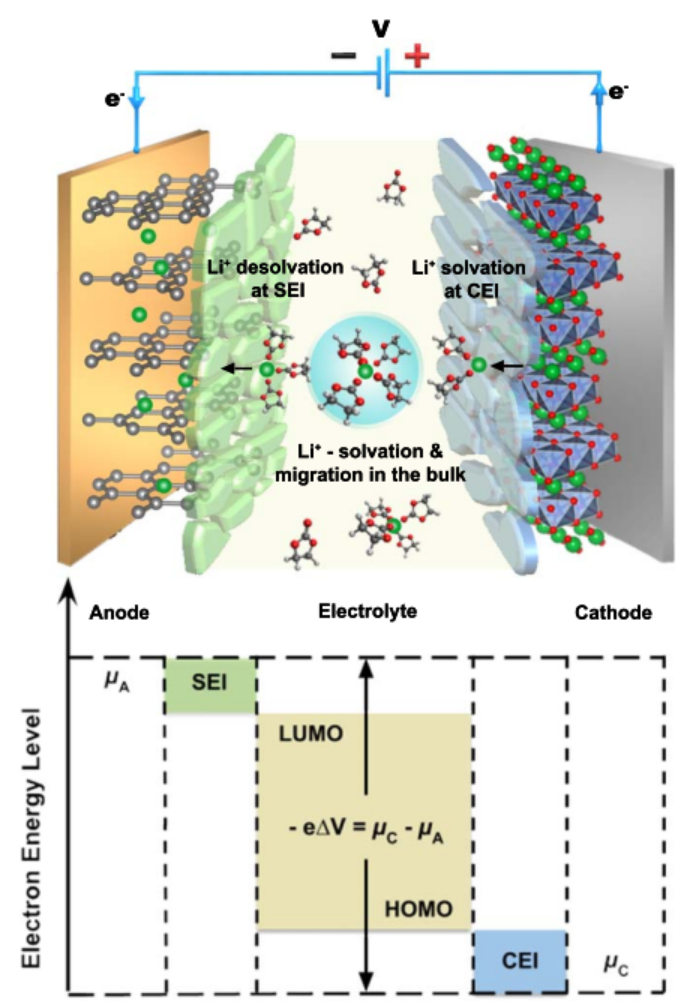
圖 1.電解質(zhì)的工作原理。電解質(zhì)必須傳導(dǎo)離子,絕緣電子并保持穩(wěn)定,同時與所有電池組件相連接。當(dāng)正極和負(fù)極在超出LUMO和HOMO之間封閉區(qū)域的電位下運(yùn)行時,就會出現(xiàn)重大挑戰(zhàn),因為其必須形成界面以確保電池化學(xué)的可逆性。
LIB的能量密度和充電能力依賴于中間相的特性(圖1)。由于LIB中石墨負(fù)極的電位(相對于Li的~0.01V)遠(yuǎn)遠(yuǎn)超出了電解質(zhì)的熱力學(xué)穩(wěn)定窗口,正如最高占有分子軌道(HOMOs)和最低未占有分子軌道(LUMOs)所標(biāo)志的那樣,可逆的鋰化/去鋰化化學(xué)反應(yīng)依賴于界面的保護(hù)性能。最先進(jìn)的鋰離子電池所使用的電解質(zhì)因制造商和所使用的正極化學(xué)性質(zhì)的不同而不同;然而,它們幾乎都遵循由六氟磷酸鋰(LiPF6)組成骨架,然后溶解在碳酸鹽酯類溶劑的混合物中,這是平衡每個電池組件的要求的結(jié)果,特別是在低電位(?0.01 V相對于Li+/Li)和過渡金屬氧化物或磷酸鹽正極在高電位(?3.5至4.5 V相對于Li+/Li)下更是如此。現(xiàn)在人們普遍認(rèn)為,LIB中的SEI主要來自于碳酸鹽溶劑和鹽類陰離子的還原分解。這些物質(zhì)通常以分層結(jié)構(gòu)排列,最內(nèi)層是更多的無機(jī)物(LiF和Li2O),外層是更多的有機(jī)物(半碳酸鹽、草酸鹽、烷氧基化物和聚合物)。另外,與SEI相比,人們對CEI的了解要少得多。在某些情況下,甚至CEI的存在也有爭議。盡管研究表明,傳統(tǒng)的電解質(zhì)在某些條件下可以支持電池運(yùn)行到5.6V。但在必須承受長期循環(huán)的電池中,對CEI的需求仍然從根本上受到熱力學(xué)因素不匹配的驅(qū)動(圖1)。與完全覆蓋負(fù)極的SEI不同,正極表面的沉積物(主要是無機(jī)氟化物和氧化物)經(jīng)常被發(fā)現(xiàn)是分散的和不連續(xù)的,這大大引起了人們對它們是否真的具有保護(hù)作用的懷疑。
2.為新興電池化學(xué)設(shè)計電解質(zhì)和界面
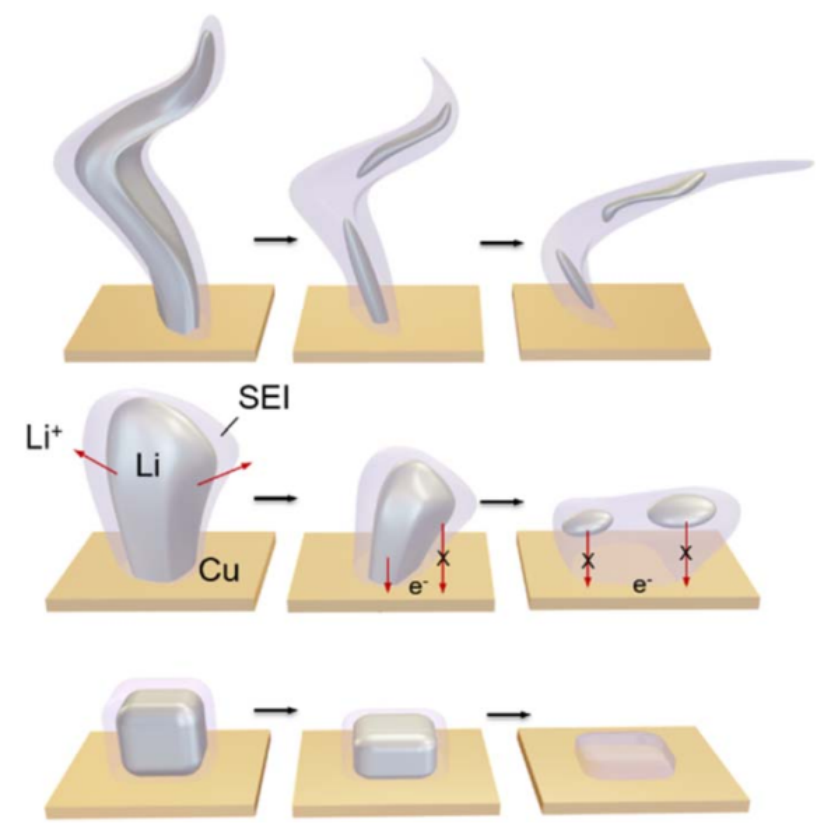
圖2. Li0負(fù)極的挑戰(zhàn)。設(shè)計一種電解質(zhì)和相關(guān)的SEI以消除樹枝狀和死Li0的危險形態(tài)是實現(xiàn)可充電鋰金屬電池的關(guān)鍵。上圖:不均勻的SEI促進(jìn)樹枝狀Li0在對Li+更有導(dǎo)電性的位置生長,而在樹枝狀根部附近的溶解導(dǎo)致死Li0與集電器相隔離。中圖和下圖:設(shè)計更好的電解質(zhì)和相間層可以引導(dǎo)密集型Li0的生長,從而使低長徑比的晶體成為首選,這意味著它們在重復(fù)電鍍和剝離過程中可以保持電氣連接。
更為嚴(yán)峻的挑戰(zhàn)與鋰金屬(Li0)負(fù)極有關(guān),由于其能量密度,鋰金屬正被重新視為終極負(fù)極材料。鋰的高能量伴隨著極端的反應(yīng)性,這與過度和持續(xù)的相間生長有關(guān),其最終導(dǎo)致鋰電極的低效率和危險的形態(tài)(如樹枝狀和死鋰)。確定具有有效SEI化學(xué)性質(zhì)的電解質(zhì)已成為一個投入巨資的研究方向,目標(biāo)是鋰的沉積可以在高庫侖效率(CE%)下均勻進(jìn)行。特別重要的是要規(guī)避分形的、大長寬比的晶體(圖2)。這些晶體要么滲透到電池中,形成內(nèi)部短路,要么在根部附近容易被切斷,形成高度危險的死Li0。迄今為止確定的最佳電解質(zhì)是基于氟化醚分子而不是酯類,它可以達(dá)到99.9%的CE%,并在長期循環(huán)中抑制危險的Li0形態(tài)。電解質(zhì)成分和相間化學(xué)的這種普遍氟化改善了Li0的可逆性,這歸因于Li0在LiF上成核的高表面能。另外,在正極方面,對新興化學(xué)的追求一直集中在尋找極高的能量密度或獨(dú)立于Co或Ni的材料,LIB化學(xué)一直嚴(yán)重依賴這兩種元素,但它們要么在地殼中極為罕見,要么只能在高地緣政治或道德風(fēng)險下獲得。作為近期目標(biāo),已經(jīng)探索了相對更成熟的材料,如改進(jìn)的插層化合物,其中一些已經(jīng)被LIB行業(yè)逐步采用。從概念上講,它們與最先進(jìn)的LIB正極材料沒有明顯的區(qū)別,但其晶格的結(jié)構(gòu)修改使它們能夠在更高的電位下容納更多的Li+。
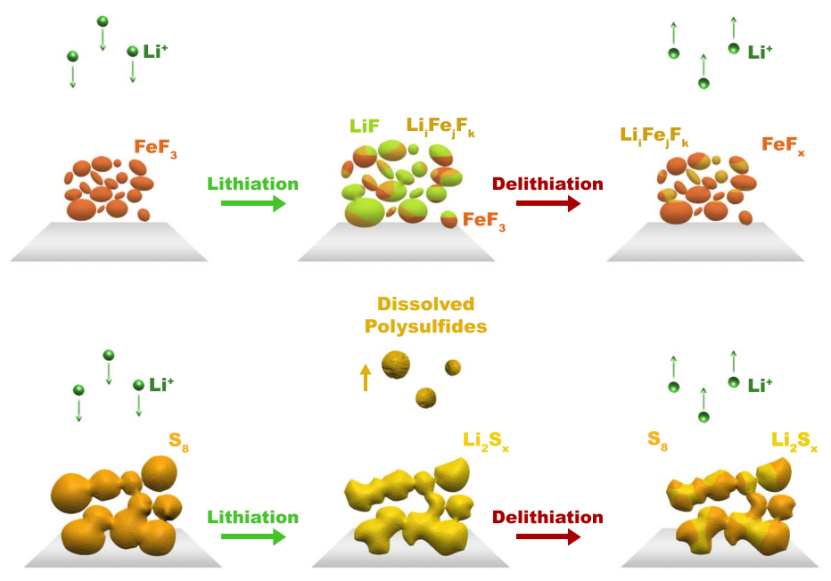
圖3. 新興的轉(zhuǎn)換-反應(yīng)電池化學(xué)。氟化鐵(上圖)和硫(下圖)都依靠劇烈的結(jié)構(gòu)破壞和結(jié)構(gòu)重組來提供高容量和能量密度,但其可逆性遇到了嚴(yán)重的挑戰(zhàn),因為幾乎不可能完全恢復(fù)原始結(jié)構(gòu),而且產(chǎn)生的活性材料可能溶于電解質(zhì)并離開電極空腔。
利用轉(zhuǎn)化反應(yīng)化學(xué)物質(zhì)的更激進(jìn)的材料被認(rèn)為是長期目標(biāo),主要包括金屬氟化物、硫化物、元素硫,甚至是氧氣,這些材料在充電電池研究的早期都沒有成功應(yīng)用。與結(jié)構(gòu)變化最小的插層型電極不同,這些電極材料在放電過程中經(jīng)歷了完全的重組,使容量大大增加,但代價是可逆性降低,因為幾乎不可能完全恢復(fù)原來的電極結(jié)構(gòu)(圖3)。由于在納米結(jié)構(gòu)材料的合成方面取得了進(jìn)展,這些曾經(jīng)無法使用的化學(xué)材料可以以更高的可行性被重新審視。因此,相應(yīng)的電解質(zhì)和界面需要抵抗來自金屬氟化物或硫化物產(chǎn)生的納米金屬顆粒的強(qiáng)大催化活性,抑制可溶性多硫化物在電池中的寄生穿梭,并對氧還原產(chǎn)生的活性過氧化物或超氧化物中間物保持惰性。迄今為止,在解決這些挑戰(zhàn)方面所做的改進(jìn)十分有限,這為研究人員留下了廣闊的探索空間。
3.新概念電解質(zhì)和界面相
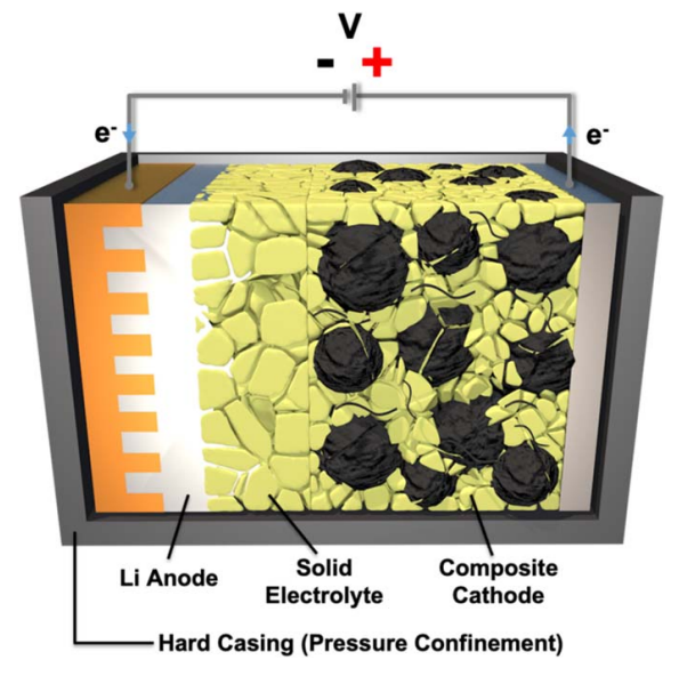
圖4. 固體與固體的連接。在全固態(tài)電池中,固體材料的連接遇到了活性負(fù)極/正極材料的固體接觸點(diǎn)和SEs的挑戰(zhàn)和機(jī)遇。
SE當(dāng)前的首要挑戰(zhàn)仍然來自固-固界面,因為SE不能流動或滲透到電極的孔隙結(jié)構(gòu)中。克服物理接觸問題的一個常見方法是加入受控數(shù)量的液體電解質(zhì)來填充空隙和間隙。這使系統(tǒng)的固體含量減少,并導(dǎo)致混合電解質(zhì)或半固態(tài)。相反,固-固接觸的挑戰(zhàn)也可以變成一種優(yōu)勢,使鋰或硅負(fù)極的三維(3D)結(jié)構(gòu)成為可能,因為相間反應(yīng)只能發(fā)生在這些接觸點(diǎn)上,而大的體積膨脹和收縮可以通過適當(dāng)?shù)娜S設(shè)計和動態(tài)壓力控制來適應(yīng)(圖4)。SEs的單離子導(dǎo)電性質(zhì)消除了濃度極化,并允許容納導(dǎo)致非均勻反應(yīng)和最終容量消退的局部效應(yīng)。盡管量化電化學(xué)和機(jī)械的耦合現(xiàn)象仍然是電池領(lǐng)域的一個關(guān)鍵障礙,但最近的研究工作有很大進(jìn)展,已經(jīng)科研人員制備出實驗室規(guī)模的電池同時具有穩(wěn)定和長的循環(huán)壽命。
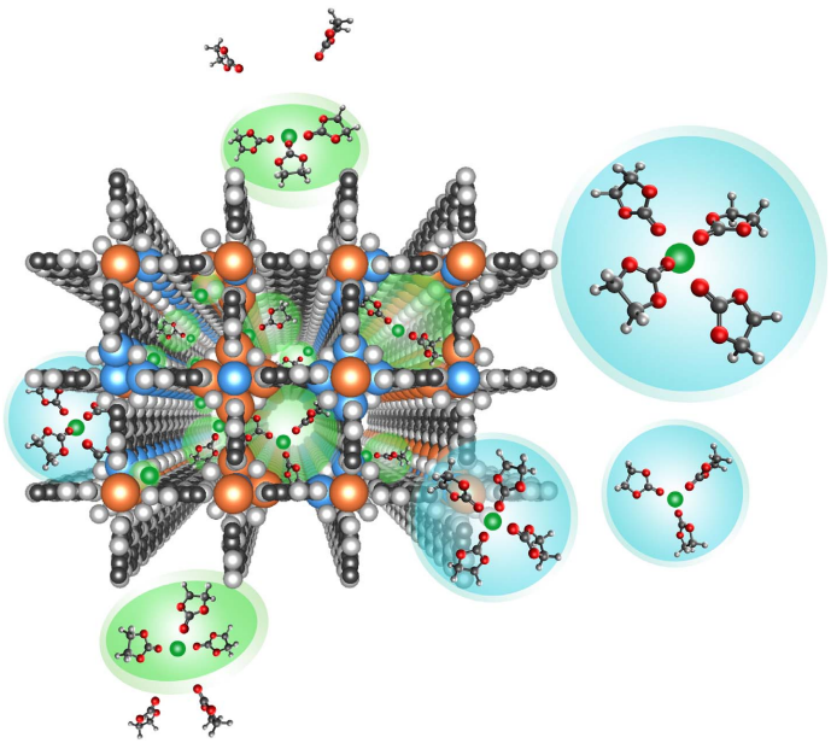
圖5. 納米封存中的溶解作用。當(dāng)宿主環(huán)境的大小與離子溶解鞘相當(dāng)時,宿主與離子或其溶劑成員之間的強(qiáng)制相互作用變得不可避免,這誘發(fā)了離子的部分或完全脫溶并產(chǎn)生了一系列不尋常的特性
大多數(shù)離子溶解鞘的尺寸從一埃到近一納米不等,取決于溶劑分子和溶解數(shù)。隨著多樣化的納米材料的出現(xiàn),一個有趣的問題出現(xiàn)了:被溶解的離子在這些亞納米結(jié)構(gòu)中會有什么表現(xiàn)?當(dāng)前已經(jīng)有許多關(guān)于電解質(zhì)在納米壓制中的不尋常特性的報告。例如,當(dāng)溶解的四烷基銨陽離子被迫進(jìn)入小至0.65納米的孔隙時,出現(xiàn)了反常的電容。當(dāng)把傳統(tǒng)的LIB電解質(zhì)注入平均直徑約40納米的陶瓷-聚合物復(fù)合體的納米孔中時,出現(xiàn)了明顯不同的Li0負(fù)極的相間行為和形態(tài)。當(dāng)醚基電解質(zhì)被凍結(jié)在由金屬有機(jī)框架結(jié)構(gòu)創(chuàng)造的0.29納米的亞納米通道中時,電化學(xué)穩(wěn)定性窗口被大大擴(kuò)展。最后,當(dāng)同樣的聚合物被嵌入到直徑為40納米的陶瓷主機(jī)的通道中時,沿陶瓷-聚合物界面發(fā)生了遠(yuǎn)高于相應(yīng)的大塊聚合物電解質(zhì)的超快離子傳輸。盡管這些分散的現(xiàn)象似乎沒有什么聯(lián)系,而且每項研究中的研究者都提供了不盡相同的理由,但所有這些都有一個趨同的因素:在納米結(jié)構(gòu)環(huán)境中,溶解的離子很可能與宿主材料的表面存在相互作用(圖5)。在此過程中,離子發(fā)生了部分或甚至完全的脫溶,產(chǎn)生的電解質(zhì)的化學(xué)狀態(tài)還沒有被完全理解。
4.展望:光明而曲折的未來
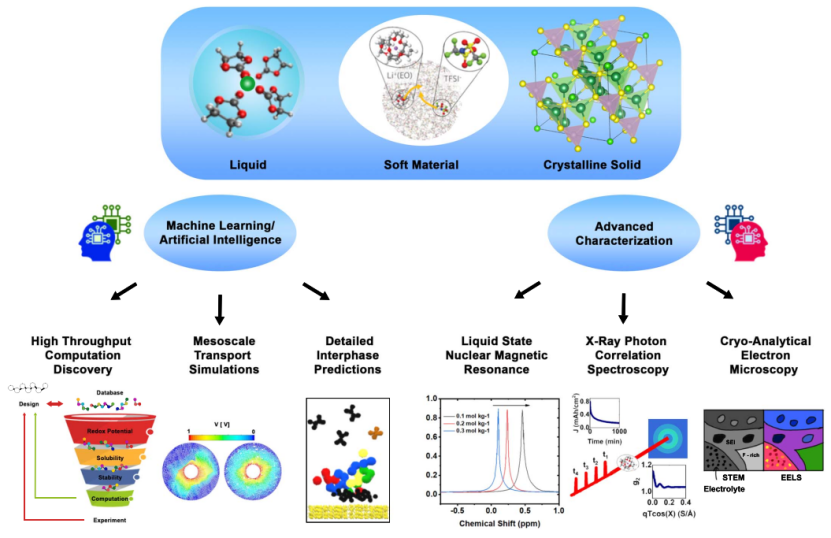
圖6. 在分子分辨率下看到電解質(zhì)的動態(tài)。在計算模擬和建模的幫助下,先進(jìn)的原位/現(xiàn)場表征為理解和發(fā)現(xiàn)電解質(zhì)及其相間性帶來了新的視野。
為了回答前面提到的問題,需要開發(fā)新的表征技術(shù),特別是那些在原位/現(xiàn)場條件下運(yùn)行的技術(shù)和那些具有極高的空間和時間分辨率的技術(shù)。在過去的幾十年里,盡管已經(jīng)開發(fā)了許多先進(jìn)的表征工具來探測和量化相間的物質(zhì),但直接探測電解質(zhì)的工具仍然十分缺乏。鑒于典型電解質(zhì)的非晶體和快速離子動力學(xué)性質(zhì),具有高化學(xué)敏感性和局部結(jié)構(gòu)全散射的光譜方法是最合適的,因為它們能檢測長程無序排列。如圖6所示,全面了解電解質(zhì)中的溶解結(jié)構(gòu)、相關(guān)的相間化學(xué)、其沿二維和三維長度尺度的分布,以及在電化學(xué)過程中化學(xué)如何演變,可以通過研究使用一系列技術(shù)組合收集的大型數(shù)據(jù)集來實現(xiàn)。這些技術(shù)包括液體和固體核磁共振、從X射線或中子散射得到的差分PDF以及配備斷層掃描和電子能量損失光譜的低溫分析電子顯微鏡。
審核編輯 :李倩
-
電極
+關(guān)注
關(guān)注
5文章
807瀏覽量
27163 -
電解質(zhì)
+關(guān)注
關(guān)注
6文章
805瀏覽量
20017
原文標(biāo)題:Science綜述:設(shè)計更好的電解質(zhì)
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關(guān)注!文章轉(zhuǎn)載請注明出處。
發(fā)布評論請先 登錄
相關(guān)推薦
胡先羅教授在AEM發(fā)表研究:探索寬溫電解質(zhì)設(shè)計新路徑

一種創(chuàng)新的超薄固體聚合物電解質(zhì)
固態(tài)電池中復(fù)合鋰陽極上固體電解質(zhì)界面的調(diào)控

無極電容器有電解質(zhì)嗎,無極電容器電解質(zhì)怎么測
具有密集交聯(lián)結(jié)構(gòu)的明膠基水凝膠電解質(zhì)(ODGelMA)
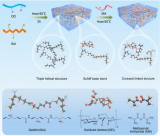
氧化物布局格局一覽 氧化物電解質(zhì)何以撐起全固態(tài)?
鈮酸鋰調(diào)控固態(tài)電解質(zhì)電場結(jié)構(gòu)促進(jìn)鋰離子高效傳輸!
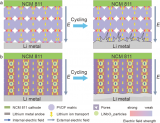
電解質(zhì)電極信號采集控制板

請問聚合物電解質(zhì)是如何進(jìn)行離子傳導(dǎo)的呢?
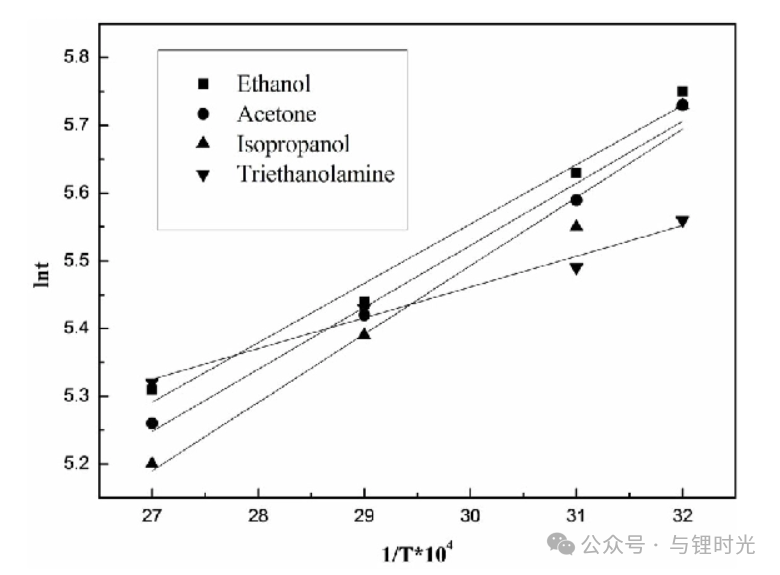
不同類型的電池的電解質(zhì)都是什么?
新型固體電解質(zhì)材料可提高電池安全性和能量容量
固態(tài)電解質(zhì)離子傳輸機(jī)理解析
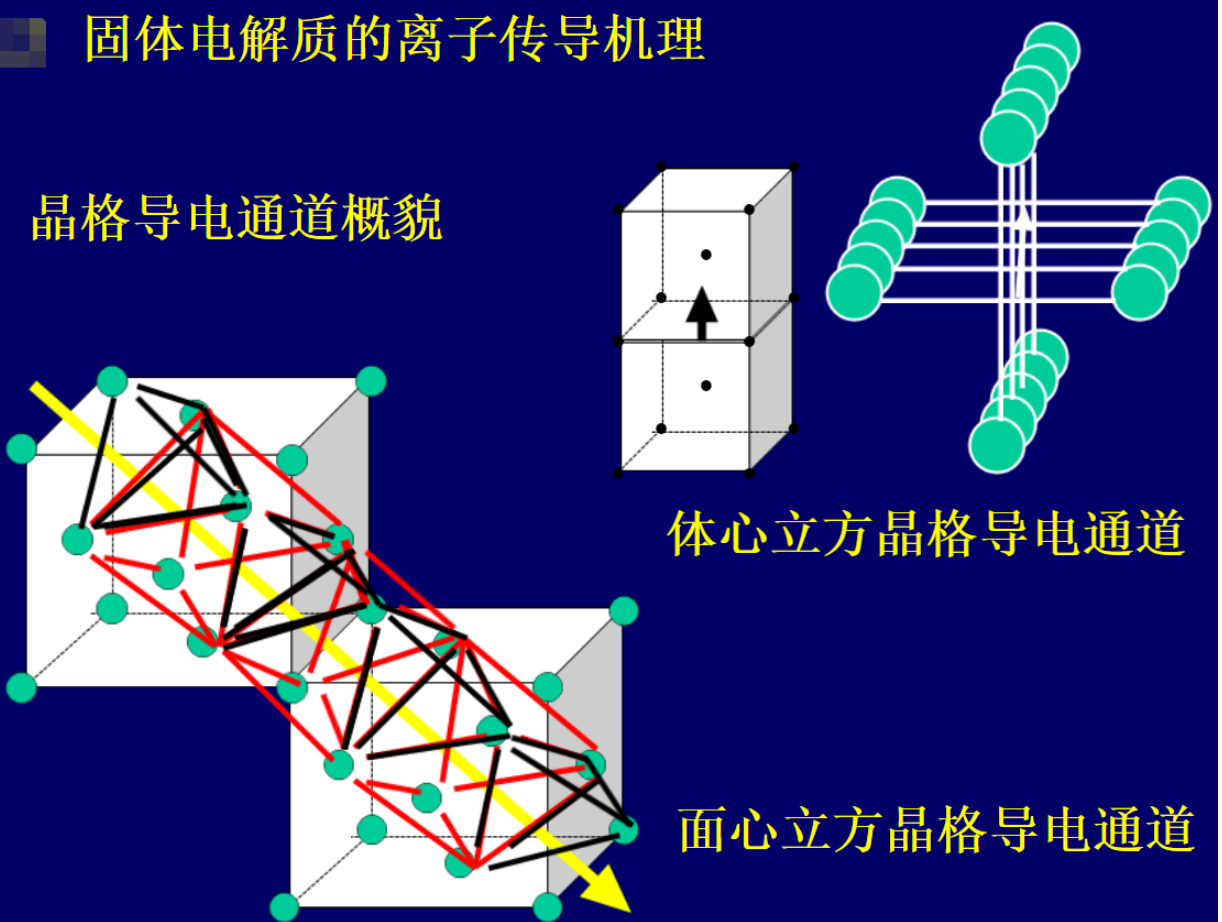
關(guān)于固態(tài)電解質(zhì)的基礎(chǔ)知識
一種有機(jī)-無機(jī)非對稱固態(tài)電解質(zhì),實現(xiàn)長循環(huán)穩(wěn)定的高壓鋰電池





 Science綜述:設(shè)計更好的電解質(zhì)
Science綜述:設(shè)計更好的電解質(zhì)











評論