當今使用的電池有很多種,其中最著名的一種是鋰離子 (Li-ion) 電池。鋰離鋰離子電池獲得2019年諾貝爾化學獎。雖然鋰離子電池在現代技術中的重要性不可低估,但實際上它們只是屬于金屬離子電池類別的眾多電池之一,但它們的使用更為廣泛,因為它們更高效、更安全。
不同的基本細胞化學
所有金屬離子電池都是可充電電池。在談到金屬離子電池的化學時,制造電池涉及到很多材料化學。每個金屬離子電池由兩個電極(陽極和陰極)、電解質、隔膜和外部電子電路組成。在討論金屬離子電池時,我會想到四個主要例子。最明顯的例子是鋰離子電池,其他還有鋁離子(Al-ion)、鈉離子(Na-ion)和鋰離子聚合物電池(LiPo)。這四種電池的主要區別在于電極、電解質和作為電池內活性電荷載體的離子的組成。
鋰離子電池通常有一個鋰基陰極,它可以由氧化鋰、層狀鋰氧化物或聚陰離子材料制成。陽極是碳基的,但這里的材料可能會有很大差異。長期以來的選擇是石墨,但最近的發展已經看到使用石墨烯和石墨烯-石墨混合電極以及其他各種碳復合材料作為陽極材料。電解質是液體和鋰鹽,可有效傳輸鋰離子。電解質是各種有機和非水成分的復雜混合物,例如碳酸亞乙酯(或二亞乙基)與 LiPF6、LiAsF6、LiClO4、LiBF4 或 LiCF3SO3 陰離子鹽。鋰離子電池是最有效的,因為鋰離子可以進入電極,有效地進行電化學反應,并輕松退出電極。這使得電池的充電和放電循環更有效率。
鈉離子電池的成分與鋰離子電池相差無幾,因為兩種活性離子都具有一個正電荷。在鈉離子電池中,鈉離子是電荷載體,陰極是由鈉過渡金屬氧化物制成的復合材料,陽極通常由無定形碳制成。電解質本質上可以是水性或非水性的,但在鋰離子電池中發現的非水性陰離子鹽電解質的鈉當量是最廣泛使用的,NaPF6 是常見的選擇。
鋁離子電池還沒有那么成熟,但顯示出很大的前景。他們進行大量研究的主要原因是鋁攜帶三個電荷,而鋰只有一個,因此它有可能儲存更大的能量。但是鋁離子的大量有效電荷使得它們一旦發生電化學反應就更難離開電極,這也是為什么我們還沒有看到它們被商業化使用的原因。鋁基材料和石墨往往分別構成陽極和陰極,電解質是由氯化鋁組成的液體,但所有這些基礎領域目前都在開發中,并且可能會隨著新研究產生更有效的材料/化學物質而改變物種。
與其他電池不同的是鋰聚合物電池,它是傳統鋰離子電池的一種變體。兩個電極都由與鋰離子電池相同的材料制成,但電解質是主要區別。電解質不是由非水液體制成,而是由聚合物制成,因此它具有凝膠狀(半固體)稠度,但仍具有足夠的流動性以傳輸鋰離子。鋰聚合物電池中使用的大多數電解質由固體聚合物組成,例如聚(環氧乙烷)(PEO)、聚(丙烯腈)(PAN)、聚(甲基丙烯酸甲酯)(PMMA)或聚(偏二氟乙烯)(PVdF) ),它們已分散在有機溶劑中,使其具有所需的凝膠狀稠度。
金屬離子電池的工作原理
上面我們討論了用于構建電極的材料和用作電解質的材料。大多數金屬離子電池的基本工作機制是相同的,所以舉一個例子比討論所有電池的工作原理更容易。鋰離子電池就是最好的例子;但是,對于鋁離子和鈉離子電池,如果分別用鋰離子代替鋁離子和鈉離子,原理是相同的。應該注意的是,在陽極和陰極發生的特定電化學反應對于所有電池都是不同的。因此,有太多的電化學反應無法詳細提及不同的反應。
可充電電池有兩種主要機制:充電和放電。充電機制是電池儲存能量的過程,而放電是在它釋放能量時——例如,當設備打開時。當電池充電時,來自為電池充電的電源的電子與陰極中的鋰離子結合。這導致離子通過電解質和隔板移動到陽極,在那里它們通過陽極材料中的分子孔進入 - 這一過程稱為嵌入。然后能量以束縛電子的形式儲存在陽極內的鋰離子中。當裝有電池的設備打開時,陽極會發生氧化反應,導致鋰離子離開陽極并移動到(并嵌入)陰極。然后釋放存儲的電子以產生為設備供電的電流。如果電池未被使用或充電,則鋰離子會解吸到電極之間的電解質介質中。
結論
大多數金屬離子電池的工作方式相似,主要區別在于構成電極和電解質的化學成分,這反過來會影響電池內發生的電化學反應。對于使用不同電解質的相同電池,這些電化學反應也可能不同。在所有不同的金屬離子電池中,鋰離子電池是最有效的,因為它們可以輕松地在電極之間移動并進行必要的電化學反應,而不會卡在電極的分子孔中。鋁電池顯示出很大的前景,但在商業使用之前,必須首先解決離開電極的電荷重離子的問題。
審核編輯黃昊宇
-
電池
+關注
關注
84文章
10473瀏覽量
129041
發布評論請先 登錄
相關推薦
石墨負極在鋰離子電池中的發展與儲鋰機制
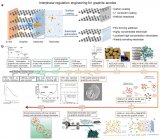




 金屬離子電池的化學
金屬離子電池的化學















評論