研究背景
與液態電解質發生副反應形成非活性鋰是鋰金屬電池失效的原因之一。為了抑制非活性鋰的形成和生長,需要進一步了解非活性鋰的形成機制和組成。但是,使用大多數現有的分析技術進行研究具有挑戰性,特別是在研究具有復雜成分的SEI時。除了液態電解質外,氣態物質的形成,如氫、乙烯、二氧化碳(CO2)等,也會自發地與鋰金屬反應,但目前氣體與鋰金屬之間的反應很少被討論。鋰金屬電池中鋰能夠與氫氣反應生成氫化鋰(LiH)。然而,LiH與循環過程中形成的氫氣之間的直接相關性還不完全清楚。此外,是否有其他氣體可以與鋰金屬反應,形成其他非活性鋰物種?這些都需要進一步探究。
成果簡介
近日,廈門大學楊勇教授在Nature Communications上發表了題為“Gas induced formation of inactive Li in rechargeable lithium metal batteries”的論文。該工作以碳酸乙烯為例,研究了產氣反應對非活性鋰形成的影響。碳酸乙烯是石墨基負極常用的電解質成分,但與鋰金屬負極不兼容。通過質譜滴定結合13C和2H同位素標記,發現碳酸乙烯分解不斷釋放乙烯氣體,乙烯氣體進一步與金屬鋰反應生成非活性的物種LiH和Li2C2。此外,相場模擬表明,非離子導電的氣態物質可能導致鋰離子分布不均勻,促進枝晶和死鋰的形成。通過優化電解質組成可以選擇性地抑制乙烯氣體的形成,以限制鋰金屬和石墨基負極中LiH和Li2C2的形成。
研究亮點
(1)本文首先利用原位質譜(OMS)將LiH的演化與氣體形成聯系起來,表明乙烯是整個循環過程中連續形成的主要氣體種類。 (2)利用同位素標記的質譜滴定(MST)技術,證明了乙烯和鋰金屬可以反應生成LiH和碳化鋰(Li2C2)。 (3)通過相場模擬證明了氣泡的存在會改變界面電場和離子濃度的分布,從而導致非均勻的Li金屬沉積和死Li形成。抑制乙烯的形成可以進一步抑制LiH和Li2C2的形成。
圖文導讀
首先,采用MST技術作為定量方法,使用1 M LiPF6/碳酸乙烯(EC):甲基碳酸乙酯(EMC)(基線)研究LiFePO4||Cu電池中形成的非活性鋰中LiH的演變。氘水(D2O)是與非活性Li反應生成各種氣體的滴定劑,其中HD(半氘氫)氣體是由LiH反應產生的:LiH+D2O=LiOD+HD↑。HD信號在質譜中呈現出獨特的質荷比(m/z=3)值,因此可用于跟蹤LiH的演化(圖1a)。同時,D2O與死鋰反應生成D2(m/z=4),其演化代表死鋰的形成。從圖1b可以看出,HD和D2信號的積分面積都隨著循環數的延長而不斷增加,表現為不可逆的積累,導致活性Li的持續損失。 為了將LiH與H2氣體的形成聯系起來,采用原位質譜儀(OMS)監測使用基準電解質的無負極電池中的氣體演化,包括H2(m/z=2)、乙烯(C2H4)(m/z=28)、乙烷(C2H6)(m/z=30)和CO2(m/z=44)(圖1c)。在第一次充電過程中主要觀察到H2的形成,但在長循環中沒有檢測到(圖1c)。H2的形成可能來自水雜質的分解。
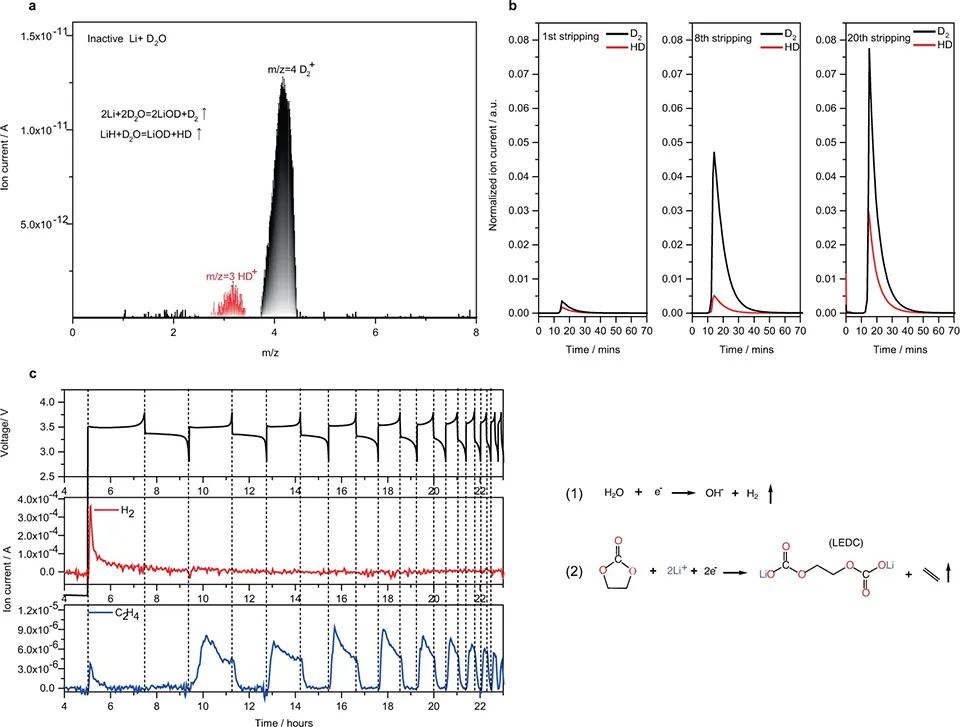
圖 1、(a)非活性Li與D2O反應產生的氣體產物質譜。(b)死Li和LiH的質譜滴定結果。(c)在2.8 V~3.8 V、0.75 mA cm?2下循環時,Cu||LiFePO4電池的電壓曲線,以及相應的H2(m/z=2)和C2H4(m/z=26)的原位質譜結果。與H2相比,C2H4在整個循環過程中持續演化(圖1c)。對于每一個循環,C2H4信號在充電(Li沉積)過程中開始上升,在電流反向時突然衰減,這表明C2H4的形成伴隨著Li沉積。C2H4是EC通過雙電子還原反應產生的分解產物:EC+2e-→(CH2OCO2Li)2+ C2H4。OMS和MST結果表明,LiH的形成和電解液的分解是同時進行的。考慮到有機電解質是質子的主要來源,這一同時發生的過程意味著LiH的形成與C2H4的演化之間存在潛在的相關性。 鋰金屬與乙烯反應可能生成LiH和Li2C2:

因此,可以用乙炔(C2H2)(m/z=26)的信號來驗證Li2C2的存在。對于正在運行的電池,MST結果已經觀測到了LiH。然而,Li2C2在循環過程中是如何演化的? 本文采用MST技術研究了Cu||LiFePO4電池中形成的非活性Li中Li2C2的存在和演化。圖2a顯示了使用H2O滴定劑在基準電解質中循環20次后形成的非活性Li的滴定結果。反應氣體以H2(m/z=2)和CO2(m/z=44)為主,對應于死鋰(或LiH)和二碳酸乙烯鋰(LEDC)的形成。重要的是,信號C2H2(m/z=26)的存在驗證了Li2C2的存在(圖2a),證明了其不可逆性質。對第1、8、20個循環后形成的非活性Li進行了MST測量,發現Li2C2(圖2b)與LiH(圖2c)的演化模式相似。這兩個非活性Li物種的相互形成和增加也暗示了式1的可行性。
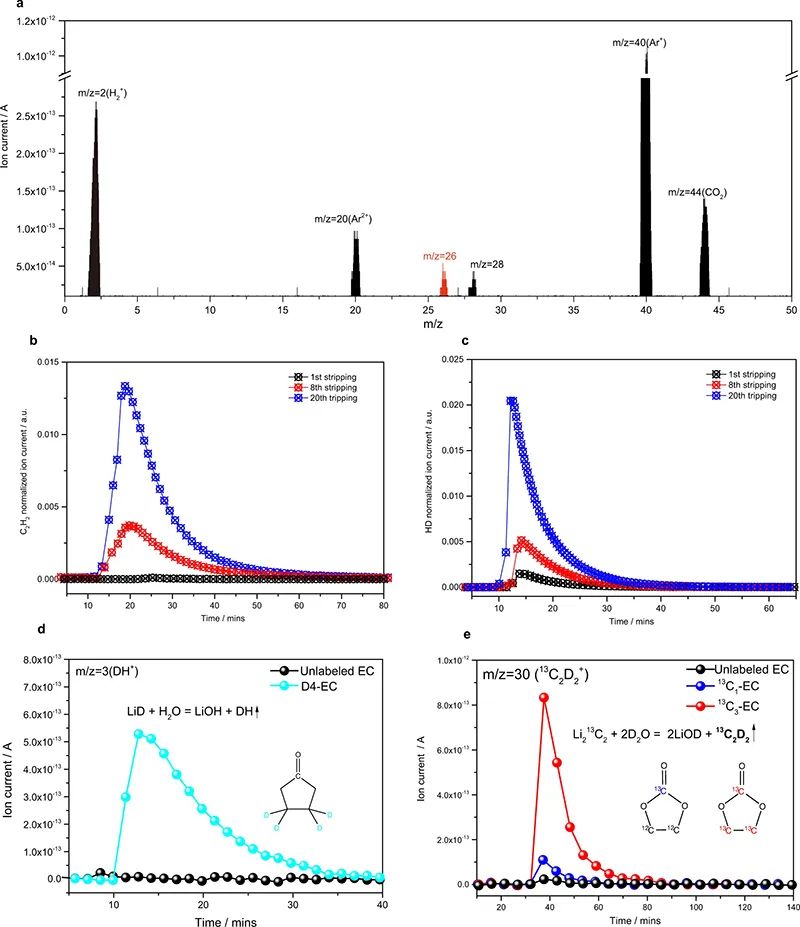
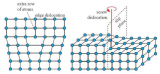
圖 2、(a)用H2O滴定非活性Li的質譜結果。(b)C2H2(m/z=26)信號和(c)HD(m/z=3)信號的演化,分別代表Li2C2和LiH的積累過程。(d)在未標記的EC和所有氘化EC(D4-EC)中形成的非活性Li的質譜滴定結果。(e)在未標記的EC、羰基碳標記的EC(13C1-EC)和全碳標記的EC(13C3-EC)中形成的非活性Li的質譜滴定結果。為了進一步證明LiH和Li2C2的形成與EC分解的產物乙烯直接相關,用三種同位素標記的EC:全氘化EC(D4-EC)、羰基碳標記EC(13C1-EC)和全碳標記EC(13C3-EC)取代純的EC(未標記EC),形成LiPF6/EC:EMC電解液。D4-電解質和未標記電解質中形成的非活性Li用H2O滴定。僅在D4-電解質中觀察到DH+(m/z=3)信號,證實LiD的形成。這一結果證實了在EC溶劑中LiH的形成與質子直接相關。此外,當用D2O滴定13C1電解質和13C3電解質中形成的非活性Li時,13C3電解質中主要出現13C2D2+(m/z=30)信號,而13C1電解質和未標記的EC中信號較小。這一結果表明,Li2C2的形成主要與非羰基碳有關,非羰基碳也是C2H4的來源(圖1中的反應2)。 LiH和Li2C2的離子電導率和電子電導率等物理性質對Li金屬負極的界面反應有很大的影響。鋰在Li2C2中的擴散比Li2O和Li2CO3慢得多。LiH和Li2C2的帶隙比Li2O、Li2CO3和LiF的帶隙低,說明其電子導電性較高,不利于電池性能。因此,考慮到離子電導率和電子電導率,LiH和Li2C2并不是理想的SEI物種,它們可能導致界面阻抗大,Li離子分布不均勻。除化學效應外,氣體對電化學過程的力學效應也不可忽視。氣泡會減小電化學活性面積,阻斷離子輸運途徑。首先,用COMSOL模擬研究了氣泡對Li+濃度分布和電場分布的影響。模擬結果表明,氣泡會導致Li+濃度(圖3a)和電場(圖3b)分布不均勻,導致鋰枝晶生長。相場模型進一步描述了沉積Li金屬的形貌。如果沒有氣泡效應,Li+和電場的均勻分布將導致沉積的Li金屬在水平和垂直方向上同時生長,呈現苔蘚型形貌(圖3c)。當氣泡附著在銅箔上時,沉積金屬的水平生長被極大地抑制(圖3d)。在這種情況下,沉積的金屬鋰傾向于形成枝晶。在銅箔上漂浮氣泡的情況下觀察到相同的情況(圖3e)。圖3f總結了沉積Li金屬的長度和寬度,表明不導Li+的氣泡有利于Li枝晶的形成。氣泡的脫離會使一些鋰金屬碎片從體相上懸垂下來,形成死鋰。
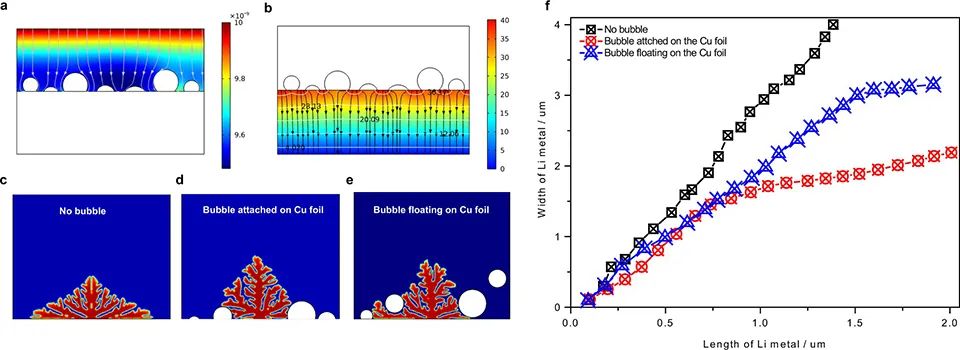
圖 3、氣泡附著在銅表面時(a)Li+濃度和(b)電場分布的模擬。相場模擬研究了氣泡對沉積鋰金屬形態演化的影響:(c)無氣泡,(d)氣泡附著在銅表面,(e)浮在銅箔上。(f)氣泡對枝晶長度和寬度的影響。上述結果表明,LiH和Li2C2的形成與乙烯的演化高度相關,乙烯主要來自EC的分解。因此,通過精心選擇電解質配方來阻礙乙烯的形成是阻止Li2C2和LiH進一步形成的關鍵。首先,去除基準電解質中的EC溶劑,形成1 M LiPF6/EMC(EMC電解質)。在第一次循環后,使用這種無EC電解液的AFBs失去了近99%的容量(圖4a)。EMC電解質有限的循環圈數使得無法得出可靠的結論。因此,保持溶劑(EC:EMC)不變,將基準電解質中的LiPF6替換為二氟化鋰(草酸)硼酸鋰(LiODFB),形成1M LiODFB/EC:EMC。LiODFB先在Li金屬上分解,形成所謂的陰離子衍生SEI,并阻止溶劑的進一步分解。 圖4a顯示,以LiODFB為電解質的AFBs具有優異的循環性能。在相同的循環時間(20 h)下,分別積分了LiODFB和基線電解質原位質譜中的H2面積,結果顯示,LiODFB的H2面積為2.25*10?4 a.u.,基線電解質為1.73*10?4 a.u.,表明兩種不同電解質產生的H2數量相似。根據上述結果和公式1,可以得出結論,使用LiODFB可以極大地抑制EC的分解。
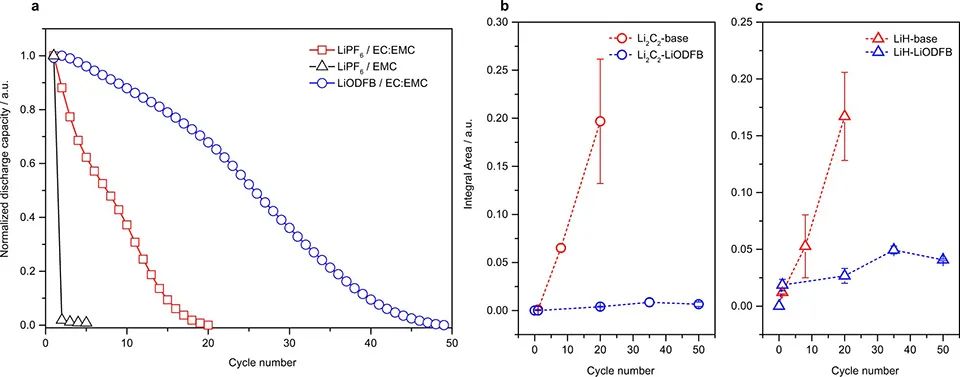
圖 4、(a)在0.75 mA cm?2下,分別使用1 M LiPF6/EMC、1 M LiPF6/EC:EMC(基線)和1 M LiODFB/EC:EMC(LiODFB)電解質的Cu||LiFePO4電池的循環性能。在基線和LiODFB電解質中形成的(b)Li2C2和(c)非活性Li的LiH的相應滴定結果。為了驗證上述假設,進行了MST測試,以測量LiH和Li2C2在LiODFB基電解質中的演變。從圖4可以看出,使用LiODFB電解質時,Li2C2和LiH的信號都被抑制。LiH仍然存在于LiODFB電解質中,但LiH的形成主要來自于第一次循環,并在長循環中緩慢增加,而基線電解質是持續增加。這一結果與LiODFB電解液中氣體的析出過程相吻合:H2在初始循環中占主導地位,C2H4在整個循環過程中受到抑制。
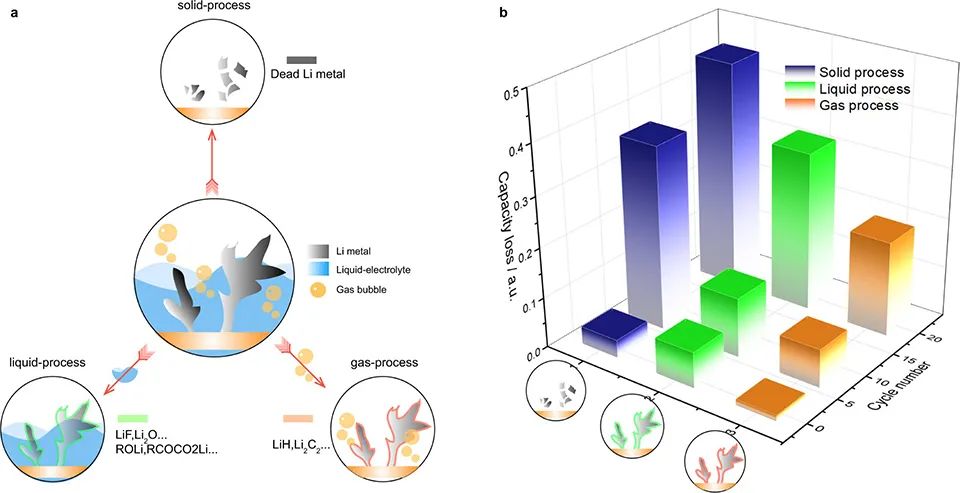
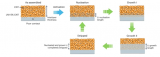
圖 5、(a)非活性鋰形成示意圖(i)固相過程:形成死鋰;(ii)液相過程:液態電解質與鋰金屬反應形成非活性鋰;(iii)氣相過程:氣相與鋰金屬反應形成非活性鋰。(b)基線電解質中非活性的鋰分布。非活性Li的形成一般源于兩個過程:(1)固相過程,即死Li的形成過程只涉及固體(金屬鋰);(2)液相過程,即鋰金屬與液態電解質反應形成SEI的過程(圖5a)。
而第三個過程,即氣體參與生成非活性鋰的過程,則很少被討論。分子動力學(MD)模擬表明,在SEI層的內殼層中存在氣相。在鋰剝離過程中,由于這些氣體的存在,晶體鋰原子很容易被剝離,從而形成死鋰。 圖5b顯示了使用基線電解質在Cu||LiFePO4電池中形成的非活性Li的定量結果。在20次循環后,LiH和Li2C2對非活性Li形成的容量損失貢獻為19.0%。相比之下,在基于LiODFB的電解質中,該值僅為3.2%。在LiODFB電解質中,電池的循環性能較好,這可以歸因于整個循環過程中形成的LiH和Li2C2較少,表明抑制氣體生成對LMBs實現更長的循環壽命具有重要意義。
總結與展望
本工作首次揭示了EC分解的副產物乙烯與LiH具有相似的積累模式。利用MST和同位素示蹤方法,系統地研究了金屬Li與乙烯之間的反應,該反應有助于非活性Li(Li2C2和LiH)的形成。相場模擬結果表明,氣泡的存在會影響沉積Li金屬的形貌,并導致更多的枝晶形成。通過合理選擇電解液配方,能夠抑制乙烯的形成,并進一步抑制鋰金屬和石墨負極中LiH和Li2C2的形成。該研究結果強調了一種被忽視的非活性鋰形成途徑,即氣體誘導的非活性鋰,這在電池研究中很少討論并缺乏全面的研究。這項工作將激發人們探索氣體對鋰和其他堿金屬電池循環性能的影響。
審核編輯 :李倩
-
石墨
+關注
關注
2文章
111瀏覽量
18500 -
電解質
+關注
關注
6文章
805瀏覽量
20018 -
電解液
+關注
關注
10文章
839瀏覽量
23064
原文標題:廈大楊勇Nature子刊:氣體誘導非活性鋰的形成
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
觸覺傳感重磅《Nature》!無線、低功耗、多刺激模式觸覺電子皮膚(附原論文)

激光誘導擊穿光譜技術介紹

激光誘導擊穿光譜技術絕緣子污穢快速定量檢測
絕緣子形成污穢的原理及危害 絕緣子污穢度在線監測
氧化誘導期測試儀

絕緣子形成污穢的原理及危害
一種基于AlGaAs/GaAs漸變帶隙pn結探測器的單像素智能微型光譜儀
氧化誘導期如何檢測?

河南鄭州高新區“一谷多園”產業空間布局形成,華盛昌智能傳感測量儀生產建設項目封頂
氧化誘導期分析儀具備哪些優勢

闡明鋰金屬電池中與溫度相關的鋰沉積/剝離過程以及非活性鋰的演變





 廈大楊勇Nature子刊:氣體誘導非活性鋰的形成
廈大楊勇Nature子刊:氣體誘導非活性鋰的形成












評論