研究背景
在固態煅燒過程中,隨著溫度的升高,材料經歷了復雜的相變,并具有非均相的固態反應和質量傳輸。因此,煅燒化學的精確控制對于合成最先進的富鎳層狀氧化物至關重要。雖然電池的性能取決于正極材料煅燒過程中的化學不均一性,但它尚未被闡明。
成果簡介
近日,首爾國立大學Jongwoo Lim教授,利用一系列先進的同步x射線、質譜顯微鏡和結構分析等表征工具,揭示了溫度依賴的反應動力學、固體鋰源的擴散率和環境氧控制了煅燒粒子中反應中間體的局部化學成分。此外,還發現過渡金屬還原能力的變化決定了納米尺度上的局部結構。通過成像分析研究其反應機理,為調節煅燒化學和開發高能量密度鋰離子電池提供了有價值的信息。
研究亮點
固態煅燒過程中成分演化的復雜性可以用固態反應映射來全面解釋;
描述了Ni、Co和Mn在不同溫度下的反應動力學機制以及中間相的形成與演變;
為設計和理解鋰離子電池中的各種固態反應開辟新的途徑。
圖文導讀
[重量損失和氣體演化過程]
作者首先用熱重質譜法(TGA-MS)測定了煅燒過程的重量損失和氣體演化,結果如圖1所示,兩個主要的減重區域在200 - 400 ℃和400 - 870 ℃的溫度范圍內,這分別對應于水和二氧化碳的釋放,這是由于Ni0.6Co0.2Mn0.2(OH)2和Li2CO3分解。為了更好地了解溫度的影響,作者對在室溫(RT)、300 ℃、400 ℃、600 ℃、870 ℃、完全煅燒(FC)的樣品進行原位分析,確定中間相的化學成分。
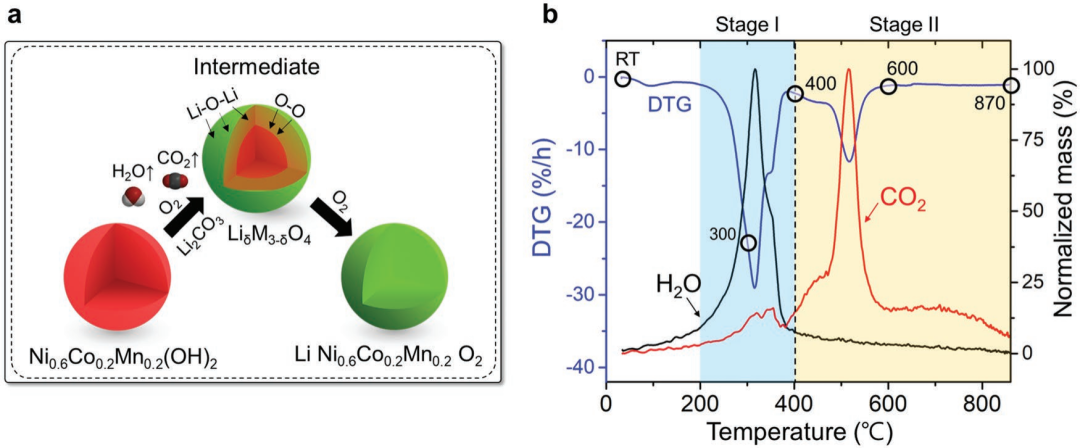
圖1. 煅燒過程產物的分析:a 固態合成過程中化學成分演化的示意圖;b DTG質譜曲線
[反應中間相的化學成像]
作者通過納米二次離子質譜(nano-SIMS)和同步加速器的透射X射線顯微鏡(TXM),觀察了粒子內鋰和氧的分布以及過渡金屬(TM)的氧化態變化,如圖2所示。在300 ℃,靠近樣品表面的氧分布密度明顯高于顆粒內部,表明環境氧從表面開始擴散,表面的Ni、Co和Mn分別被氧化到+3、+3和+4價,由X射線衍射儀(XRD)和擴展X射線吸收精細結構譜(EXAFS)確定了三者的化學成分分別對應于Co3+OOH、Ni3+OOH和Mn4+O2,如圖3所示,反應方程式如(1,2)。
在沒有與環境氧反應的情況下,內部區域存在巖鹽相,這是由于Ni(OH)2自發厭氧分解,形成NiO并釋放H2O。這也是300 ℃樣品的氧分布密度低于RT樣品的原因。此外,作者還計算了各金屬離子的平均氧化態,如圖2 c所示,對比發現,Ni的反應速率較Co和Mn慢。
M(OH)2 + ? O2 (in air) → M3+OOH + ? H2O [M = Ni / Co](1)
M(OH)2 + ? O2 (in air) → M4+O2 + H2O [M = Mn](2)
在400 ℃,氧和鋰分布有明顯差異,在一定半徑的殼內存在均勻的氧濃度和明顯的非均勻鋰濃度(圖2 a)。這是因為環境氧均勻擴散,而鋰的插入從固相表面點接觸開始。部分Li2CO3分解為CO2和Li2O,Li2O與表面的氫氧化鎳(Ni3+OOH)反應形成層狀氧化物(LiNi3+O2),反應方程式如(3,4)。此時的Ni3+和Mn4+殼結構域厚度增加到3 - 4 μm(圖2 a),這表明Ni和Mn氧化從表面逐漸擴散到顆粒內部。
有趣的是,在400 ℃,Co在粒子被均勻地還原為Co2.3+(圖2 e),這是由于Co3+OOH的熱分解產生了Co3O4(尖晶石,占據了八面體位)和Co2+(占據了四面體位),反應方程式如(5)。
Li2CO3 → Li2O + CO2(3)
NiOOH + ? Li2O → LiNiO2 + ?H2O(4)
CoOOH → ? (Co2+Tetra)(Co3+Oct)2O4 + ?H2O + 1/12 O2(5)
在600 ℃,環境氧的加速摻入和傳輸導致Co3+和Mn4+在顆粒內均勻分布(圖2 a)。但是,氧的核殼幾何形狀并不是來自環境氧的傳輸,而是來源于Li2O的核殼分布。雖然固態氧(Li2O)可以使顆粒內的TM氧化態均質化,但顆粒內部仍然處于缺氧狀態,核心區域的Li2O數量不足,因此反應生成的Li(1-x)Ni0.62.3+Co0.23+Mn0.24+O(1.89-x/2)仍然是尖晶石狀層狀結構,如圖3(a)所示。
在870 ℃時,鋰的摻入幾乎完成,經過FC條件下延長退火后,鋰和氧的分布變得均勻。Ni的氧化態從Ni2.30+(600 ℃)逐漸增加到Ni2.60+(870 ℃),退火10.5 h后逐漸增加到Ni2.67+(FC),此時粒子的組成為LiNi0.62.67+Co0.23+Mn0.24+O2。
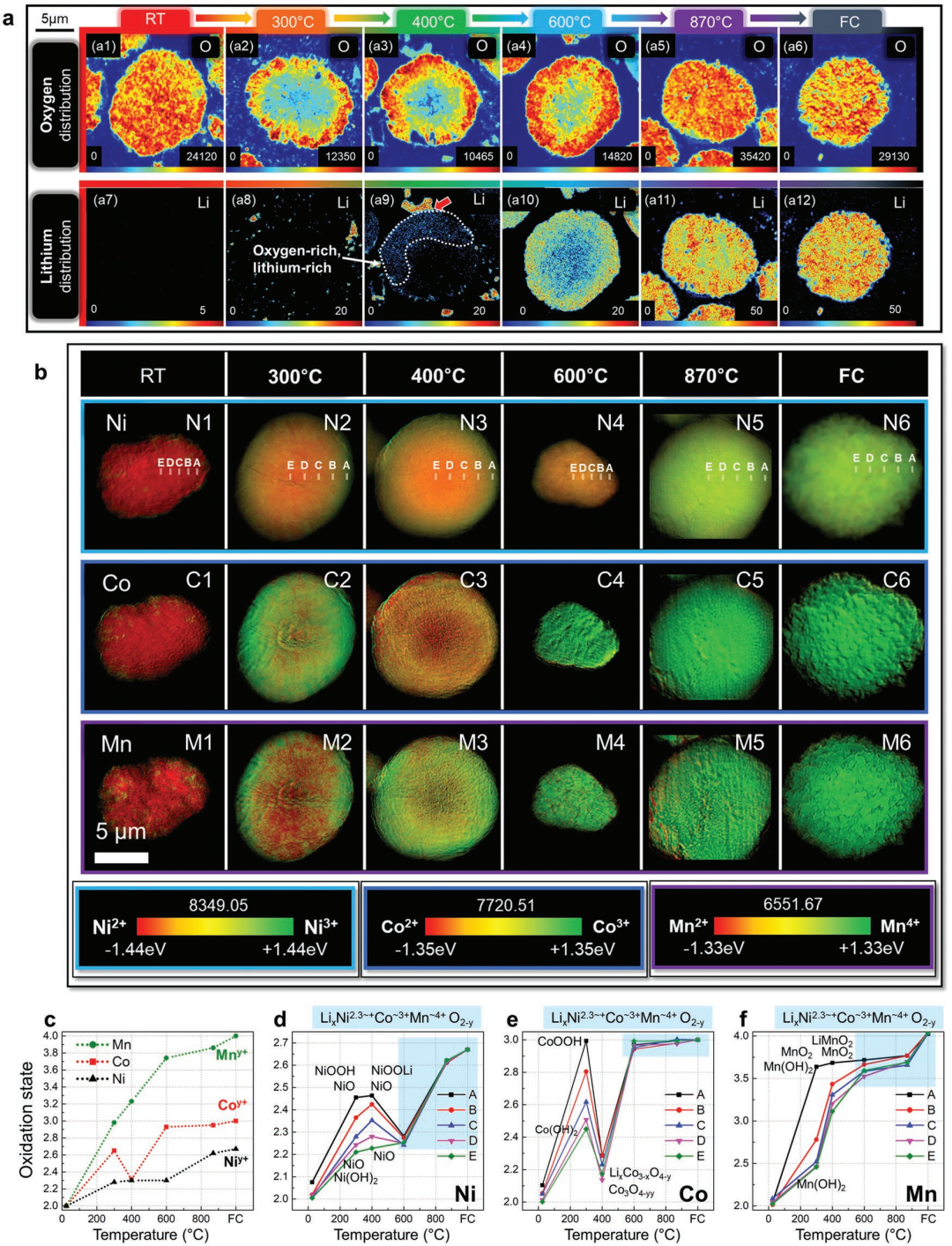
圖2. 納米SIMs和TXM的結果:a 在RT、300 ℃、400 ℃、600 ℃和870 ℃和FC條件下煅燒樣品的納米SIMs的O分布和Li分布;b 在不同煅燒條件下產生的中間粒子的彩色氧化圖(紅色表示還原狀態,綠色表示氧化狀態);c-f 根據TXM結果計算出的中間體、Ni、Co和Mn的平均氧化態
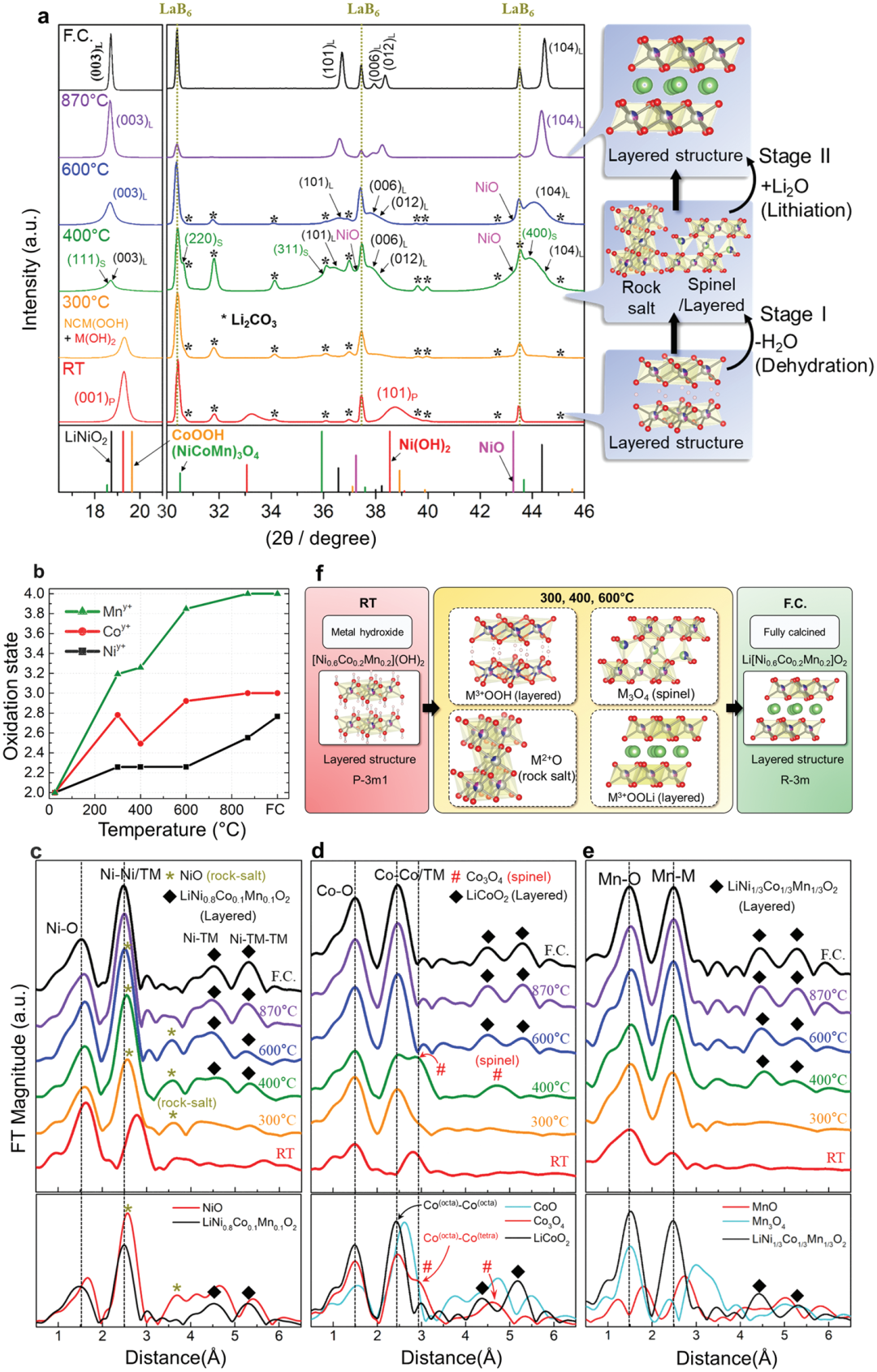
圖3. XRD和XAFS分析結果:a 在RT、300 ℃、400 ℃、600 ℃和870 ℃和FC條件下煅燒樣品的原位XRD圖和晶體結構模型;b Ni、Co和Mn k邊XANES光譜;c-e 中間樣品的Ni、Co和Mn的EXAFS光譜的傅里葉變換;f 合成過程中結構演化示意圖
[結構演化過程]
圖4描述了在不同溫度下的煅燒過程中表面和體相的局部原子構型的非均勻性,它主要源于環境氧和固態鋰源的輸運性質,以及溫度依賴的熱力學。當溫度從300 ℃增加到400 ℃時,由NiOOH、Co3O4和MnO2組成的表面相與鋰物質(Li2O)之間的反應促進了鋰層狀氧化物結構的生成,其中,鋰離子傾向于在LixNiO2-y, LixCo2O4-y, and LixMnO2-y中占據八、四和八面體位。
在600 ℃下,隨著Li2O和環境氧在表面的快速流入,使得樣品反應生成層狀氧化物Li(1-x)Ni0.62.3+Co0.23+Mn0.24+O(1.89-x/2)。雖然氧的傳輸被充分加速,但鋰源的擴散仍然緩慢,并導致鋰/氧的同心不均勻性。將溫度提高到870 ℃克服了擴散勢壘,使粒子內的鋰分布均勻化。通過附加退火,消除了鋰/氧缺乏和鋰過渡金屬無序。
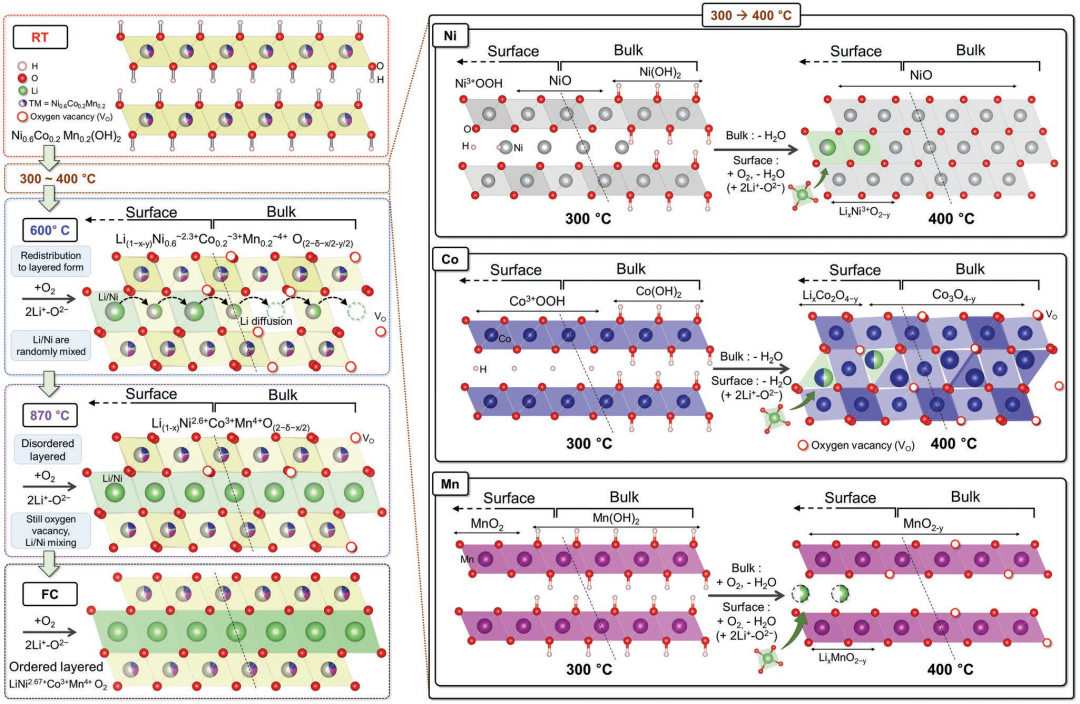
圖4. 在煅燒過程中環境氧和固態鋰源有限擴散引起的結構演化
根據在特定溫度下煅燒過程中粒子和元素特定原子構型的結果,作者提出了圖5所示的反應機制。表面的有氧分解,促進了MOOH(層狀)→LixTMO2(層狀)轉變,并促進了較低的溫度下Li2CO3→Li2O+CO2的分解過程。由于層狀MOOH和LixTMO2的鋰離子擴散速率很高,有利于Li2O摻入與擴散。
然而,樣品核心中巖鹽結構的NiO具有較低的鋰離子擴散速率,阻止了Li2O在低溫下的進一步摻入,延緩了整個煅燒過程。當溫度升高到600 ℃時,粒子內所有過渡金屬的均質氧化態表明固態氧擴散足夠快,但還需要更多的環境氧來完成進一步的氧化過程。
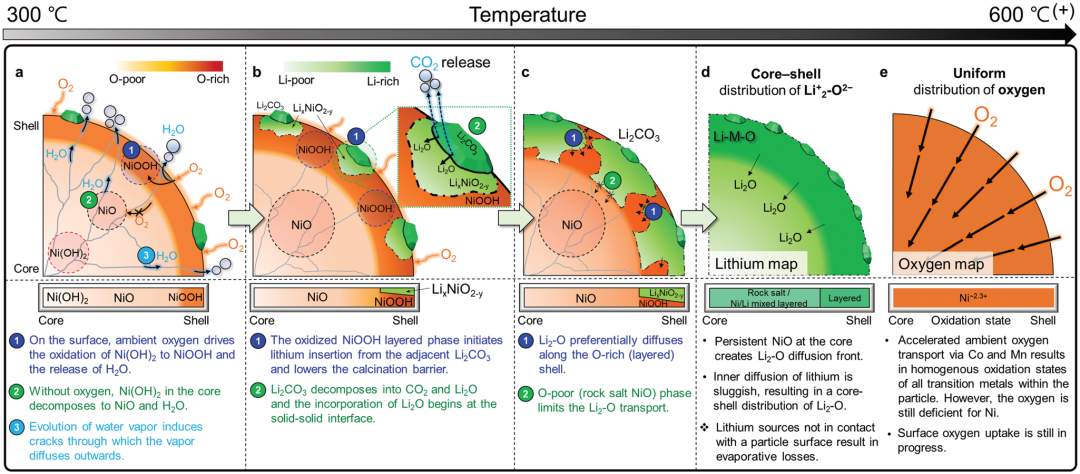
圖5. LiNi0.6Co0.2Mn0.2O2煅燒過程中的內部顆粒和元素特定的原子結構。
總結與展望
在鋰離子電池的背景下,作者提供了一個富鎳層狀氧化物正極的煅燒機理,包括前驅體的脫水過程,環境氧Li2O的插入過程,以及Li2CO3的熱分解過程。通過化學成像和同步加速器結構分析,闡明了15 μm粒子內的反應異質性。此外,明確地指出Ni、Co和Mn不同的氧化態將構成不同的物相結構,并描述了它們在不同溫度下的反應動力學機制。這項工作成功地證實了固態煅燒過程中成分演化的復雜性可以用固態反應映射來全面解釋,為設計和理解鋰離子電池中的各種固態反應開辟新的途徑。
審核編輯:劉清
-
鋰離子電池
+關注
關注
85文章
3215瀏覽量
77566 -
加速器
+關注
關注
2文章
795瀏覽量
37772 -
傅里葉變換
+關注
關注
6文章
438瀏覽量
42566 -
XRD
+關注
關注
0文章
131瀏覽量
9061 -
txm
+關注
關注
2文章
3瀏覽量
3147
原文標題:首爾國立大學Jongwoo Lim教授:鋰電正極煅燒過程中的固態反應異質性
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
實時原位監測光電催化過程中反應物濃度與熱效應的微光纖傳感器技術
固態電池的優缺點 固態電池與鋰電池比較
當升科技上半年固態電池正極材料出貨量突破數百噸大關
康謀分享 | 在基于場景的AD/ADAS驗證過程中,識別挑戰性場景!

3芯M16插頭運輸和安裝過程中的安全性如何





 鋰電正極煅燒過程中的固態反應異質性
鋰電正極煅燒過程中的固態反應異質性












評論