病變細胞的定位和細胞器功能的靶向調控可以促進病變修復。然而,常規調節難以到達深部病變和靶向線粒體。基于此,上海交通大學醫學院崔文國教授團隊采用動態螺旋鑲嵌技術構建螺旋鑲嵌微/納米水凝膠微球傳熱微針(ST針),利用分子鏈運動響應熱刺激來調節無取向三嵌段聚合物的粘附,作為熱能和生物因子的傳輸系統(圖1a)。ST針系統利用其物理特性,準確到達病灶深處,基于動態螺旋鑲嵌機制,去除水凝膠微球的鑲嵌狀態,釋放熱能和生物因子,治療骨關節炎(圖1b)。該體系實現了熱能與生物因子協同調節線粒體,從而抑制軟骨細胞凋亡(圖1c)。相關研究成果以“Localization of Lesion Cells and Targeted Mitochondria Via Embedded Hydrogel Microsphere using Heat Transfer Microneedles”為題發表在Adv. Funct. Mater.期刊上。
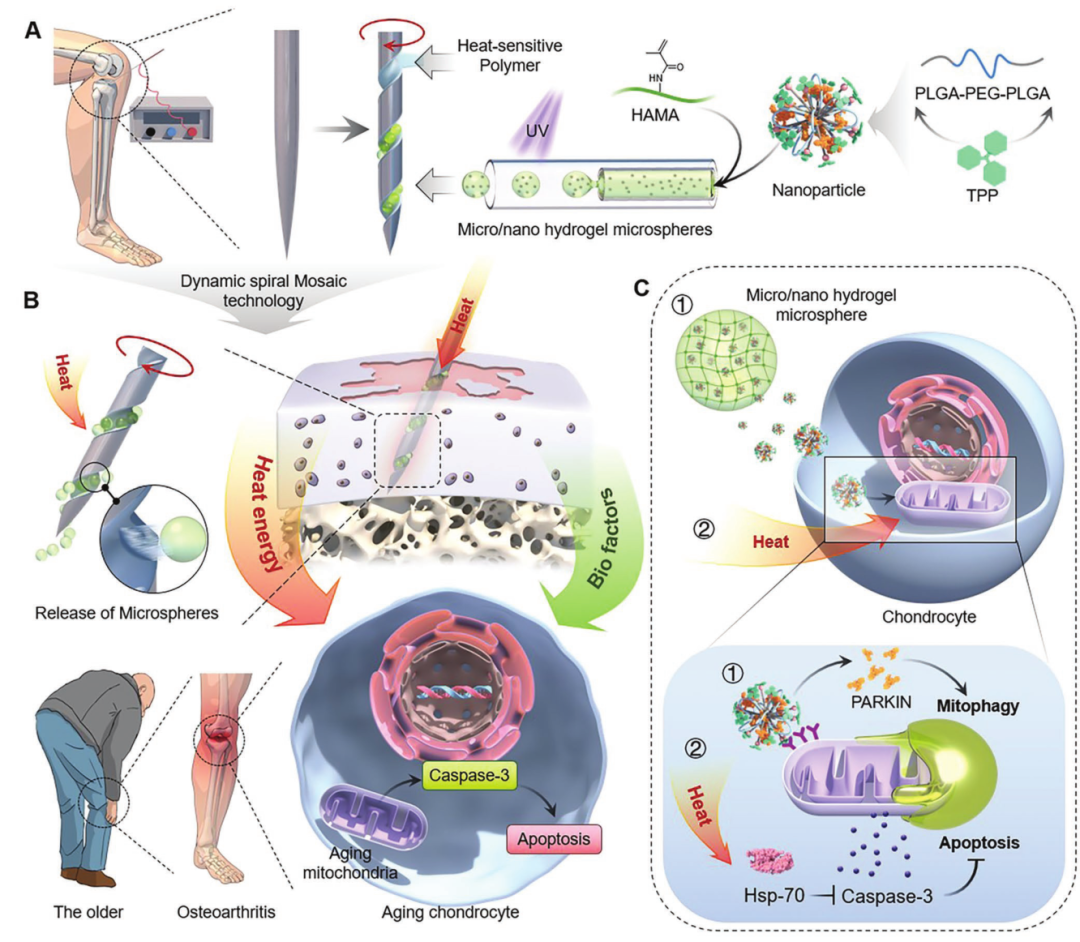
圖1 傳輸熱能和生物因子的ST針系統示意圖
微針將熱能傳輸至深部病變
中國針灸微針(CA針)是中醫最成熟的傳熱工具,被廣泛用于治療各種疾病,如手腕(圖2Ai)、腰部(圖2Aii)、和肩膀(圖2Aiii)疼痛。在該研究中,研究人員選擇CA針的尾部(C點)和尖端(D點)來確定溫度。艾草柱燃燒后,C點的溫度從≈26.5℃升高到≈37.5℃(總升高≈9℃),隨后達到熱平衡,溫度不再進一步升高(圖2C)。隨后,隨著熱量從C點轉移到D點(圖2D),在D點觀察到從基本溫度升高到28.2℃(總增加≈1.7℃)。實驗在室溫(25℃)下進行;因此,針頭散發的熱量相對較大,導致尖端溫度降低。
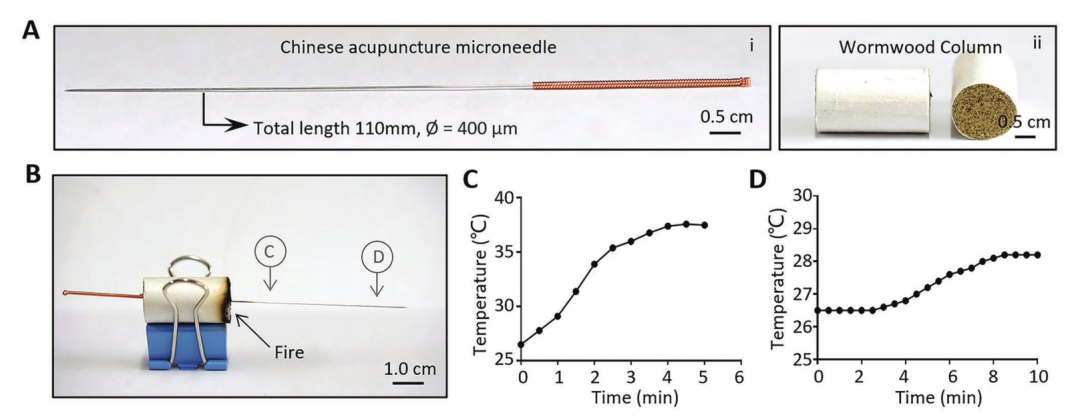
圖2 使用CA針的傳統傳熱的特點
熱敏粘合劑聚合物及微/納米水凝膠微球的合成與表征
隨后研究人員合成了熱敏粘合劑聚合物(圖3A),然后對其流變曲線、儲能模量和損耗模量曲線、不同溫度下的流動性進行了一系列表征(圖3B-E)。
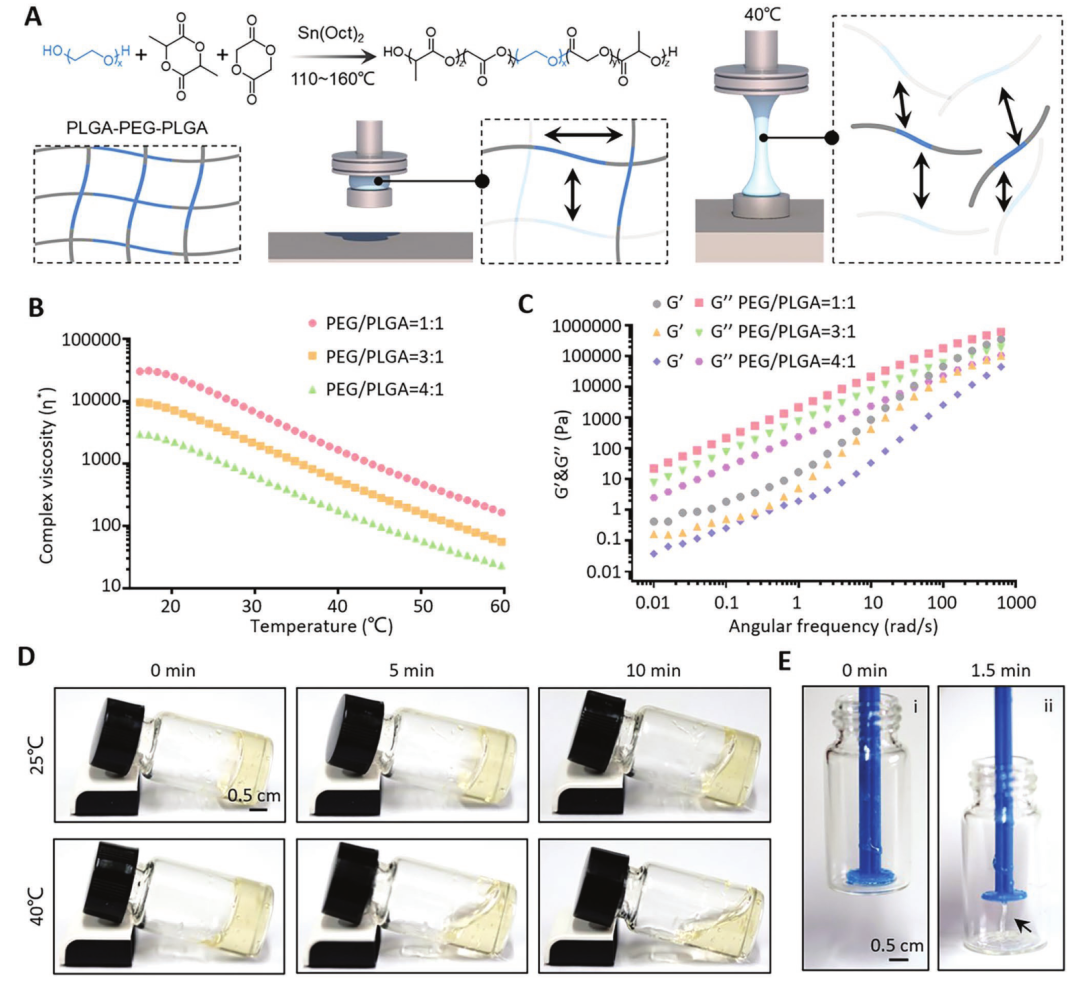
圖3 熱敏粘合劑聚合物的特性
隨后研究人員合成了以線粒體為靶點的微/納米微球(圖4A)。對其進行TEM、粒徑分布、Zeta電位、光電子顯微鏡、尺寸分布、SEM等一系列表征(圖4B-H)。
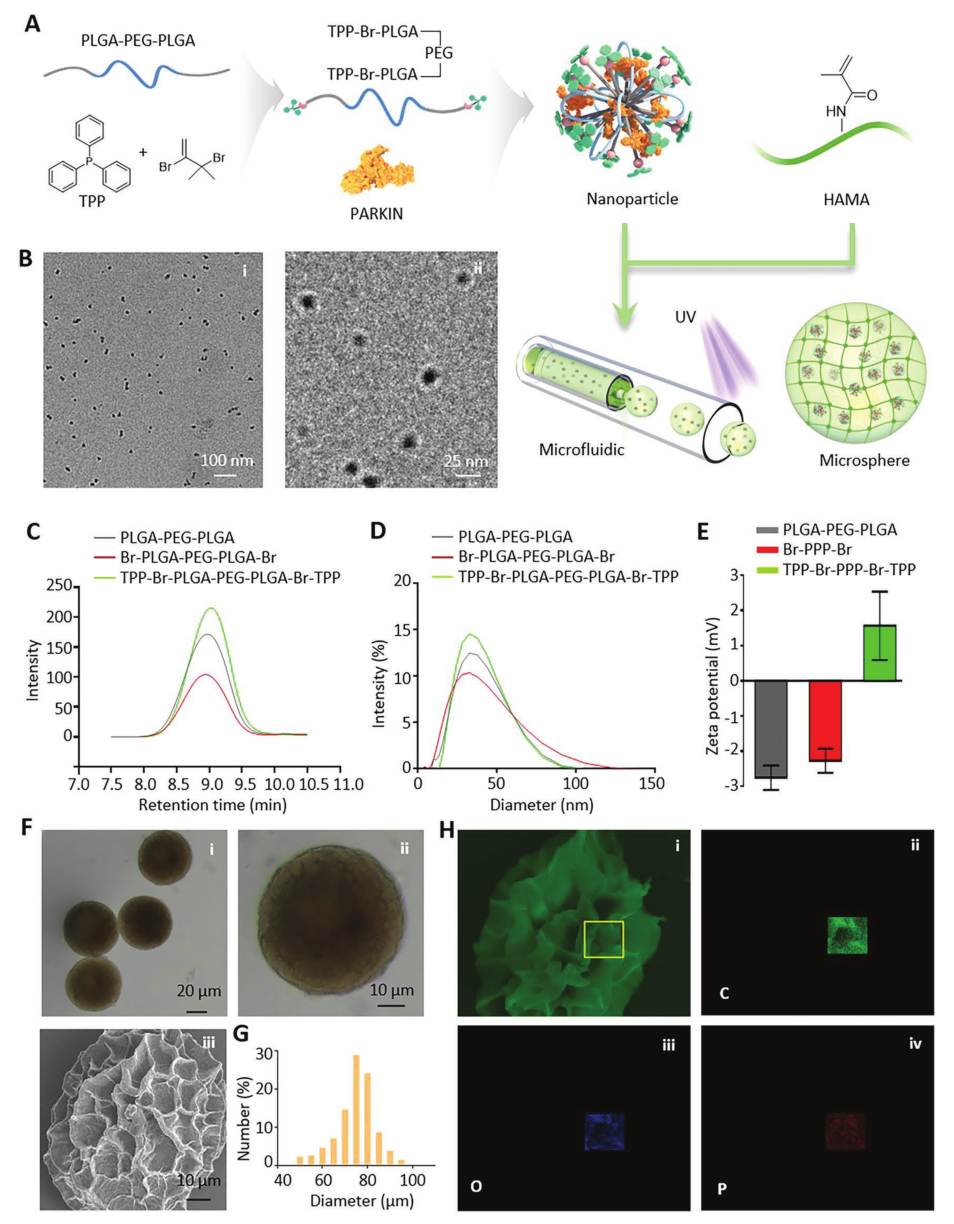
圖4 靶向線粒體的微/納米微球的表征
螺旋鑲嵌水凝膠微球CA針的構建,以及傳輸熱能和水凝膠微球的能力
為了提高CA針加載水凝膠微球的能力,在針尖(ST針)上構建了螺紋槽結構,并與傳統的CA針進行了比較(圖5A)。利用熱敏聚合物的粘合特性,將水凝膠微球粘貼在CA針上并嵌入到ST針上。通過旋轉ST針釋放水凝膠微球,并允許水凝膠微球留在病變部位以實現長期治療(圖5B)。隨后,通過模擬兔子的臨床治療,驗證了ST針系統傳輸熱量的能力。溫度檢測器探頭放置在皮膚上ST針的入口處,而尖端位于組織內(圖5C)。兩個溫度之間的關系符合一階函數:Y = 0.9356X ? 4.078(圖5D)。這些發現表明ST針具有良好的導熱性,可以將熱量傳輸到更深的病灶。將載有熒光染料的水凝膠微球嵌入ST針中,以驗證ST針系統可以傳輸水凝膠微球。ST針系統傳輸水凝膠微球的效率可以通過測量治療前后ST針和穿刺部位的熒光強度來評估。結果表明,在熱敏粘合劑聚合物和螺紋槽的保護作用下,ST針系統可以成功地將水凝膠微球傳輸到體內(圖5F)。因此,ST針系統可以將水凝膠微球傳輸到組織中,并在熱刺激下釋放,并留置在病灶中。
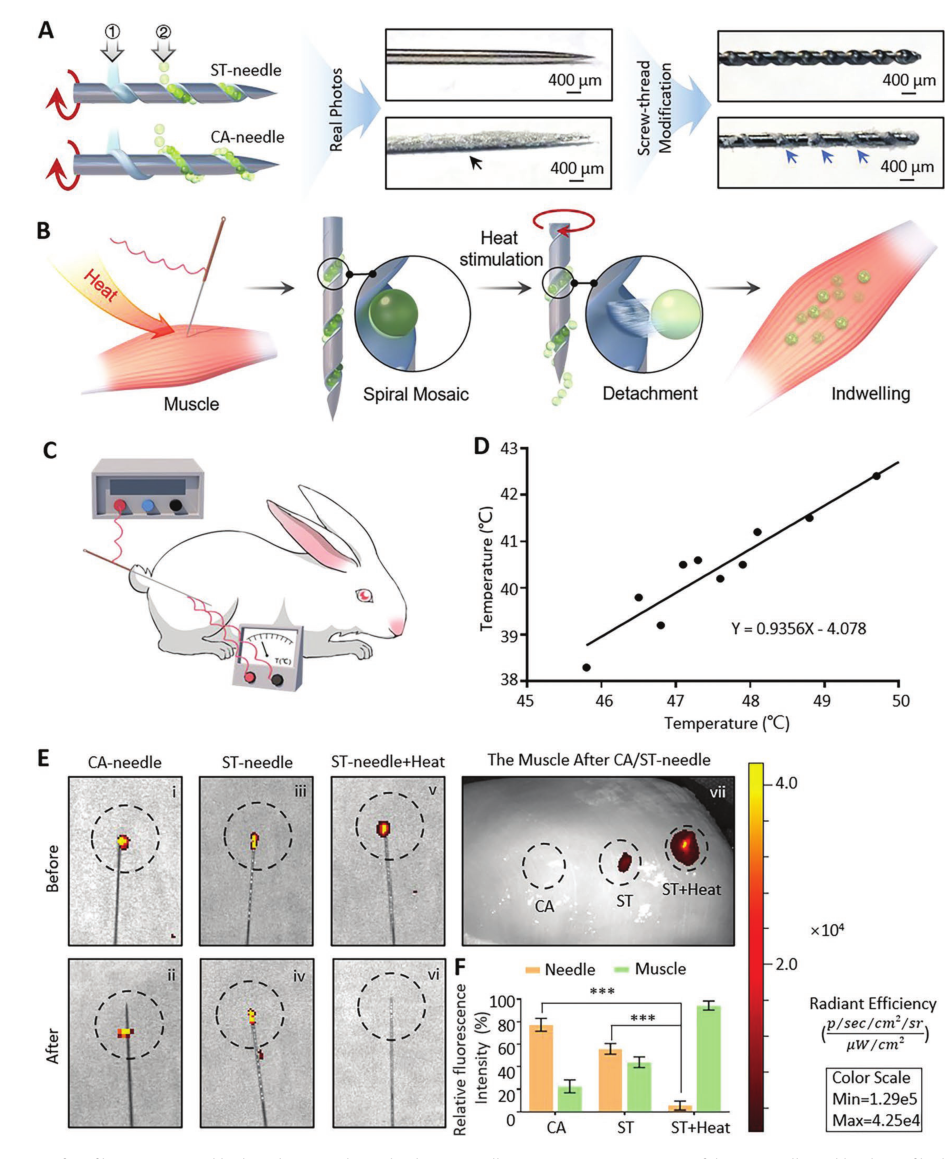
圖5 通過ST針系統傳輸熱能和水凝膠微球
熱傳輸ST針在骨關節炎治療中的應用
使用ST針治療骨關節炎(OA)時,必須穿過軟骨基質的致密屏障才能到達深部軟骨病變的軟骨細胞。然后,軟骨細胞通過釋放熱能和生物因子進行調節(圖6A)。因此,為驗證ST針能否穿過軟骨基質的物理屏障,高效傳輸水凝膠微球,進行了兔膝關節軟骨模擬穿刺實驗(圖6B),結果表明CA針無法將水凝膠微球傳輸到軟骨基質深處的病變處,ST針可以。為了證明ST針系統可以將熱量傳輸到軟骨,研究人員對未經處理的軟骨樣本進行了熱成像(圖6C)。實驗結果表明,熱療部位的溫度顯著升高≈4.5℃。隨后,利用兔軟骨進行的熒光殘留實驗表明,CA針上殘留熒光的比例明顯高于ST針(圖6D),表明ST針能夠成功突破軟骨的物理屏障,并將水凝膠微球傳輸到軟骨中(圖6E)。
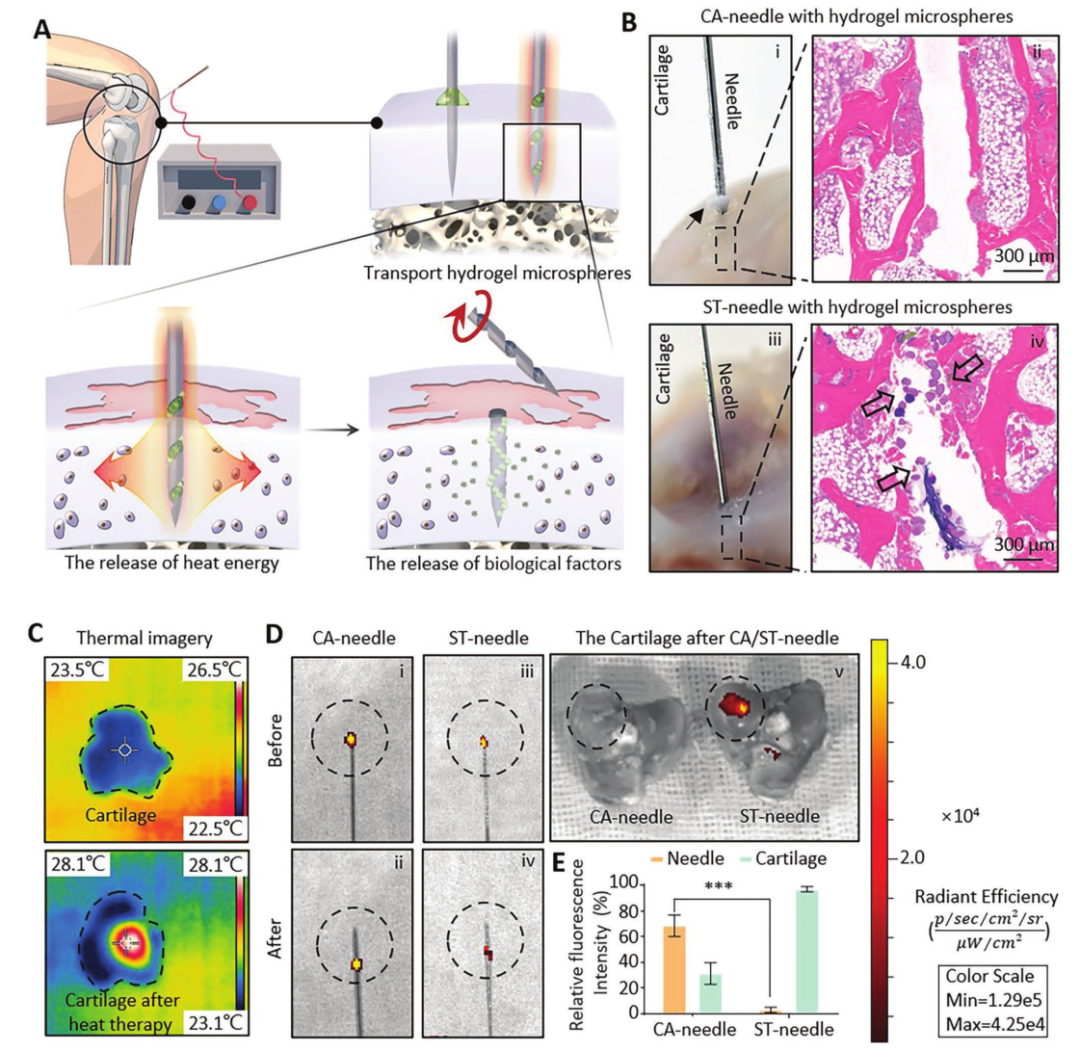
圖6ST針系統在骨關節炎治療中的應用
使用ST針系統靶向調節軟骨細胞線粒體的機制
ST針作為熱能和生物因子的雙重傳輸系統,能夠通過熱能快速抑制線粒體凋亡,通過水凝膠微球釋放生物因子誘導線粒體自噬,從而實現協同靶向調控線粒體功能和抑制軟骨細胞細胞凋亡(圖7)。ST針釋放的熱能刺激軟骨細胞,促進HSP-70的分泌。然而,HSP-70可以抑制caspase-3分泌和線粒體凋亡。ST針系統釋放的水凝膠微球保留在病灶內并繼續釋放納米粒子。在TPP結構的引導下,納米粒子進入軟骨細胞并靶向線粒體。此外,促進線粒體自噬的PARIN因子被釋放,老化的線粒體被清除。
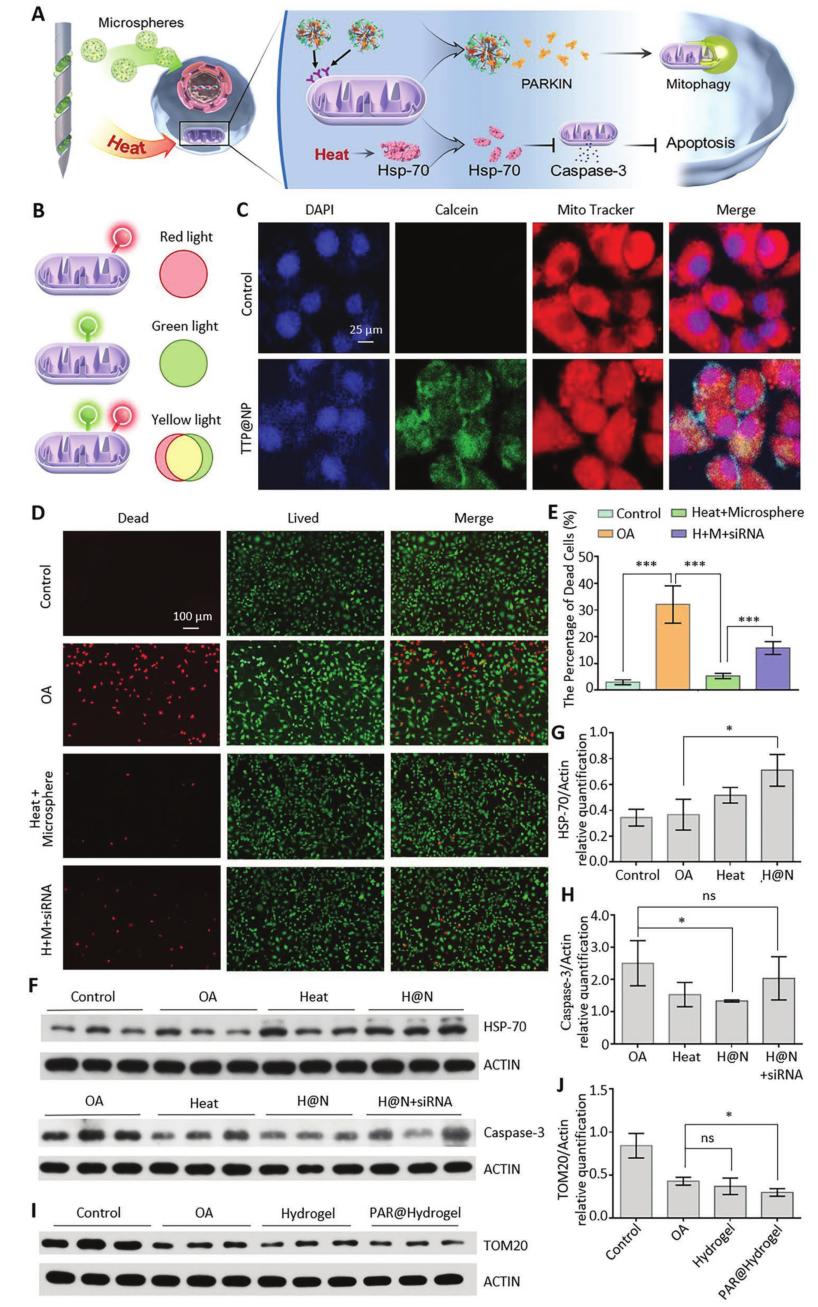
圖7 熱能和微/納米水凝膠微球共調節的分子機制
ST針系統可顯著改善軟骨細胞功能并治療OA
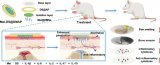
隨后,開發了OA大鼠模型以驗證ST針系統治療OA的療效(圖8)。組織學染色結果表明,通過ST針調節線粒體可顯著改善軟骨細胞的生命周期,從而有效治療骨關節炎。
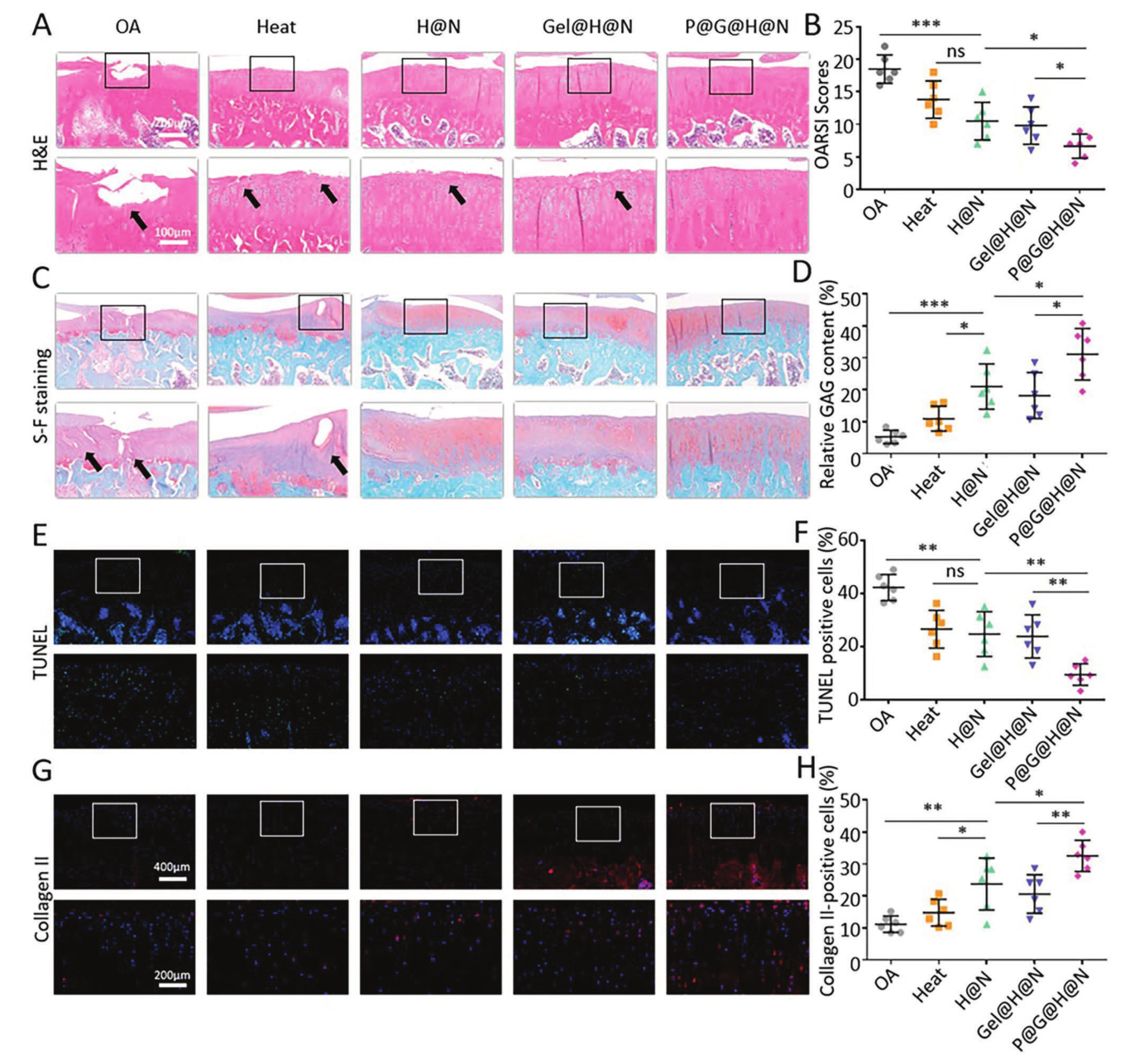
圖8使用ST針系統治療骨關節炎的動物實驗
綜上,在這項研究中,創新性地使用動態螺旋鑲嵌技術開發了具有螺旋鑲嵌微/納米水凝膠微球的傳熱微針作為熱能和生物因子的雙重傳輸系統,利用分子鏈運動響應熱刺激調節無取向三嵌段聚合物的粘合力。ST針系統利用其優異的物理特性,準確到達病灶深處,將熱量傳輸給病灶細胞。熱量激活ST針系統的動態螺旋鑲嵌機制,去除水凝膠微球的鑲嵌狀態,實現熱量和水凝膠微球同時到達病灶。通過熱能快速抑制線粒體凋亡和釋放生物因子的水凝膠微球誘導長期線粒體自噬,實現了熱能和生物因子對線粒體功能的協同靶向調控。OA大鼠模型進一步驗證了ST針系統能夠抑制軟骨細胞凋亡,促進軟骨損傷修復,從而緩解OA。這項研究的結果對未來生物材料的設計和各種疾病治療策略的規劃具有重要意義。
論文鏈接
https://doi.org/10.1002/adfm.202212730
審核編輯 :李倩
-
水凝膠
+關注
關注
0文章
26瀏覽量
9113 -
微針技術
+關注
關注
2文章
74瀏覽量
8692
原文標題:鑲嵌水凝膠微球的傳熱微針,用于骨關節炎治療
文章出處:【微信號:Micro-Fluidics,微信公眾號:微流控】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
初創公司:正在使用深度學習來更有效、更經濟地診斷膝關節
治療關節炎新技術:生物3D打印組織
國產機器人完成輔助關節置換手術 機器人的精度是傳統手術無法企及的
科學家新發明3D成像技術,將有助于關節炎的護理
科學家研發可分泌抗炎藥的智能軟骨
微電機更好地治療類風濕性關節炎
PharmaTher研發水凝膠微針貼劑,用于治療神經類疾病
直線模組3D打印脊柱助力X形腿變直
微流控技術中使用的不同類型的水凝膠
超聲波驅動的微針貼片,用于細菌感染痤瘡的高效治療
iPhone和Apple Watch助醫生診斷類風濕性關節炎
基于顏色變化水凝膠的集成微流控壓力傳感





 鑲嵌水凝膠微球的傳熱微針,用于骨關節炎治療
鑲嵌水凝膠微球的傳熱微針,用于骨關節炎治療











評論