磁珠的構成
一般磁珠由三層構成,最里面是聚苯乙烯,外面包裹一層磁性物質四氧化三鐵,最外面再包一層官能基團修飾的高分子材料,上面偶聯不同的官能團。不同功能的磁珠,偶聯的官能團不同,純化核酸用的一般是羧基(-COOH)。
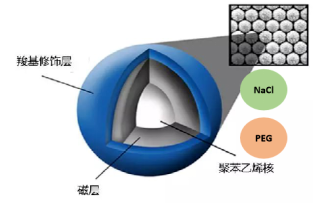
磁珠結構示意圖
當然不僅磁珠應用在核酸制備上,在化學發光、細胞分選、蛋白純化等應用磁珠依然是大顯身手,是因為不同的官能基團,或者偶聯其他,如蛋白抗體等。
磁珠吸附DNA的原理
NGS上用的最多還是貝克曼的XP磁珠。這種羧化磁珠比羥基磁珠產量更高,非特異性結合更少。(Solid-phase reversible immobilization,SPRI):
(1)反應體系中,較高濃度的 PEG 和 NaCl 導致 DNA 分子水化層脫去,DNA膠體熱力學穩定性破壞,構象也隨之改變,DNA分子發生聚集沉淀,帶負電荷的磷酸基團大量暴漏在外面;
(2)帶電荷的磷酸基團通過 Na^+^與羧基形成“離子橋”,使得 DNA 被特異吸附到帶羧基的磁珠表面。(該過程是可逆的,在適當條件下,結合的 DNA 分子可以被洗脫回收)


DNA吸附原理圖
純化磁珠進行 “片段分選” 的原理
磁珠雙選很大程度依賴于PEG:PEG作為一種分子擁擠試劑,達到一定的濃度時,奪取了一定的水,溶液環境變化,會使較大DNA的結構變緊湊,發生坍塌性的轉變而凝聚。不同長度的DNA構象穩定性不同,在遵循熱力學規律的情況下,溶液環境與分子擁擠試劑的濃度有很大的關系。即在特定的溶液中,當PEG濃度達到某一臨界值時,就會發現一定大小以上的DNA分子構象非連續的發生凝聚。
(1) DNA越長 :表面裸露出來帶負電的磷酸基團越多,整條分子帶的負電就更強,更容易吸附到磁珠,只需要較低濃度的PEG和NaCl,就可以回收(需要加入的磁珠體積更小)。
(2) DNA越短 :就需要更高濃度的PEG和NaCl,將其表面的水化層破壞得更徹底,裸露出來足夠多帶負電的磷酸基團,才能被磁珠吸附住,從而回收回來(需要加入的磁珠體積更大)。
 磁珠純化圖
磁珠純化圖
此外,體系中的PEG還可以增加溶液的粘稠度,讓磁珠保持懸浮不容易沉聚,在DNA binding過程中更充分與DNA接觸,同時PEG也不易造成蛋白變性和非特異性吸附。但是PEG的DNA沉聚效果容易收到pH、溫度等的影響,溫度過低PEG也不易與水完全互溶,所以磁珠一般都要求室溫平衡后再用,其儲存buffer里也會加一些低濃度的pH穩定劑,如Tris-HCl等。
酒精清洗及DNA洗脫
酒精清洗 :第一,DNA在這個濃度的酒精里溶解度很低;第二,DNA這個時候是聚集狀態,磁珠剛好提供一個聚集的奇點,讓DNA沉聚在其周圍,所以絕大部分DNA不會掉下來。但酒精濃度很重要,一般都要求新鮮配制。濃度太低,鹽離子可以清洗得更干凈,但是體系中過多的水會將部分DNA從磁珠上溶解下來,造成DNA損失,DNA的回收率可能會收到影響。濃度越高,體系中水越少,清洗鹽離子的能力減弱,可能會使鹽離子清洗不干凈,但DNA的溶解度小,回收率高;
DNA洗脫 :酒精清理后,先需要晾干磁珠上殘留的酒精,以防影響下游實驗。(注意晾干時磁珠表面無光澤即可,過度干燥,體系失水過多,會導致磁珠DNA進一步聚集,最終DNA很難回溶到水中,影響回收率)晾干后加入水或者TE buffer,這時體系中已經沒有鈉離子和PEG,無法形成電橋結構,帶負電的DNA和磁珠之間相排斥,水重新包裹DNA形成水化層,使其從磁珠上洗脫下來,溶解到溶液中。
-
磁珠
+關注
關注
6文章
266瀏覽量
44144 -
DNA
+關注
關注
0文章
243瀏覽量
30983 -
PEG
+關注
關注
0文章
4瀏覽量
6575
發布評論請先 登錄
相關推薦
磁珠簡介
什么是生物磁珠_磁珠法提取DNA簡介
什么是磁珠,磁珠法核酸提取儀的優點是什么
什么是磁珠?用途有哪些?
鐵氧體磁珠的作用 鐵氧體磁珠的選型方法
貼片磁珠的構成元素





 磁珠的構成、吸附DNA的原理
磁珠的構成、吸附DNA的原理










評論