應用背景
1970年,Bockris在《Mordern Electrochemistry》一書中把電化學定義為:研究帶電界面的現象的科學,及研究電子導體和離子導體界面現象的科學。利用第一性原理計算探究界面反應機理,是目前廣泛應用的研究手段之一。
在電化學界面反應過程中,由于電化學反應界面通常與恒定電極電勢的外電極相連,為確保電子的化學勢與外電極的電勢達到平衡,即電子的巨正則系綜(grand canonical ensemble),實際體系中會存在電子的流入與流出過程。傳統的第一性原理計算通常是在正則系綜下,即在電荷守恒的條件下展開的,因此它并不能很好的描述電化學界面反應,下文中我們將在電荷守恒的條件下展開的計算模型稱為恒電荷模型(constant charge model,CCM)。
因恒電荷模型并不適于處理電化學界面問題,我們可采用在電子巨正則系綜下展開第一性原理計算,這種計算方法又被稱為固定電勢方法(fixed potential method/constant potential method)。在下文中我們將利用固定電勢計算的模型稱為恒電勢模型(constant potential model,CPM)。
后文提供了使用DS-PAW計算電催化氮還原反應(Electrocatalytic nitrogen reduction reaction, eNRR)過程中反應能計算的詳細教程。
案例概覽
本文展示了如何使用DS-PAW模擬一個電催化還原氮氣反應。該反應以碳基負載過渡金屬Ru單原子為催化劑,使用DS-PAW對電催化 N2分子的吸附及還原過程進行模擬。在計算過程中使用了CCM_vacuum,CCM_water,CPM_water三種不同的模型,本文詳細介紹了在不同模型下如何設置參數及計算反應能。
N2分子的吸附及還原過程進行模擬。在計算過程中使用了CCM_vacuum,CCM_water,CPM_water三種不同的模型,本文詳細介紹了在不同模型下如何設置參數及計算反應能。
更多關于DS-PAW的使用細節,請移步DS-PAW手冊查看。
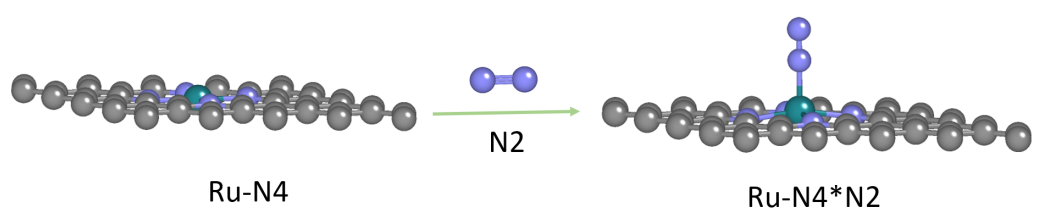
圖1. 吸附過程示意圖
計算流程
DS-PAW模擬的反應為 N2 分子在碳基負載Ru單原子上的吸附過程,反應的表達式可簡寫作:(Ru ? N4 ) + N2 = (Ru? N4 ? N2 )
第一步:搭建模型
模型包括:(a) 碳基負載Ru原子模型(Ru ? N4) ,(b) N2單分子模型,(c) 吸附了 N2 分子的碳基負載Ru原子模型(Ru? N4 ? N2)
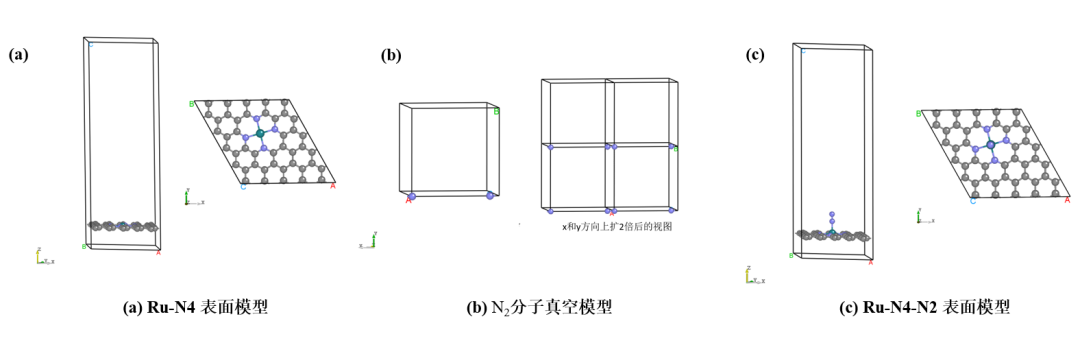
圖2.計算模型圖
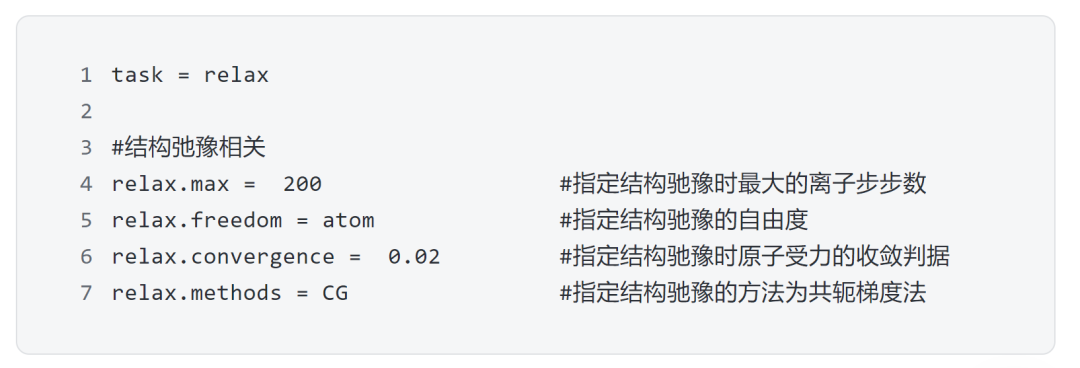
第二步:結構弛豫
對搭建的結構進行結構弛豫,獲得穩定結構,在DS-PAW中進行結構弛豫需要的核心參數:
第三步:能量計算
在不同模型條件下進行能量計算,獲得穩定構型對應能量,下面按不同模型分別進行介紹:
CCM_vacuum
常規的真空層下的scf計算,即可獲得CCM_vacuum模型下的能量,下面列出了在DS-PAW中進行單點能計算需要設置的核心參數:

CCM_water
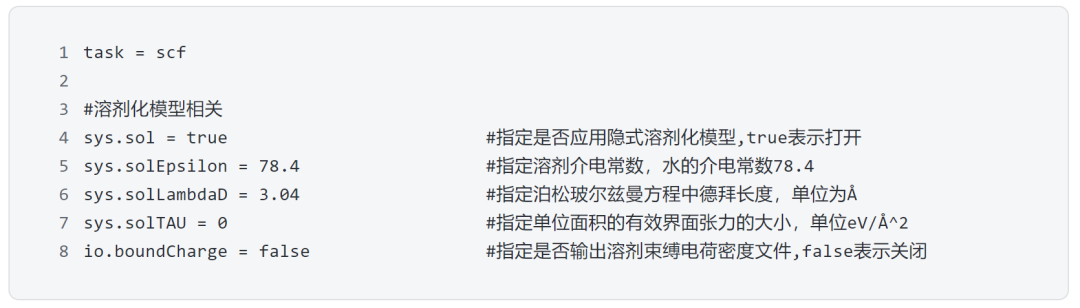
在CCM模型下,也可以利用隱式溶劑化模型來考慮溶劑效應,這里我們以水溶液為例,列出利用DS-PAW在scf計算中引入溶劑化模型所需要設置的核心參數:
CPM_water
在DS-PAW中用固定電勢方法計算即可獲得CPM模型下的能量。在新發布的2023A版本中進行固定電勢計算必須引入溶劑化模型,這里列出了利用DS-PAW在隱式水溶液環境下進行固定電勢計算的核心參數:

第四步:反應能計算
本文選取了3個不同的計算模型,首先介紹各模型下的吸附反應式:
CCM_vacuum:
該模型下,吸附反應式可寫作:
(Ru-N4)+N2 (ideal gas)=(Ru-N4-N2)
我們定義ΔE為反應能,反應能的計算表達式為:
ΔE=E0(Ru-N4-N2)-E0(Ru-N4)-E0(N2)
其中,E0對應真空模型下體系的總能((sigma→0),該數值可從自洽計算所得的scf.h5(或system.json)文件中獲取,查找關鍵字 “TotalEnergy0” 即可。
CCM_water:
該模型下,吸附反應式可寫作:
(Ru-N4)(in water)+N2 (ideal gas)=(Ru-N4-N2) (in water)
ΔE=E0(Ru-N4-N2)-E0(Ru-N4)-E0(N2)
其中,E0對應水溶液浸潤的模型下體系的總能((sigma→0),該數值可從自洽計算所得的scf.h5(或system.json)文件中獲取,查找關鍵字 “TotalEnergy0” 即可。
CPM_water 該模型下模擬的反應過程為氣相中的N2在由水溶液浸潤并與0V vs. SHE(標準氫電極)電極接觸的催化劑表面的吸附過程,此時吸附反應式有兩種寫法,為便于描述,我們定義了以下物理量符號:
ne0 : 中性體系下的核電荷數
ne : 當體系電壓為設定值(sys.fixedPPotential所設數值,此例對應 0 V)時體系的總電子數
dne : 當體系電壓為設定值時,體系的帶電量:dne = ne ? ne0
μe : 體系電子化學勢,電勢零點為溶液深處(即DFT計算得到的電荷密度最低點的電勢值)
Δe : 吸附態體系價電子數(eAB)與吸附基底和吸附分子總價電子數(eA+eB)的差值
Ω0 : grand total energy(sigma→0): 電子巨正則系綜下的體系總能,其表達式為:Ω0 = E0 ? dne ? μe
此時,CPM_water模型下吸附反應式可參考如下寫法:
方法一、在反應式中考慮 Δe ,吸附反應式可寫作:
Ru-N4 (0V vs. SHE) + N2(ideal gas) = Ru-N4-N2 (0V vs. SHE) - Δe
ΔE = E0(Ru-N4-N2) ? Δe * μe ? E0(Ru-N4) ? E0(N2)
其中,E0的數值可從自洽計算所得的 scf.h5(或system.json)文件中獲取,查找關鍵字 “TotalEnergy0” 即可。
ne 和 μe 的數值可從自洽計算所得的 DS-PAW.log (或 scf.h5 或 system.json)文件中獲取,最后一個LOOP下查找關鍵字 “Electron” 和 “Chemical Potential(electron) ” 即可。
方法二、考慮電子巨正則系綜下的體系總能 Ω0
由于固定電勢計算是模擬的電子的巨正則系綜,此時反應能計算式中的體系總能 E0 應當用Ω0 來代 替。吸附反應式可寫作:
(Ru-N4) (0V vs. SHE) + N2(ideal gas) = (Ru-N4-N2) (0V vs. SHE)
ΔE = Ω0 (Ru-N4-N2) ? Ω0 (Ru-N4) ? Ω0 (N2)
其中,Ω0 的數值可從自洽計算所得的DS-PAW.log (或 scf.h5 或 system.json)文件中獲取,最后一個LOOP下查找關鍵字 “Grand Total Energy” 即可。
由于(Ru-N4)與(Ru-N4-N2)的電勢為0V vs. SHE,故對(Ru-N4)與(Ru-N4-N2)進行0V下的固定電勢計算,從DS-PAW的相應輸出文件提取數據,得到如下表格,能量單位為 eV:
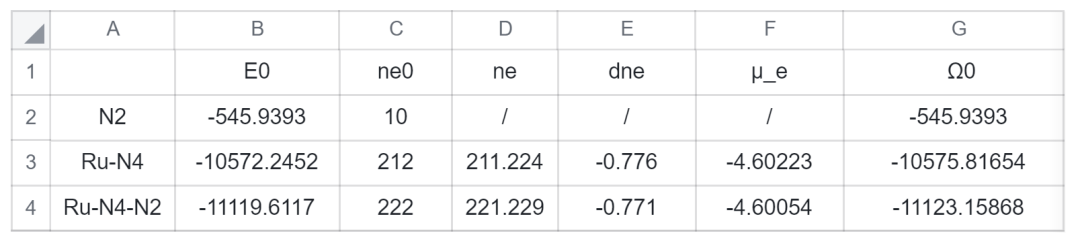
表 1. CPM_water模型下固定電勢計算數據
接下來將表1的數據代入對應的表達式中進行計算:
方法一、在反應式中考慮 Δe ,反應能計算過程如下:
Ru-N4 (0V vs. SHE) + N2(ideal gas) = Ru-N4-N2 (0V vs. SHE) - Δe
ΔE = E0(Ru-N4-N2) ? Δe * μe ? E0(Ru-N4) ? E0(N2)
= ? 11119.6117 ? (221.229 ? 211.224 ? 10) × ( ? 4.600) ? ( ? 10572.2452) ? ( ? 545.9393)
= ? 1.4042 eV
方法二、考慮電子巨正則系綜下的體系總能 Ω0 ,反應能計算過程如下:
(Ru-N4) (0V vs. SHE) + N2(ideal gas) = (Ru-N4-N2) (0V vs. SHE)
ΔE = Ω0 (Ru-N4-N2) ? Ω0 (Ru-N4) ? Ω0 (N2)
= ? 11123.1586 ? ( ? 10575.8165) ? ( ? 545.9393)
= ? 1.4027 eV
通過兩種方法計算所得的吸附能一致。可見?DS-PAW中定義的Ω0即可很方便的計算固定電勢下的反應能。
結果展示
將表1的數據分別代入CCM_vacuum、CCM_water、CPM_water模型的吸附反應式,計算三個模型下,eNRR前三步反應的反應能,結果如下表2所示:
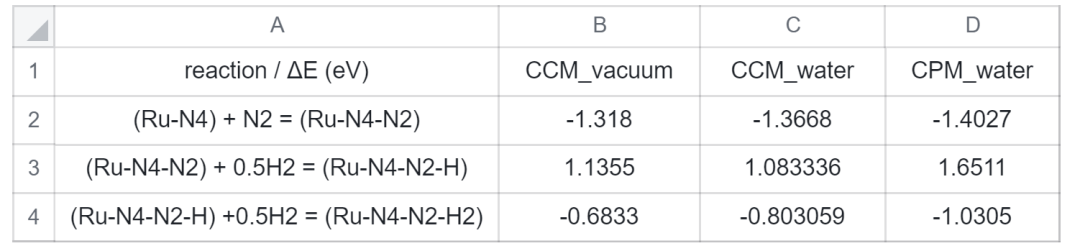
表 2. 反應能數據表
最后將上述結果繪制成反應坐標曲線,效果如下圖3所示:
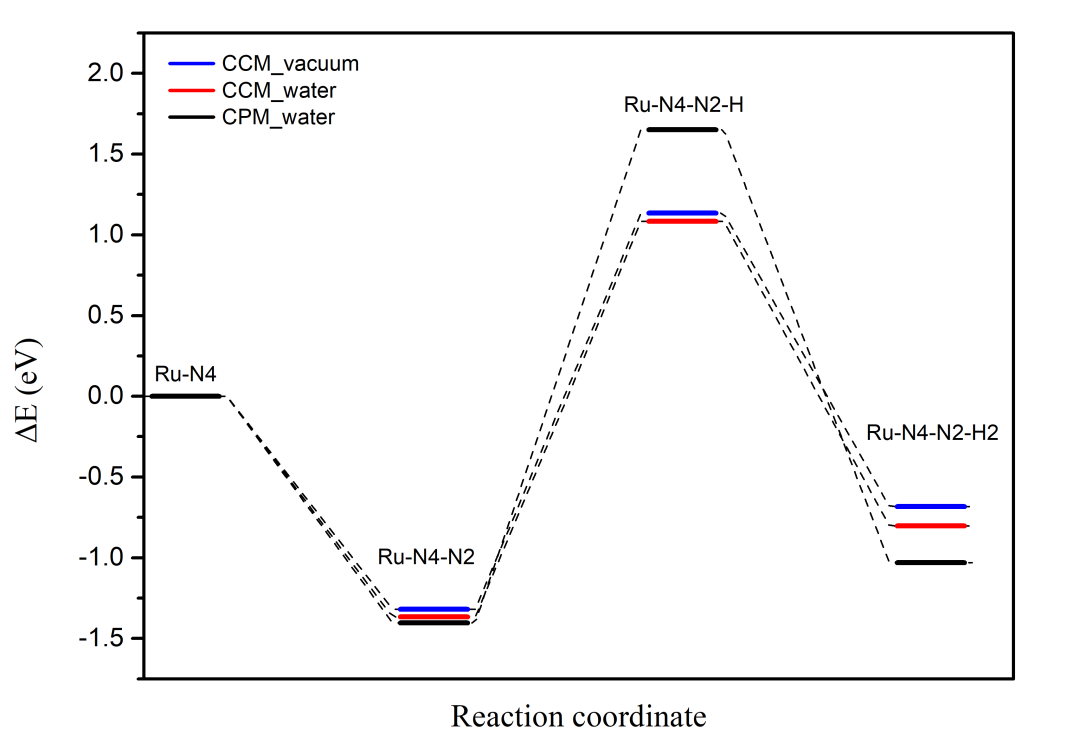
圖 3. 反應坐標-反應能曲線
審核編輯:劉清
-
CPM
+關注
關注
0文章
12瀏覽量
7695
原文標題:DS-PAW應用案例丨固定電勢在電化學反應中的應用
文章出處:【微信號:hzwtech,微信公眾號:鴻之微】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦




 固定電勢在電化學反應中的應用
固定電勢在電化學反應中的應用










評論