循環(huán)腫瘤細(xì)胞(CTC,CirculatingTumor Cell)是存在于外周血中的各類腫瘤細(xì)胞的統(tǒng)稱,因自發(fā)或診療操作從實(shí)體腫瘤病灶(原發(fā)灶、轉(zhuǎn)移灶)脫落,大部分CTC在進(jìn)入外周血后發(fā)生凋亡或被吞噬,少數(shù)能夠逃逸并發(fā)展成為轉(zhuǎn)移灶,增加惡性腫瘤患者死亡風(fēng)險(xiǎn)。
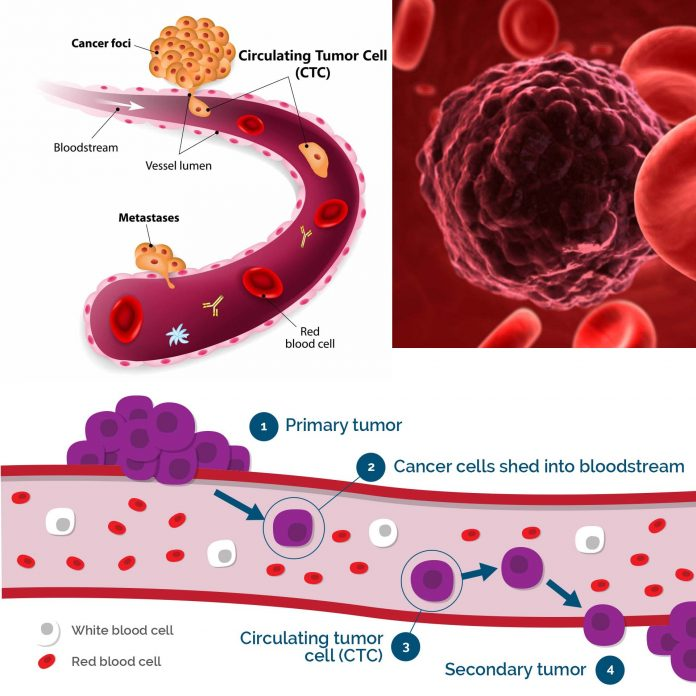
原發(fā)腫瘤細(xì)胞脫落或轉(zhuǎn)移進(jìn)入血液,形成循環(huán)腫瘤細(xì)胞
因此CTC的檢測(cè)具有重要的預(yù)后和治療意義,但由于其數(shù)量可能非常少,因此不容易檢測(cè)到這些細(xì)胞。據(jù)估計(jì),在已經(jīng)脫離原發(fā)腫瘤的細(xì)胞中,只有0.01%能夠形成轉(zhuǎn)移。
在轉(zhuǎn)移性癌癥患者中,循環(huán)腫瘤細(xì)胞的頻率約為每毫升全血1-10個(gè)CTC,而相比之下,一毫升血液中含有幾百萬(wàn)白細(xì)胞和十億紅細(xì)胞。這種低頻率導(dǎo)致識(shí)別癌細(xì)胞十分困難,這意味著理解CTC生物學(xué)特性的關(guān)鍵一步是富集、純化、分離每毫升血液中極少量CTC的技術(shù)和方法。
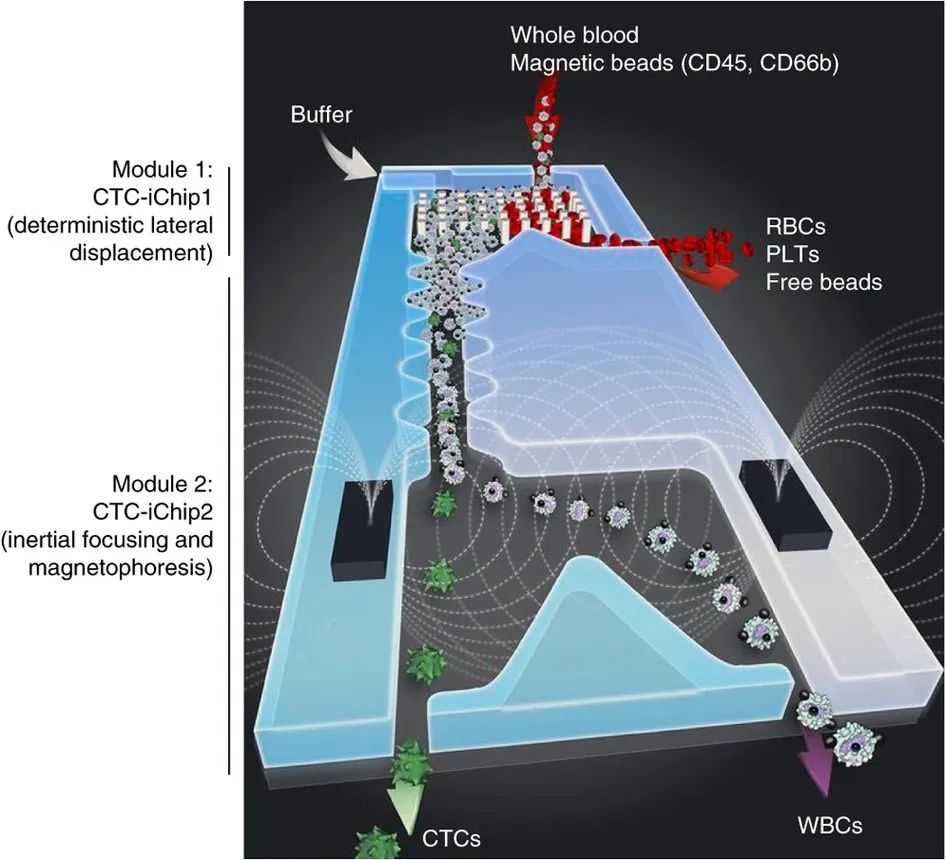
微流控芯片利用慣性和磁力從血液中分離出循環(huán)腫瘤細(xì)胞
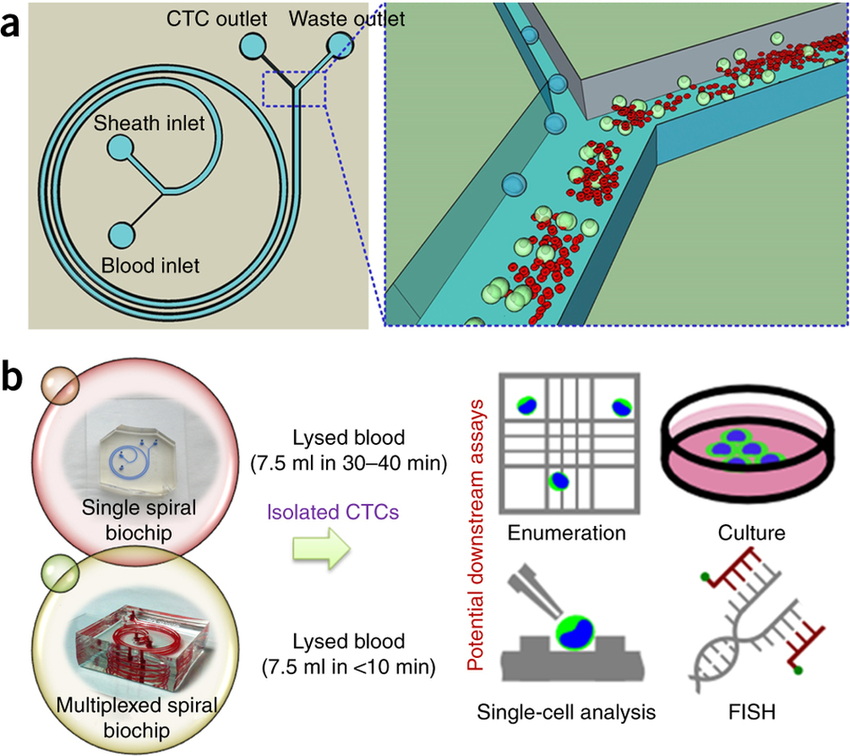
微流控芯片利用慣性從血液中分離出循環(huán)腫瘤細(xì)胞
為克服這一困難,來(lái)自杭州電子科技大學(xué)的科研團(tuán)隊(duì)結(jié)合高精度3D打印和軟光刻技術(shù)制造了多層微流控芯片,可用于超高通量富集和分離血液中的循環(huán)腫瘤細(xì)胞,同時(shí)能夠降低終端流速,便于后續(xù)實(shí)時(shí)阻抗和光學(xué)檢測(cè),未來(lái)有望推動(dòng)早期癌癥的血液篩查。

用于從血液中分離循環(huán)腫瘤細(xì)胞(CTC)的三層微流控芯片
基于慣性的循環(huán)腫瘤細(xì)胞收集
研究人員提出了一種用于循環(huán)腫瘤細(xì)胞(CTC)收集和下游分析的3D堆疊多層慣性微流控分選芯片。該芯片頂部使用梯形螺旋通道分離CTC和血紅細(xì)胞,然后中間和底部使用兩級(jí)方形蛇形通道進(jìn)一步去除RBC并純化目標(biāo)樣品溶液。
通過(guò)整合螺旋通道和蛇形通道降低流速,可以在通道收集出口處應(yīng)用各種檢測(cè)方法,例如阻抗檢測(cè)和成像。因此,多級(jí)分揀芯片可以實(shí)現(xiàn)高流量輸入和低流量輸出,滿足醫(yī)療診斷對(duì)吞吐量和檢測(cè)的要求。
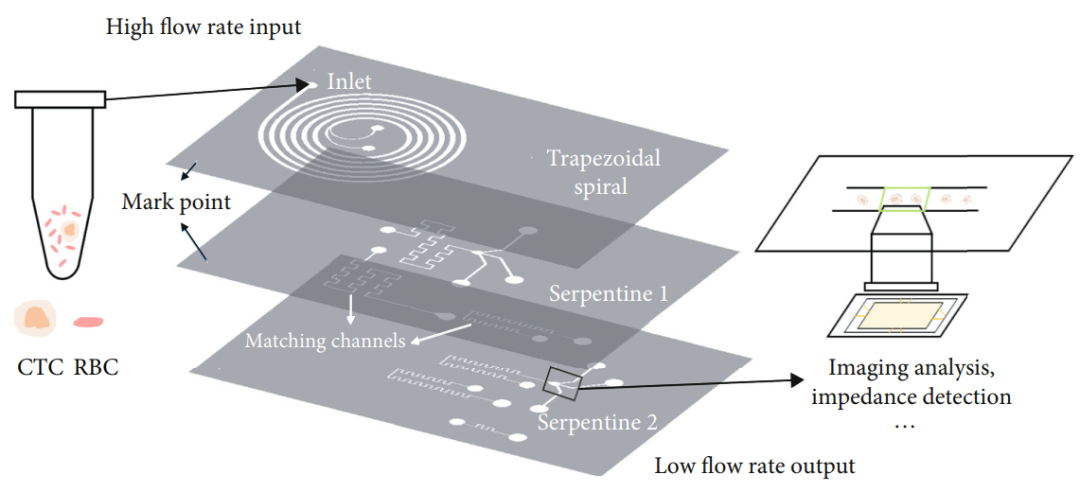
基于三層微流控芯片分離CTC用于后續(xù)醫(yī)學(xué)檢測(cè)
此外,由聚二甲基硅氧烷(PDMS)鑄造的3D堆疊結(jié)構(gòu)減少了芯片面積(2cm×3cm),并具有良好的多層觀察透明度。性能方面,該3D微流控芯片能夠以1.3 mL/min的高流速?gòu)拇罅縍BC背景細(xì)胞中分離SW480(人結(jié)腸癌細(xì)胞)、A549(人肺腺癌細(xì)胞)和Caki-1(人腎透明細(xì)胞癌細(xì)胞),分離效率>80%,分離純度>90%,濃度倍數(shù)約為20。
這項(xiàng)工作旨在提供一種可以用于快速醫(yī)學(xué)診斷的檢測(cè)方法集成的樣品處理方法。
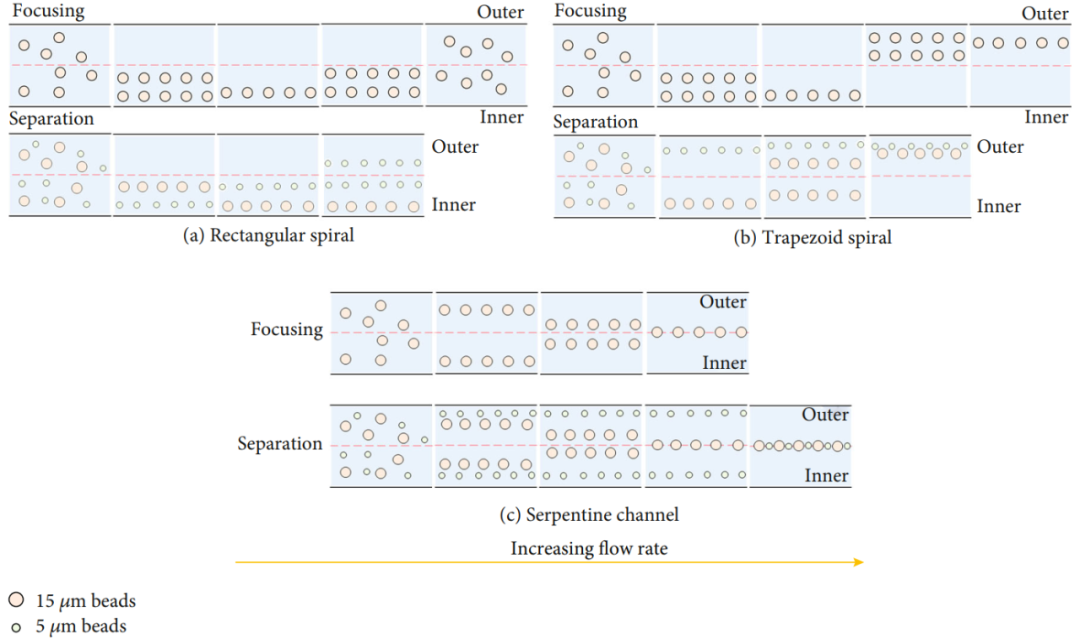
螺旋和蛇形通道分離不同尺寸顆粒的原理和示意圖
微流控芯片設(shè)計(jì)、制造及參數(shù)優(yōu)化
該3D堆疊多級(jí)慣性微流體細(xì)胞分選芯片集成了梯形螺旋通道和兩個(gè)方形蛇形通道。梯形螺旋通道具有一個(gè)入口和兩個(gè)出口,是芯片的第一級(jí)。在梯形螺旋通道中,流速相對(duì)較高,紅細(xì)胞將集中在外壁附近,而CTC將集中在內(nèi)壁附近,進(jìn)而實(shí)現(xiàn)CTC與紅細(xì)胞的分離。不同層的通道按照液體流動(dòng)方向從上到下排列,整個(gè)芯片只有一個(gè)入口,無(wú)需額外輸入鞘流。
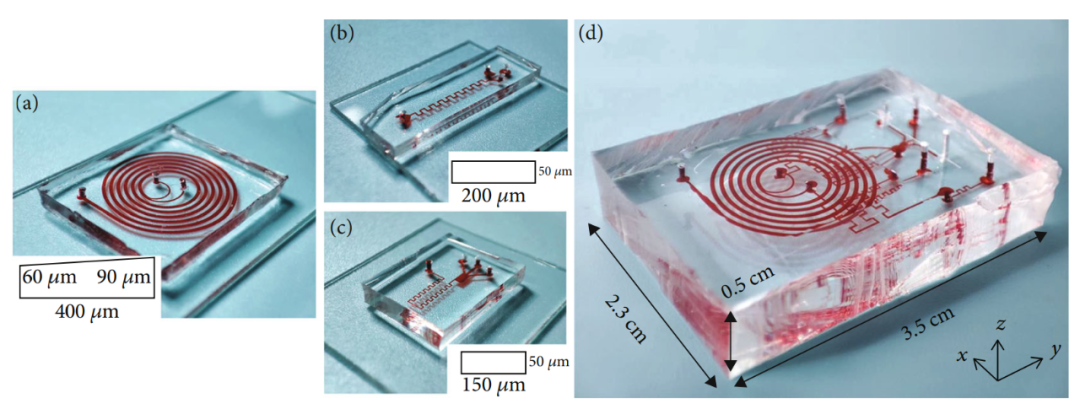
多層微流控芯片。(a)(b)(c)分別為第一、第二和第三層。(d)三層疊加。
此外,為了確保通道的所有階段都能在最佳工作狀態(tài)下工作,還設(shè)計(jì)了匹配通道以匹配流動(dòng)阻力。在自動(dòng)多級(jí)去除紅細(xì)胞和目標(biāo)流的減速、聚集和濃縮后,流速?gòu)膍L/min降至μL/min,這使得與下游檢測(cè)和分析(如阻抗檢測(cè)和成像分析)更容易集成。
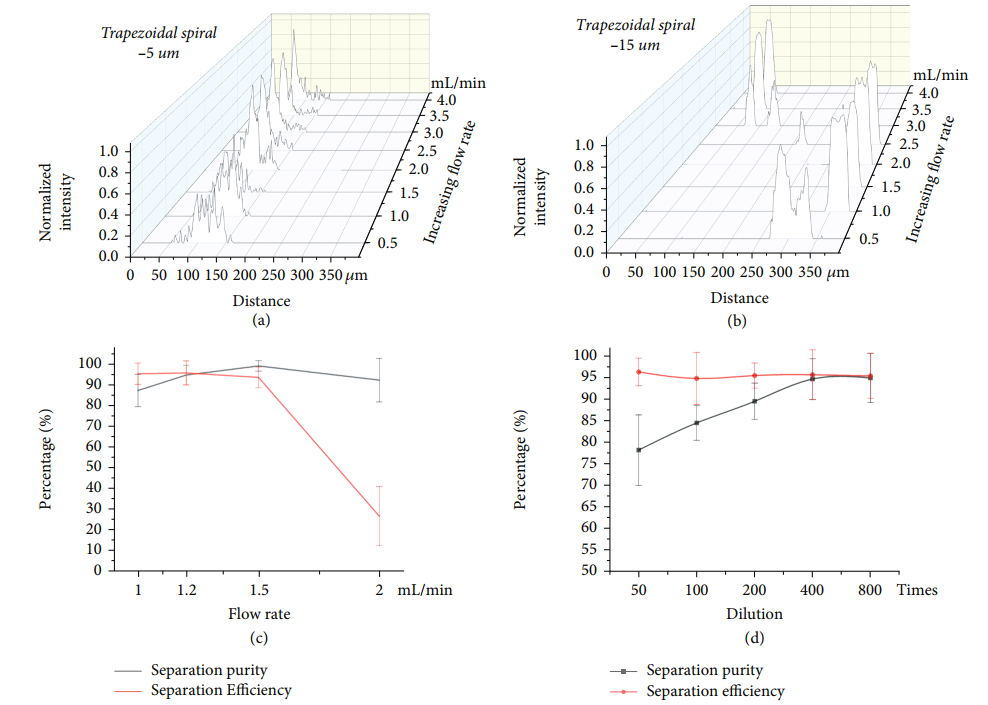
參數(shù)優(yōu)化過(guò)程
概念驗(yàn)證
概念驗(yàn)證實(shí)驗(yàn)可以通過(guò)分離兩種不同尺寸的聚苯乙烯微粒進(jìn)行。在只有一個(gè)單通道注射泵驅(qū)動(dòng)輸入樣品的情況下,光學(xué)顯微鏡可以捕獲通道每一級(jí)出口處的分選過(guò)程。在每次測(cè)試中,將10秒的視頻數(shù)據(jù)作為圖像疊加的原始數(shù)據(jù)。然后,通過(guò)ImageJ軟件對(duì)600張圖片的垂直疊加最小化,獲得粒子軌跡。
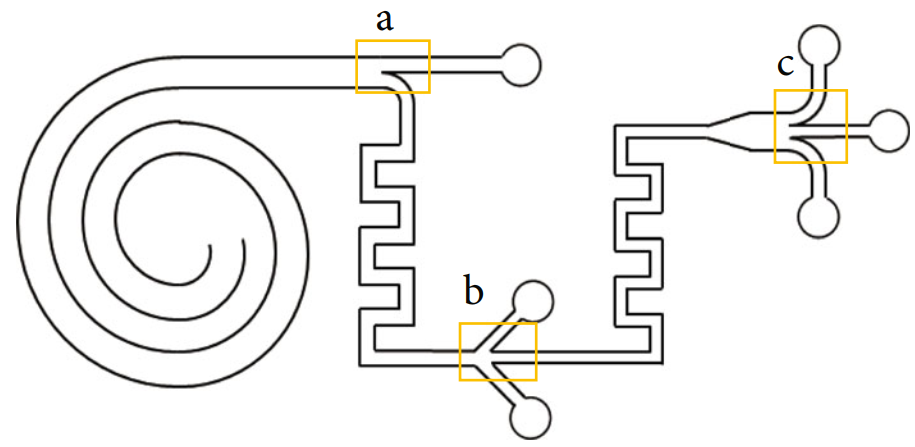
多級(jí)通道結(jié)構(gòu)圖

基于慣性實(shí)現(xiàn)不同尺寸微顆粒的篩選。較大顆粒會(huì)保持向前流動(dòng),但較小顆粒會(huì)被兩側(cè)支線分流
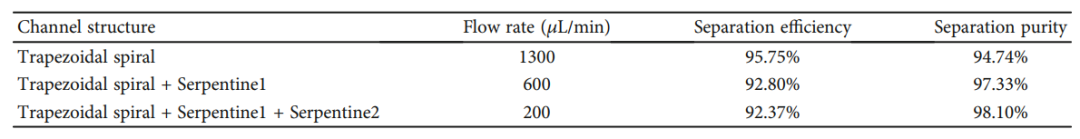
組合不同通道結(jié)構(gòu)的各級(jí)出口分離效果比較
腫瘤細(xì)胞實(shí)驗(yàn)
最后,研究者使用腫瘤細(xì)胞(SW480、A549和Caki-1)進(jìn)行了驗(yàn)證。通過(guò)使用概念驗(yàn)證實(shí)驗(yàn)中所得的最佳工作流速,將配置的血細(xì)胞與腫瘤細(xì)胞的混合液通入多級(jí)芯片結(jié)構(gòu),對(duì)收集口細(xì)胞情況進(jìn)行分析。結(jié)果表明,該3D堆疊芯片可以實(shí)現(xiàn)了從大量背景細(xì)胞中分離多種類型的腫瘤細(xì)胞,分離效率>80%,分離效率>90%。

該微流控芯片能有效分離血紅細(xì)胞(RBC)和循環(huán)腫瘤細(xì)胞(A549)
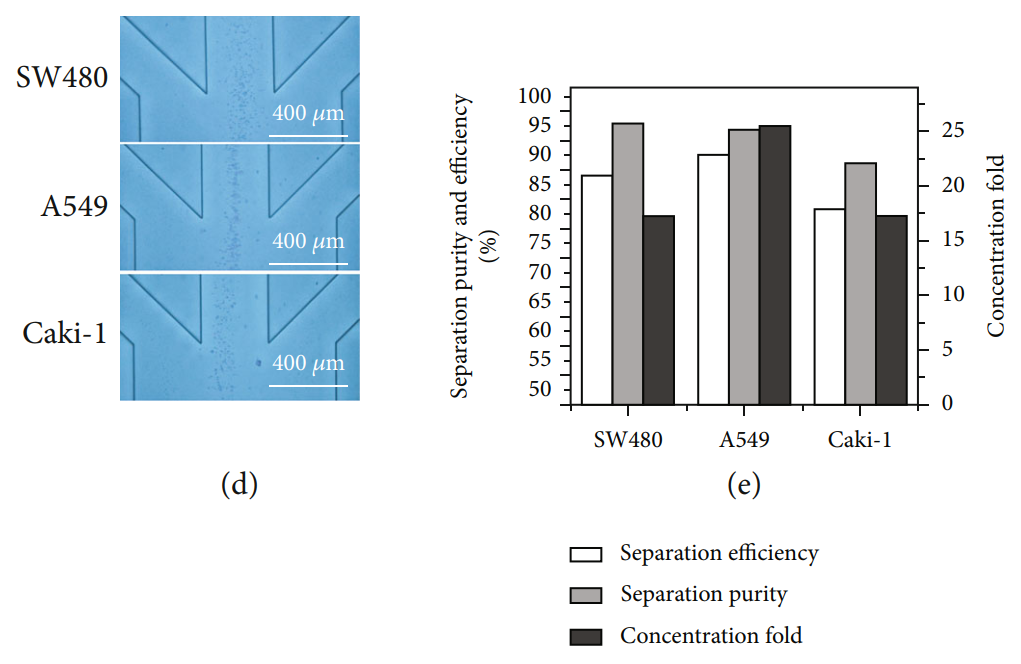
芯片用于CTC分選驗(yàn)證(a)紅細(xì)胞與A549的混合液 (b)廢液口(c)收集口(d)SW480、A549和Caki-1在最終出口的疊加軌跡(e)三種CTC的分離效率、分離純度和濃度倍數(shù)
未來(lái)與展望
CTC作為腫瘤發(fā)生遠(yuǎn)端轉(zhuǎn)移的關(guān)鍵環(huán)節(jié),是腫瘤液體活檢的主要材料之一,在腫瘤患者的預(yù)后判斷、療效預(yù)測(cè)、療效評(píng)價(jià)、復(fù)發(fā)轉(zhuǎn)移以及耐藥機(jī)制的研究中都具有重要的臨床意義。
3D堆疊多級(jí)微流控芯片設(shè)計(jì)克服了現(xiàn)有單級(jí)芯片中分離純度、分離效率和吞吐量之間的限制,通過(guò)多級(jí)流速降低可為下游檢測(cè)方法的集成提供一個(gè)有效的解決方案。
該芯片所提供的樣本預(yù)處理功能能夠較好地滿足上下游檢測(cè)分析的需要,防止交叉污染、減少細(xì)胞黏附等傳統(tǒng)細(xì)胞處理方法中常見的問(wèn)題,具有較廣闊的應(yīng)用場(chǎng)景,對(duì)于腫瘤研究具有重要意義。
審核編輯:劉清
-
微流控芯片
+關(guān)注
關(guān)注
13文章
249瀏覽量
18747 -
3D打印技術(shù)
+關(guān)注
關(guān)注
4文章
219瀏覽量
31825 -
微流控系統(tǒng)
+關(guān)注
關(guān)注
1文章
60瀏覽量
1840
原文標(biāo)題:利用微流控芯片高通量收集血液中的循環(huán)腫瘤細(xì)胞,可用于早期癌癥檢測(cè)
文章出處:【微信號(hào):Microfluidics-Tech,微信公眾號(hào):微流控科技】歡迎添加關(guān)注!文章轉(zhuǎn)載請(qǐng)注明出處。
發(fā)布評(píng)論請(qǐng)先 登錄
相關(guān)推薦
寬帶功率放大器基于微流控技術(shù)的細(xì)胞分選的應(yīng)用
液滴微流控技術(shù)在癌癥研究中的應(yīng)用:從單細(xì)胞分析到3D細(xì)胞培養(yǎng)
基于微流控的納米細(xì)胞芯片,用于肺癌免疫治療的精準(zhǔn)預(yù)測(cè)

安泰ATA-7050高壓放大器在微流控細(xì)胞分選中的應(yīng)用
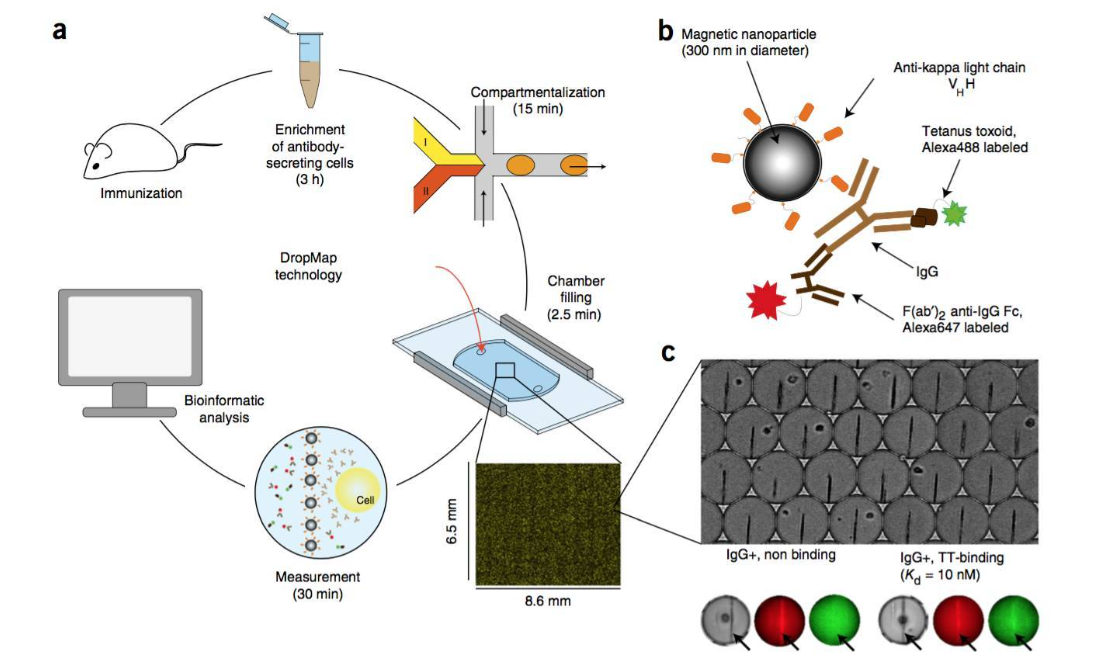
高通量測(cè)序技術(shù)及原理介紹
基于離子濃度極化的微流控平臺(tái)用于ctDNA的高靈敏度檢測(cè)

基于磁性探針的級(jí)聯(lián)相轉(zhuǎn)移微流控芯片用于循環(huán)腫瘤細(xì)胞檢測(cè)

LabVIEW進(jìn)行癌癥預(yù)測(cè)模型研究
基于液滴微流體的微流控芯片系統(tǒng)的研究
功率放大器應(yīng)用分享:微流控細(xì)胞分選在軟骨芯片關(guān)節(jié)炎治療中應(yīng)用
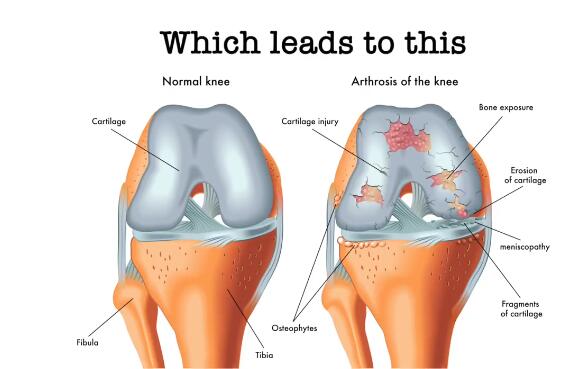
一種用于富集循環(huán)腫瘤細(xì)胞的螺旋微流控芯片設(shè)計(jì)

利用慣性-磁微流控技術(shù)實(shí)現(xiàn)惡性腫瘤細(xì)胞的快速、高純度分離
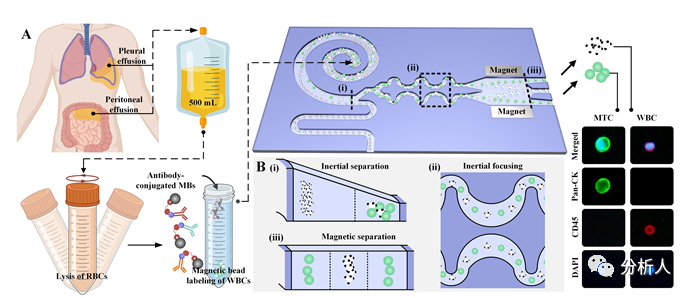
微流控技術(shù)為高通量藥物發(fā)現(xiàn)提供與人體生理學(xué)相關(guān)的細(xì)胞模型

如何利用微圖案化芯片實(shí)現(xiàn)高通量細(xì)胞篩選中程序化藥物添加




 利用微流控芯片高通量收集血液中的循環(huán)腫瘤細(xì)胞檢測(cè)癌癥
利用微流控芯片高通量收集血液中的循環(huán)腫瘤細(xì)胞檢測(cè)癌癥










評(píng)論