細(xì)胞通過限制性三維遷移可導(dǎo)致核包膜完整性喪失、DNA損傷和基因不穩(wěn)定。盡管有這些有害的現(xiàn)象,暫時(shí)暴露在封閉環(huán)境中的細(xì)胞通常不會(huì)死亡。目前,這是否也適用于受到長(zhǎng)期禁錮的細(xì)胞仍不清楚。近日,來自美國奧本大學(xué)的Panagiotis Mistriotis教授團(tuán)隊(duì)進(jìn)行了通過下調(diào)YAP活性限制P53過度激活以促進(jìn)細(xì)胞在封閉中存活的相關(guān)研究。研究成果以“Downregulation of YAP Activity Restricts P53 Hyperactivation to Promote Cell Survival in Confinement”為題發(fā)表在Advanced Science期刊上。
在該項(xiàng)研究中,研究人員采用了光刻和微流控技術(shù)制造一個(gè)高通量的器件,該器件規(guī)避以前細(xì)胞封閉模型的限制,并能在生理相關(guān)尺度的微通道中長(zhǎng)期培養(yǎng)單細(xì)胞。這項(xiàng)研究的結(jié)果表明,連續(xù)暴露在嚴(yán)格的封閉環(huán)境中會(huì)引發(fā)頻繁的核包膜破裂,反過來又會(huì)促進(jìn)P53的激活和細(xì)胞凋亡。遷移的細(xì)胞最終會(huì)適應(yīng)密閉,并通過下調(diào)YAP活性來逃避細(xì)胞死亡。YAP活性的降低是封閉誘導(dǎo)YAP1/2轉(zhuǎn)位到細(xì)胞質(zhì)的結(jié)果,抑制了核包膜破裂的發(fā)生率,并廢除P53介導(dǎo)的細(xì)胞死亡。總之該研究建立了先進(jìn)、高通量的生物模擬模型,以更好理解健康和疾病中的細(xì)胞行為,并強(qiáng)調(diào)環(huán)境線索和機(jī)械傳導(dǎo)途徑在調(diào)節(jié)細(xì)胞生命和死亡中的關(guān)鍵作用。
光刻和微流控技術(shù)在生理尺寸微通道中禁錮細(xì)胞
將微流控技術(shù)與光刻圖案化結(jié)合起來,從而能夠研究長(zhǎng)期三維封閉如何影響細(xì)胞行為。研究人員首先建立了一個(gè)平行微通道陣列,其尺寸模仿體內(nèi)遷移細(xì)胞遇到的通道狀軌道或微血管的大小。與這些微通道垂直的是兩個(gè)較大的、類似于二維的通道,作為細(xì)胞和培養(yǎng)基的儲(chǔ)存器。通過應(yīng)用PRIMO光刻技術(shù)和光活化試劑PLPP,降解了襯在微通道壁上的防粘層,并使用ECM蛋白涂覆。接著將細(xì)胞引入微流控器件,在入口和出口之間產(chǎn)生一個(gè)壓力差,促使細(xì)胞流經(jīng)最下層的二維類通道。盡管細(xì)胞未能粘附在用PLL-mPEG-SVA處理的通道上,但它們卻附著在膠原蛋白I光刻圖案微通道的入口附近。在趨化作用下,細(xì)胞進(jìn)入用光刻的微通道。接下來,研究人員量化了細(xì)胞進(jìn)入后留在微通道內(nèi)的細(xì)胞比例。結(jié)果發(fā)現(xiàn),細(xì)胞在光刻圖案微通道中的夾帶效率達(dá)到80% ~ 95%,并且與幾何形狀無關(guān)。相比之下,膠原蛋白I涂層的器件,有利于細(xì)胞通過微通道遷移。總之,將微流控技術(shù)與光刻技術(shù)相結(jié)合,可以開發(fā)出一種平臺(tái)技術(shù),實(shí)現(xiàn)在規(guī)定尺寸微通道中對(duì)單細(xì)胞進(jìn)行長(zhǎng)期培養(yǎng)。
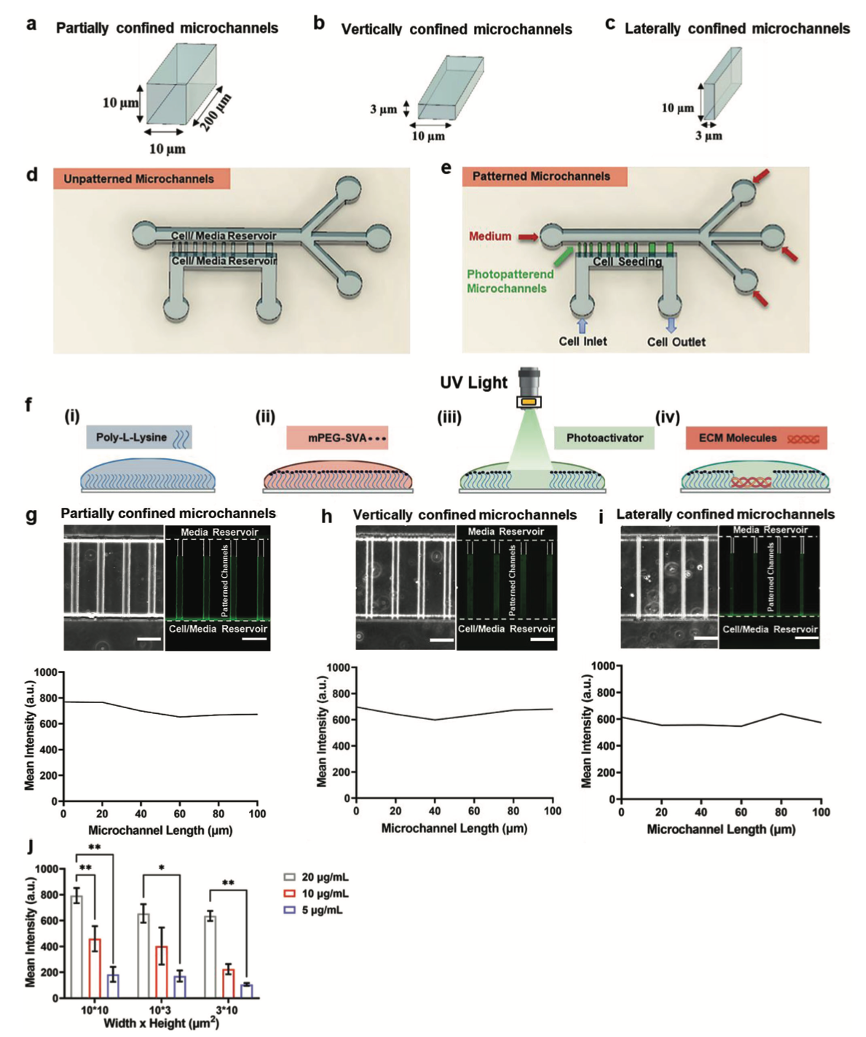
圖1 利用光刻技術(shù)在微通道壁上沉積ECM
封閉環(huán)境中的細(xì)胞分裂和死亡
接下來,對(duì)部分、全部和橫向封閉的微通道內(nèi)的細(xì)胞分裂和存活率進(jìn)行量化。作為二維對(duì)照,采用橫截面積為400μm × 50 μm的膠原蛋白I涂層通道。在封閉的微環(huán)境中,相對(duì)于二維對(duì)照,18小時(shí)內(nèi)分裂的細(xì)胞比例減少。在細(xì)胞禁錮的后期細(xì)胞增殖減少。同時(shí),大多數(shù)未分裂的細(xì)胞在封閉60小時(shí)后顯示其縱向面積增加。雖然細(xì)胞在非封閉和部分封閉微環(huán)境中保持較高的活力,但垂直而非橫向的封閉會(huì)誘發(fā)細(xì)胞死亡。通過監(jiān)測(cè)與FITC共軛的牛血清白蛋白(BSA)的擴(kuò)散,驗(yàn)證了垂直封閉的細(xì)胞可以獲得營養(yǎng)物質(zhì)。表明細(xì)胞系之間對(duì)封閉誘導(dǎo)的細(xì)胞死亡的敏感性是不同的。為了將本文研究結(jié)果從基于PDMS的微機(jī)制擴(kuò)展到更易受外界影響的生物環(huán)境,使用具有不同硬度和孔徑的三維膠原蛋白水凝膠基質(zhì)。將HT-1080纖維肉瘤細(xì)胞包裹在柔軟的、平均孔徑1.5 μm的水凝膠中,在3天的培養(yǎng)中支持細(xì)胞增殖、擴(kuò)散和生存。相反,僵硬的水凝膠與減少的孔徑損害了細(xì)胞伸長(zhǎng),阻礙了細(xì)胞生長(zhǎng),并促進(jìn)細(xì)胞死亡。這些發(fā)現(xiàn)表明,細(xì)胞死亡可能發(fā)生在具有生理學(xué)相關(guān)力學(xué)的封閉微環(huán)境中。
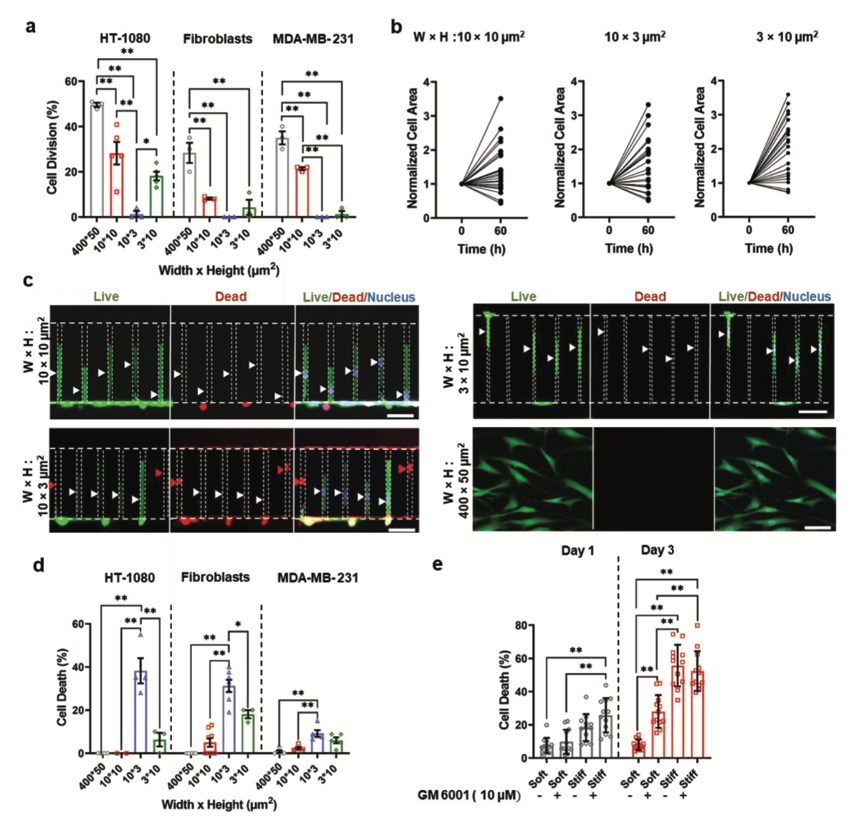
圖2 三維封閉調(diào)控細(xì)胞分裂和細(xì)胞死亡
垂直封閉中P53激活引發(fā)細(xì)胞凋亡
為了確定封閉促進(jìn)細(xì)胞死亡的機(jī)制,該研究分析了部分和垂直封閉微通道中皮膚成纖維細(xì)胞或HT-1080細(xì)胞表型。垂直封閉成纖維細(xì)胞在禁錮1或3天后有60%的膜出血。在垂直封閉的HT-1080細(xì)胞中,膜出血的程度更加明顯。在禁錮一天后,80%的細(xì)胞顯示出血的表型。在部分封閉的微通道中,無論細(xì)胞類型如何,都沒有膜出血現(xiàn)象。用熒光延時(shí)監(jiān)測(cè)HT-1080細(xì)胞表達(dá)肌動(dòng)蛋白和組蛋白2B情況。結(jié)果發(fā)現(xiàn)碎裂細(xì)胞核的百分比隨著時(shí)間的推移而增加,18小時(shí)后達(dá)到20%。大多數(shù)垂直封閉的細(xì)胞在細(xì)胞死亡期間增加了caspase-3/7的活性。相反,保持活力的垂直封閉細(xì)胞或部分封閉的細(xì)胞未能激活這些蛋白酶。這些數(shù)據(jù)顯示,垂直封閉主要通過誘導(dǎo)細(xì)胞凋亡來保證細(xì)胞的活力。當(dāng)核包膜完整性受到損害時(shí),會(huì)滲漏到細(xì)胞質(zhì)中。與存活的細(xì)胞相比,最終死亡的夾層細(xì)胞中NERs的嚴(yán)重程度更為明顯。相反,在支持細(xì)胞存活的部分或橫向封閉的微通道中,NER的頻率和經(jīng)歷NER細(xì)胞的比例明顯減少。總的來說,這些發(fā)現(xiàn)表明,垂直封閉促進(jìn)了核包膜完整性的頻繁喪失,反過來又誘導(dǎo)了P53依賴的DNA損傷反應(yīng),從而使細(xì)胞凋亡。
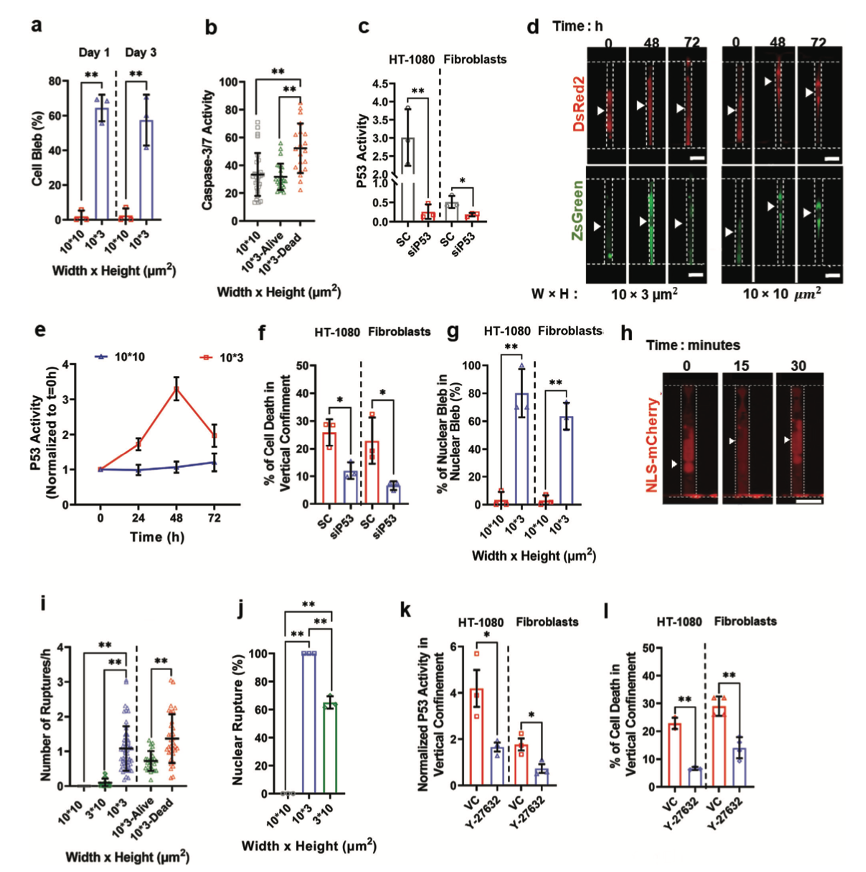
圖3 垂直封閉中P53激活引發(fā)細(xì)胞凋亡
YAP進(jìn)入細(xì)胞質(zhì)通過降低NER和P53活性發(fā)生率促進(jìn)細(xì)胞對(duì)封閉環(huán)境適應(yīng)
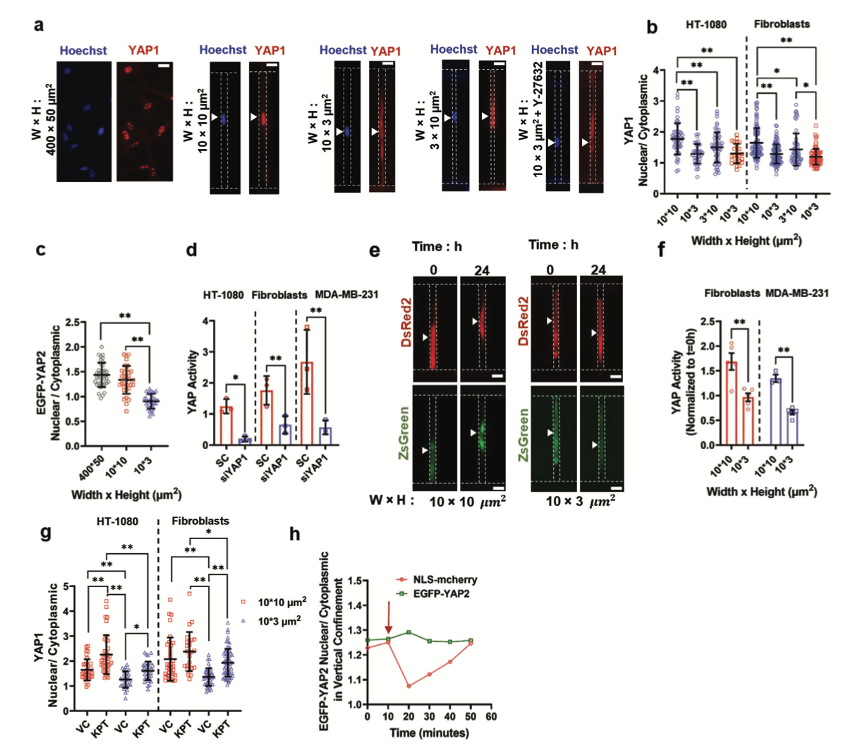
圖4 封閉誘導(dǎo)的YAP進(jìn)入細(xì)胞質(zhì)中,降低YAP的活性
一部分成纖維細(xì)胞和HT-1080細(xì)胞能夠適應(yīng)垂直封閉并存活。此外P53活性在第3天有所下降,這表明存在一種機(jī)制來限制P53依賴的促凋亡途徑激活。使用免疫熒光法,發(fā)現(xiàn)在細(xì)胞進(jìn)入垂直而非部分封閉的微通道后,機(jī)械傳導(dǎo)因子YAP1立即轉(zhuǎn)入HT-1080細(xì)胞和成纖維細(xì)胞的細(xì)胞質(zhì)中。禁錮24小時(shí)后,還觀察到Y(jié)AP1的細(xì)胞質(zhì)定位增加。YAP1和YAP2可以通過與TEAD轉(zhuǎn)錄因子相關(guān)聯(lián)來調(diào)節(jié)基因表達(dá)。因此,將YAP/TEAD-RE(ACATTCCA)亞克隆到LVDP載體,以量化YAP的轉(zhuǎn)錄活性。YAP轉(zhuǎn)錄活性的量化顯示,在細(xì)胞進(jìn)入微通道后24小時(shí),相對(duì)于部分封閉的成纖維細(xì)胞,垂直封閉的成纖維細(xì)胞顯示出YAP依賴的基因表達(dá)減少。在攜帶突變體P53基因的MDA-MB-231細(xì)胞中也有類似的減少,表明P53沒有介導(dǎo)觀察到的YAP活性下降。接下來研究了禁閉如何改變YAP的亞細(xì)胞分布。使用Exportin 1抑制劑處理部分和垂直封閉的細(xì)胞。核包膜破裂參與觸發(fā)YAP轉(zhuǎn)位到細(xì)胞質(zhì),抑制NER的側(cè)向封閉將促進(jìn)YAP的核累積。這些數(shù)據(jù)表明,RhoA/ROCK途徑控制YAP核上質(zhì)運(yùn)輸,與NER無關(guān),可能是通過抑制Exportin 1介導(dǎo)的YAP1核出口。
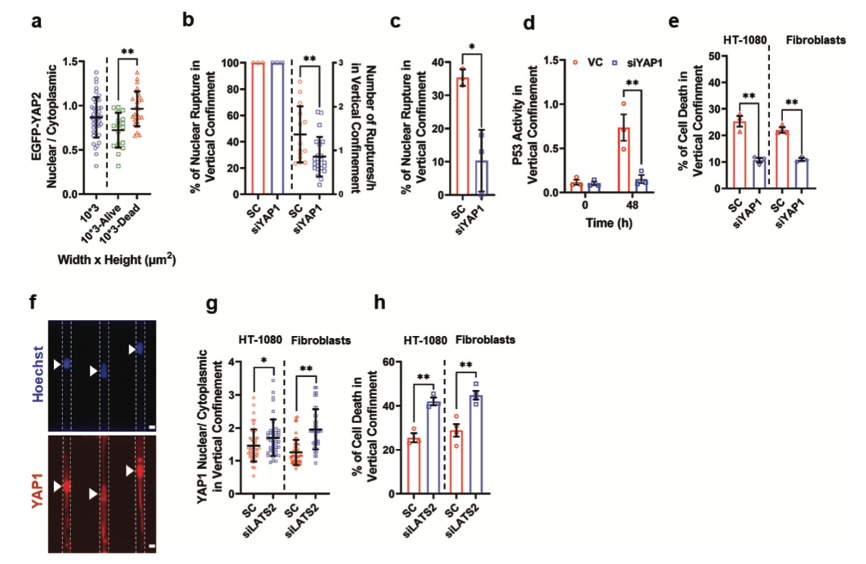
圖5 細(xì)胞質(zhì)中YAP積累支持細(xì)胞在封閉狀態(tài)下的存活
以上研究表明YAP到細(xì)胞質(zhì)出口可以由活躍的核出口機(jī)制調(diào)節(jié),而不是由NER調(diào)節(jié)。YAP的構(gòu)成性激活已證明會(huì)損害核膜的完整性。這些發(fā)現(xiàn)促使研究人員假設(shè),禁閉誘導(dǎo)YAP進(jìn)入細(xì)胞質(zhì)中,抑制YAP依賴的轉(zhuǎn)錄活動(dòng),最終減少了NER、P53活性和細(xì)胞死亡的頻率。與這一假設(shè)一致,該研究證明垂直封閉的HT-1080細(xì)胞仍然存活,相對(duì)于那些死亡的細(xì)胞,EGFP-YAP2的核水平降低。此外,該研究發(fā)現(xiàn)用siYAP1處理的垂直封閉的HT-1080細(xì)胞的細(xì)胞核相對(duì)于對(duì)照細(xì)胞的細(xì)胞核破裂頻率較低。YAP1敲除也抑制發(fā)生NER成纖維細(xì)胞的比例,并減少了P53的激活。這種干預(yù)促進(jìn)兩種細(xì)胞類型在垂直封閉中的生存能力。相反,用針對(duì)LATS2的siRNA轉(zhuǎn)染HT-1080細(xì)胞和皮膚成纖維細(xì)胞,使YAP磷酸化和失活,明顯增加YAP1的核水平,并加劇封閉誘導(dǎo)的細(xì)胞死亡。總而言之,該研究數(shù)據(jù)表明,YAP活性的下調(diào)有助于細(xì)胞對(duì)封閉適應(yīng),從而使細(xì)胞存活。
綜上所述,該研究利用微流控實(shí)驗(yàn)和成像工具,證明了封閉的幾何形狀和等級(jí)控制著遷移細(xì)胞的生長(zhǎng)和生存。在封閉微環(huán)境中,腫瘤抑制因子P53是控制細(xì)胞存活和死亡的關(guān)鍵因素。YAP在調(diào)節(jié)NER和P53活性中具有關(guān)鍵作用,介導(dǎo)細(xì)胞對(duì)封閉環(huán)境的適應(yīng)。該研究對(duì)癌癥治療有更廣泛的意義,因?yàn)樗a(chǎn)生了關(guān)于遷移腫瘤細(xì)胞如何感知和應(yīng)對(duì)長(zhǎng)期三維封閉的新理念。已有研究表明,循環(huán)腫瘤細(xì)胞被困在封閉微血管中與細(xì)胞活力的降低有關(guān)。因此,制定策略以提高細(xì)胞對(duì)封閉反應(yīng)能力可能是抑制血管內(nèi)腫瘤細(xì)胞生存的一種新方法。
審核編輯:劉清
-
微流控芯片
+關(guān)注
關(guān)注
13文章
267瀏覽量
18817 -
光刻機(jī)
+關(guān)注
關(guān)注
31文章
1147瀏覽量
47270 -
PLL電路
+關(guān)注
關(guān)注
0文章
92瀏覽量
6397 -
微流控系統(tǒng)
+關(guān)注
關(guān)注
1文章
66瀏覽量
1862
原文標(biāo)題:光刻圖案化+微流控技術(shù),用于封閉環(huán)境下細(xì)胞行為和機(jī)制的研究
文章出處:【微信號(hào):Micro-Fluidics,微信公眾號(hào):微流控】歡迎添加關(guān)注!文章轉(zhuǎn)載請(qǐng)注明出處。
發(fā)布評(píng)論請(qǐng)先 登錄
相關(guān)推薦
HyperLith軟件 EUV光刻交流
Aigtek高壓放大器在介電泳的微流控細(xì)胞分離技術(shù)中的應(yīng)用
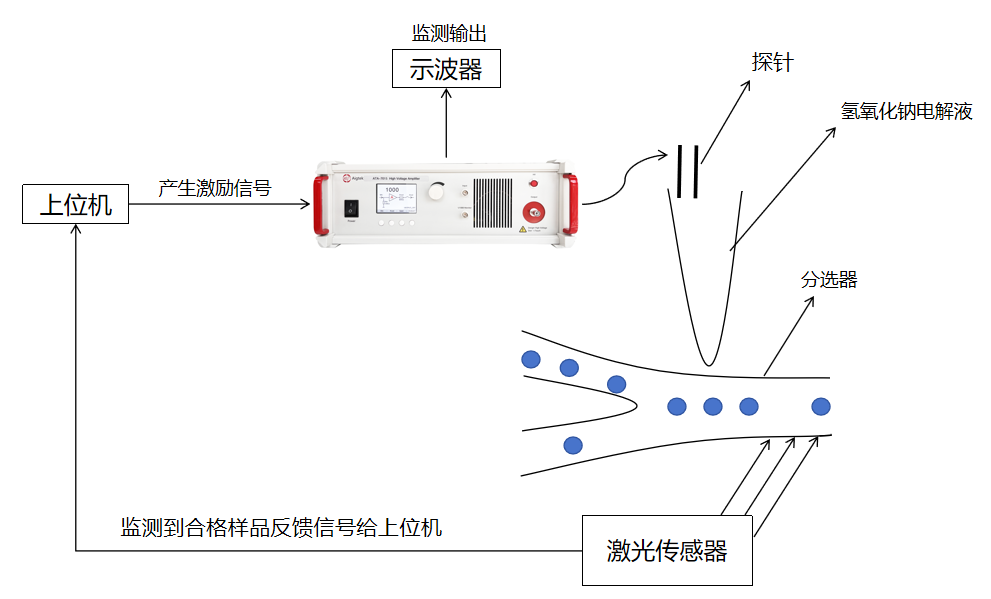
ATA-7020高壓放大器在微流控3D細(xì)胞微球培養(yǎng)中的應(yīng)用
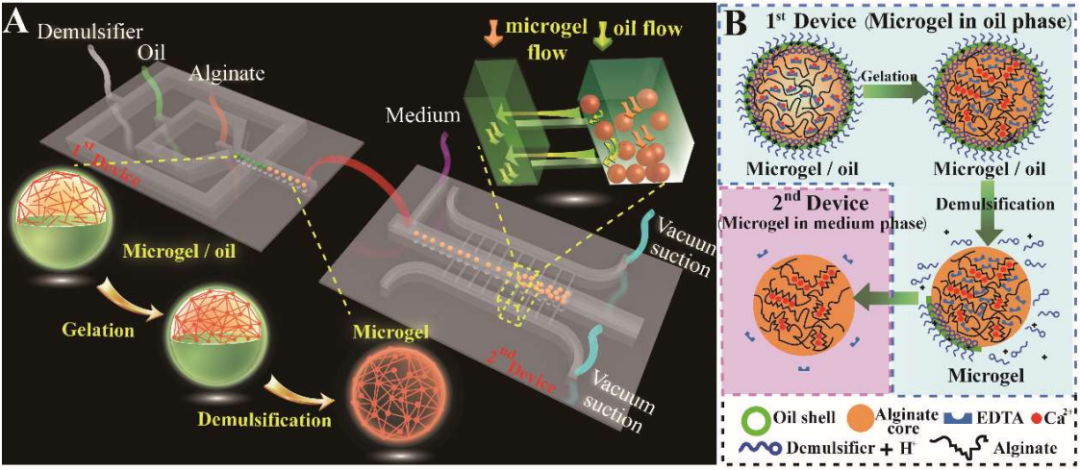
深視智能高速攝像機(jī)在液滴微控流實(shí)驗(yàn)中的應(yīng)用

微流控芯片3大制作技術(shù)
如何成功的烘烤微流控SU-8光刻膠?
如何成功的旋涂微流控SU-8光刻膠?
微流控光刻掩膜制作
微流控芯片技術(shù)的特點(diǎn) 微流控芯片與生物芯片的區(qū)別
基于雙極性電極的微流控芯片,用于生物顆粒和細(xì)胞分選
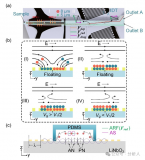
如何利用磁性微流控系統(tǒng)實(shí)現(xiàn)免疫細(xì)胞分泌行為的定量檢測(cè)呢?
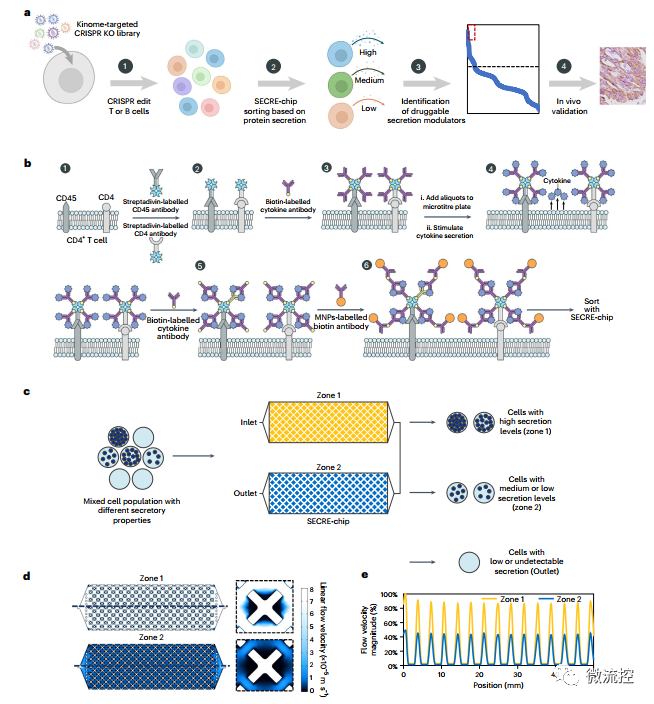
基于微流控技術(shù)的微納米馬達(dá)用于遞送神經(jīng)干細(xì)胞和恢復(fù)神經(jīng)連通性




 光刻圖案化+微流控技術(shù)用于封閉環(huán)境下細(xì)胞行為和機(jī)制的研究
光刻圖案化+微流控技術(shù)用于封閉環(huán)境下細(xì)胞行為和機(jī)制的研究










評(píng)論