心臟是人體中一個復雜而重要的器官,具有心臟毒性的藥物如烏頭堿等嚴重制約了其臨床應用,建立合適的三維(3D)體外心臟模型有助于探究烏頭堿的心臟毒性機制,指導臨床安全用藥。
通過液滴微流控技術制備的多隔室心臟顆粒模型具有低成本、高靈活性和高通量的特點,是應用于藥物心臟毒性機制研究的理想模型。
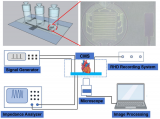
近日,清華大學林金明教授帶領研究團隊與成都中醫藥大學張藝教授團隊合作,制備了一種具有操作簡便、無標記檢測和可控性強等特點的六隔室心臟顆粒,并通過液相色譜-質譜聯用儀(LC-MS)檢測了烏頭堿心臟毒性反應下的細胞代謝物,以及利用分子生物學技術評估了烏頭堿刺激后心臟毒性相關指標的表達,最后總結了烏頭堿的心臟毒性機制。
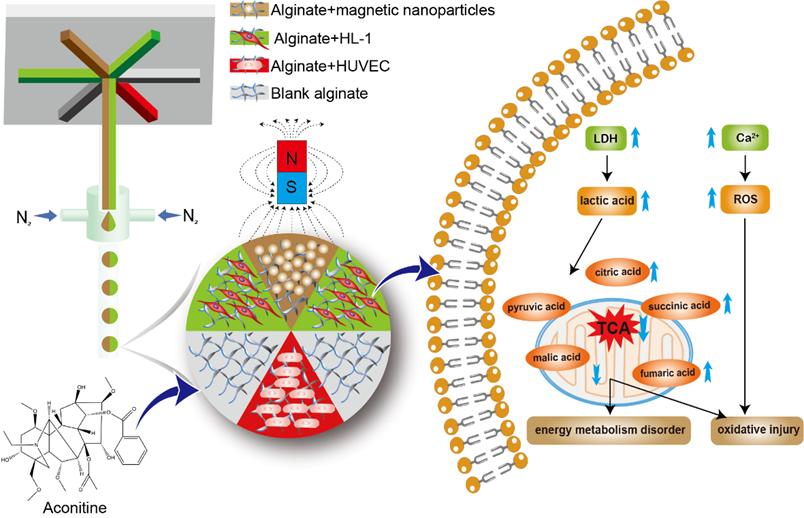
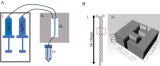
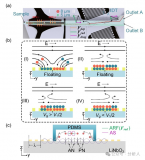
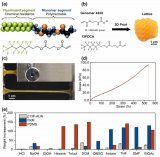
該工作設計的微流控裝置制備了由HL-1和HUVEC細胞3D共培養的六隔室心臟顆粒模型,該模型用磁顆粒定位,在不需要標記的情況下能夠清楚地觀察到每個隔室的細胞狀態。此外,研究人員通過LC-MS和分子生物學技術發現烏頭堿能夠破壞細胞膜結構引起乳酸脫氫酶(LDH)外滲和Ca2?超載,從而抑制三羧酸(TCA)循環,導致能量代謝紊亂和氧化損傷,最終引發心肌細胞凋亡。
這些結果提供了一種新型的體外心臟模型以及藥物的安全研究策略。該成果以“Evaluation of aconitine cardiotoxicity with aheart-on-a-particle prepared by a microfluidic device”為題,發表在英國皇家化學會期刊ChemicalCommunications上,并入選為hot article。
論文鏈接:
https://doi.org/10.1039/D4CC00396A
-
色譜儀
+關注
關注
0文章
39瀏覽量
11361 -
微流控
+關注
關注
16文章
513瀏覽量
18863
原文標題:3D)
文章出處:【微信號:Micro-Fluidics,微信公眾號:微流控】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
高通量生物分析技術之微流控芯片
微流控芯片3大制作技術
激光焊接技術在焊接醫療心臟射頻消融導管的工藝應用

綜述:基于微流控技術的氧釋放生物材料的制備與應用研究進展
優可測白光干涉儀AM-7000系列測量心臟支架表面粗糙度應用案例





 利用微流控技術制備的“心臟顆粒”,用于評估藥物的心臟毒性
利用微流控技術制備的“心臟顆粒”,用于評估藥物的心臟毒性












評論